
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Выявление и оценка систематической погрешности измерений, по данным выборочного контроля качества установочного вещества
|
|
|
|
Цель и сущность работы. Как показано в гл.1 (разд.1.7), по формулам нормального статистического распределения невозможно оценить численное значение систематической погрешности измерений, так как ЗНР справедлив лишь для случайных отклонений от нормы. Однако несоответствие выборочной дисперсии ЗНР указывает на то, что имеет место значимая систематическая погрешность измерений, которую нетрудно устранить, если выявить причину и источник систематической погрешности.
В данной работе показана возможность выявления систематической погрешности, по результатам статистических исследований и оценок, с применением методов и средств нормальной статистики гауссова распределения.
Объектом статистического исследования был выбран тетраборат натрия, Na2B4O7 10H2O (бура) - установочное вещество, используемое, в качестве эталона, в титриметрическом анализе, а именно, в методе нейтрализации.
Основным требованием, предъявляемым к установочным веществам, является строгое соответствие молекулярной массы и химической формулы. Если указанное требование не выполняется, то возникает источник значимой систематической погрешности результатов анализа. Если для приготовления эталонного раствора буры, при взятии навески, был использован кристаллогидрат соли, из которого выветрилась часть молекул воды, то эталонный раствор данного установочного вещества будет приготовлен неверно, с иным содержание буры, чем это было рассчитано.
Неверно приготовленный эталонный раствор установочного вещества, безусловно, становится источником систематической погрешности результатов титриметрического анализа, так как при установлении титра рабочего раствора кислоты по неправильному эталону систематическая погрешность автоматически переносится на указанный рабочий раствор, используемый в аналитическом контроле производства.
|
|
|
Для того, чтобы предотвратить ошибки аналитических определений в заводской лаборатории (ЗЛ), следует устранить первоисточник данной систематической погрешности. Но для этого, потребуется сопоставить две выборочные дисперсии, полученные, по результатам титрования стандартным раствором HCl сомнительного раствора буры и эталонного раствора, приготовленного из фиксанала.
Порядок выполнения работы. Две бюретки на 50 мл заполняются одинаковым стандартным раствором хлороводородной кислоты. Обе устанавливаются на нуль, по нижнему краю мениска жидкости. С помощью измерительной пипетки, в две чистые конические колбы для титрования помешают одинаковые аликвоты (20 мл) указанных растворов эталонной и сомнительной буры. Добавляют по 50 мл дистиллированной воды и по 3 капли кислотно-основного индикатора - метилового оранжевого.
Оба раствора титруют 0,1 М раствором HCl, до перехода окраски титруемого раствора с желтой на розовую. В момент перехода окраски раствора, по шкале бюретки, фиксируется, с точностью 0,05 мл, расход титранта в конечной точке титрования (КТТ). Результаты определений записываются в лабораторный журнал, а затем, выполняют повторные определения, в той же последовательности. Всего, требуется выполнить по 10 параллельных определений, т.е. получить две выборочных дисперсии (S 21 и S 22), с объемом выборки n = 10.
После этого, приступают к статистическим исследованиям двух серий измерений, по алгоритмам, указанным в разд.7, гл.1. По ним, устанавливают значимое различие средних арифметических результатов двух серий измерений: x m 1 и x m 2, где: x m 1 – среднее арифметическое эталонной серии, в которой заведомо отсутствует систематическая погрешность; x m 2 – среднее арифметическое результатов сомнительной серии аналитических измерений.
|
|
|
Статистическое сопоставление результатов двух серий измерений позволяет выявить и оценить систематическую погрешность, по следующей схеме:
1. Для каждой из двух серий измерений, выполненных в одинаковых условиях, вычисляют величины x m 1 и x m 2, численные значения которых могут существенно отличаться друг от друга. Но если далее будет доказано (по критерию Фишера), что все измерениях равноточны, то потребуется, лишь установить, является ли указанное различие средних значений значимым. Если да, то имеет место значимая систематическая погрешность измерений.
2. Вычисляют численные значения величин выборочной дисперсии S 2 для эталонной (S 12) и сомнительной (S 22) серии титриметрических определений, по формуле:
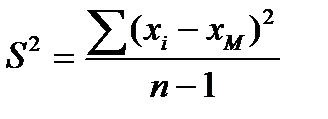 (1)
(1)
3. Численное значение F -критерия равноточности находят по соотношению указанных выборочных дисперсий: F = S 12 / S 22 или F = S 22 / S 12. Принимается значение F >1. Расчетный критерий Фишера F сопоставляют с F таб, взятым из табл.3 ПРИЛОЖЕНИЯ, с вероятностью α =0,95, при равном объеме выборки (n 1 = n 2). Результаты измерений считаются равноточными, если выполняются условия следующего неравенства: F < F таб.
4. Далее, потребуются оценить условия совместности результатов измерений для двух указанных выборочных дисперсий. Для этого уже потребуется вычислить численное значение t* - критерия по формуле:
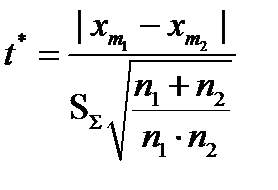 , (2)
, (2)
Где: S∑ - стандартное отклонение обобщенной выборки, вычисляемое по формуле:
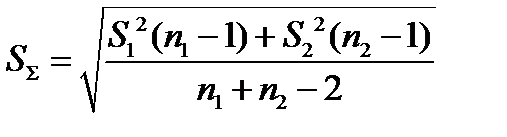 . (3)
. (3)
Расчетный критерий t * сопоставляют с табличным критерием t α,f , взятым из табл.2 Приложения, при данном числе степеней свободы f = n 1+ n 2 -2 и доверительной вероятности α = 0,95. Если t* > t α,f ., то имеет место значимое расхождение средних арифметических xm1 и xm2. Наблюдаемое в условиях равноточности, значимое расхождение xm1 и xm2, однозначно, указывает на систематическую погрешность результатов выборочного контроля. Ее численное значение, Q,% можно вычислить по формуле:
Q,% = (xm2 – xm1) 100 / x m 1 (4)
Где, xm1 - среднее арифметическое результатов измерений эталонной серии.
По результатам выполненной работы делается аргументированный вывод, где указывается источник значимой систематической погрешности, выявленной по результатам выборочного контроля качества установочного вещества.
|
|
|
Оформляется отчет, в котором приводятся данные, позволяющие обосновать полученные результаты и выводы, относительно равноточности результатов измерений и совместности сравниваемых выборочных дисперсий.
4.1.4. Лабораторная работа № 4
Проверка совместности двух аттестованных методик определения содержания железа в растворе соли Мора
Цель и сущность работы. В данной работе, как и в предыдущей работе № 3 сопоставляются две выборочные дисперсии результатов титриметрического анализа, с целью выявления их равноточности и совместности. Как и в предыдущей работе, проверку на равноточность результатов измерений осуществляют по F -критерию (критерию Фишера), а проверка на совместность двух выборочных дисперсий S 12 и S 22 и, возможности их объединения в единый вариационный ряд однородных результатов измерений осуществляется, по той же схеме, как и в работе № 3, где сначала, по уравнениям (2) и (3), вычисляют критерий t *. Затем, его сравнивают с табличным критерием t таб для объединенной выборки n = n 1 + n 2, где по условию выполнения неравенства t *< t таб доказано, что средние арифметические выборочных дисперсий незначимо отличаются друг от друга, а указанные дисперсии совместны.
Алгоритмы вычислений в работах №3 и №4 одинаковы. Поэтому, чтобы избежать повторов, в работе №4 даются ссылки на расчетные формулы (1-3), используемые в предыдущей работе. Отличие состоит лишь в том, что здесь не требуется выявлять, а затем оценивать систематическую погрешность измерений. Это невозможно, так как здесь отсутствует “эталонная дисперсия”, с которой можно сравнить исследуемую выборочную дисперсию, с целью выявления систематической погрешности измерений.
В данной работе поставлена цель, установить совместность двух методик выполнения измерений (МВИ), а именно, методик перманганатометрического и хроматометрического определения железа в соли Мора. Если доказано, что указанные МВИ совместны, то это позволяет, в случае необходимости, заменить одну методику на другую, без ущерба, в отношении достоверности результатов измерений.
|
|
|
Порядок выполнения работы. В данном случае, потребуется доказать совместность двух методик титриметрического определения железа в растворах электролитов, широко используемых в контроле, скажем, электрохимических производств, а именно, методик прямого перманганатометрического и хроматометрического титрование ионов Fe 2+, по реакциям окисления-восстановления:
5 Fe2+ + MnO4- + 8 H+ = 5 Fe3+ + Mn2+ + 4H2O
6 Fe2+ + Cr2O72- + 14 H+ = 6 Fe3+ + 2Cr3+ + 7H2O.
Подробное описание указанных операций титриметрического анализа дано в специальном МУ “Количественный химический анализ”. Здесь, в ходе выполнения экспериментальных работ потребуется получить две однородных серии равноточных результатов определения железа в соли Мора, двумя указанными способами.
Прочитав, методичку, студенты получают контрольное задание - исследуемый раствор соли Мора, помещенный в мерную колбу, на 250 мл, который доводится до метки дистиллированной водой и тщательно перемешивается.
Две чистых измерительных бюретки, на 50 мл, заполняются: одна -свежеприготовленным, стандартным раствором KMnO4 ; другая - стандартным раствором K2Cr2O7. Обе бюретки устанавливаются на нуль. На каждой из них нужно получить по 8 параллельных результатов титрования, с абсолютной погрешностью измерений расхода титранта, не превышающей 0,1 см3.
Для этого, каждый раз, измерительной пипеткой на 10 мл отбирают аликвоту исследуемого раствора соли Мора, помещая ее в чистую коническую колбу для титрования. Туда же, добавляют ответствующие реактивы и индикатор, указанные в МУ“Количественный химический анализ”, а также, около 50 см3 дистиллированной воды. Раствор в конической колбе титруют по каплям, при перемешивании, до резкого изменения окраски титруемого раствора от одной капли избытка титранта. Титрование прекращают и считывают по бюретке расход титранта до конечной точки титрования (КТТ) достижения конечной точки титрования (КТТ), записывают текущее значение объема титранта (VT) в таблицу результатов и пересчитывают его на массу железа в анализируемой пробе, по соответствующим расчетным формулам, указанным в МУ. Затем, снова устанавливают бюретку на нуль и повторяют анализ на содержание железа в аликвотной доле исследуемого раствора соли Мора.
В случае титрования перманганатом калия индикатор не требуется, так как сам титрант окрашен в малиновый цвет. От 1 капли избытка KMnO4 титруемый раствор приобретает розовую окраску, что позволяет фиксировать КТТ без индикатора. Но при титровании ионов железа дихроматом калия уже потребуется ред-окс индикатор, в данном случае, дифениламин, который вблизи КТТ меняет окраску почти бесцветного титруемого раствора на ярко синюю.
Обе указанных методики определения железа стандартизованы и они широко используются в практике аналитического контроля производства, где иногда приходится менять одну МВИ на другую и возникает необходимость в метрологической оценке их совместности. Это и является целью данной работы.
Как указано выше, МВИ могут быть совместными, если средние арифметические xm1 и xm2 полученных результатов двух выборочных дисперсий, с n 1= n 2=8, не отличаются значимо друг от друга, что можно выявить, путем их статистического исследования, по алгоритмам, описание которых дано в лаб. работе №3.
Здесь, как и в предыдущей работе сопоставляются результаты двух серий результатов титрования, полученных в одинаковых условиях, с одинаковым качеством измерений. Но в отличие от лаб. работы № 3, в данном случае, сравниваются две разных МВИ, но объект измерения одинаков.
По результатам титрования, двумя указанными способами порций (аликвот) раствора соли Мора, получают две серии параллельных определений массы железа в титруемом растворе - две выборочных дисперсии, с выборкой n = 8.
Результаты двух титрований исследуются методами нормальной статистики, где сначала вычисляются величины средних арифметических xm1 и xm2 двух выборочных дисперсий S 12 и S 22 и F -критерий равноточности (см.раб.№3).
По условиям неравенства F <F таб устанавливают насколько равноточны результаты измерений двумя указанными способами. Если расчетный критерий Фишера меньше табличного, то из этого следует, что измерения равноточны, а случайной погрешностью измерений можно пренебречь.
Для того, чтобы выявить насколько значимым является различие средних, что позволяет судить о совместности сравниваемых методик выполнения измерений (МВИ), потребуется вычислить сложный t *-критерий (см. ф.2 и 3, лаб.раб.№3) и сопоставить его с табличным критерием Стьюдента (табл.2 Прилож.), при f = n 1+ n 2-2 и α = 0,95
Условия выполнения неравенства t *< t таб, доказывают, что средние арифметические двух выборочных дисперсий не значимо отличаются друг от друга, а дисперсии совместны. Наоборот, если t * > t таб , то величины xm1 и xm2 отличаются значимо, а указанные МВИ титриметрического определения железа не могут быть совместными.
По результатам выполненной лабораторной работы студенты пишут отчет с аргументированным выводом, относительно совместности двух МВИ.
4.1.5. Лабораторная работа № 5
Оценка сходимости и воспроизводимости результатов измерений при метрологической аттестации МВИ
Сущность и цель работы. Сходимость и воспроизводимость результатов измерений является важнейшей метрологической характеристикой аттестуемой МВИ. В гл.1 (разд. 1.8) рассматривается четыре способа оценки воспроизводимости результатов измерений.
С целью численной оценки указанных метрологических показателей, в работе предлагается, пожалуй, наиболее простой способ их вычисления, через величину размаха выборочной дисперсии – R, который характеризует качество измерений, в отношении максимально возможных отклонений текущих значений вариант (v i) для некого вариационного ряда чисел от их среднего значения - v ср.
Хотя численные значения сходимости и воспроизводимости результатов измерений вычисляют по одной формуле: Р сх (Р восп) = Δ v / v ср, где: Δ v – разность (по модулю) между средним значением и максимальным (минимальным) текущим значением вариант, тем не менее следует различать указанные метрологические показатели.
Сходимость, это качество измерений, отражающее близость друг другу результатов контроля, полученных в одних условиях, т.е. в одной лаборатории, по одной МВИ.
Воспроизводимость -качество измерений, отражающее близость друг другу результатов выборочного контроля, полученных в разных условиях выполнения эксперимента, т.е. в разных лабораториях. Или в одной ЗЛ, но в разное время, при помощи разных приборов и инструментов, с использованием разных реактивов и т.д.
В данной работе предложено оценить численные значения величин сходимости и воспроизводимости результатов выборочного контроля, по величине размаха R, характеризующих вариационный ряд численных значений.
Для численной оценки величины сходимости Р сх, через величину размаха R, необходимо получить серию результатов выборочного контроля, составляющих некую выборочную дисперсию, где величину размаха вычисляют, как разность наибольшего и наименьшего результата измерений: R = v max - v min. А для оценки величины воспроизводимости, Р восп уже потребуется сопоставить выборочные дисперсии, полученные в разных условиях контроля двумя разными способами.
С целью экономии времени студентам предложено обрабатывать уже готовый пакет данных выборочного контроля, выдаваемых по указанию преподавателя. Так, полученные ранее результаты титриметрического определения железа в соли Мора (работа №4), также, могут быть использованы в лаб. работе №5, с целью оценки величин сходимости Р сх и воспроизводимости Р восп результатов выборочного контроля, по единой формуле:
Р сх = a (или b) / v ср100%, (1)
где медиану v ср вычисляют по уравнению v ср = (v max+ v min) /2, а параметры a и b, по формулам a = / v max – v ср/ и b = / v min – v ср/..
При расчете Р восп указанные величины a и b, как и v ср могут существенно отличаться от величин, ранее используемых при расчете Р сх. Поэтому, Р восп ≠ Р сх. Это объясняется тем, что в случае Р восп, величина размаха устанавливается сразу для двух выборочных дисперсий. Соответственно, могут изменяться величины a,b и v ср, влияющие на .величину Р восп.
По результатам выполненной лабораторной работы студенты оформляется отчет, где потребуется сделать аргументированный вывод, по полученным данным статистических исследований и оценок.
4.1.6. Лабораторная работа № 6
|
|
|
|
|
Дата добавления: 2014-11-29; Просмотров: 885; Нарушение авторских прав?; Мы поможем в написании вашей работы!