
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Термодинамические потенциалы. Изобарным термодинамическим потенциалом, или потенциалом Гиббса, называется величина
|
|
|
|
Изобарным термодинамическим потенциалом, или потенциалом Гиббса, называется величина
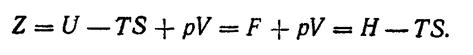 (2. 70)
(2. 70)
При обратимых изотермическом и изобарном процессах дифференцирование выражения (57.1) дает
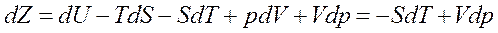 (так из основного закона термодинамики следует, что при изотермическом и изобарном процессах dU –TdS = -pdV). Термодинамический потенциал и свободная энергия имеют минимум при равновесном состоянии системы. При изохорном и изотермическом процессах
(так из основного закона термодинамики следует, что при изотермическом и изобарном процессах dU –TdS = -pdV). Термодинамический потенциал и свободная энергия имеют минимум при равновесном состоянии системы. При изохорном и изотермическом процессах
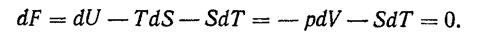 (142. 71)
(142. 71)
Свободная, энергия, энтальпия и внутренняя энергия являются термодинамическими потенциалами. Это следует из того, что при равновесных процессах, в которых остаются постоянными некоторые из параметров системы (т. е. при изотермических, изобарных и т. д. процессах), убывание термодинамических потенциалов равно совершаемой системой работе. При неравновесных процессах уменьшение термодинамических потенциалов больше совершаемой системой работы.
Дифференцированием уравнений (2.75), (2.73), (2.74) можно получить ряд важных соотношений. Действительно, из уравнения dF == — pdV — SdT следует, что
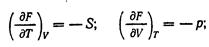
из уравнения dZ = — SdT + Vdp получим
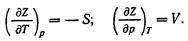
Так как dH == dU + pdV + Vdp = TdS + Vdp,
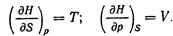
Из основного уравнения термодинамики TdS = = dU + pdV получим
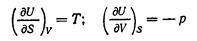
|
|
|
|
|
Дата добавления: 2014-01-14; Просмотров: 402; Нарушение авторских прав?; Мы поможем в написании вашей работы!