
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Класифікація за типом розриву хімічного зв’язку
|
|
|
|
Класифікація органічних реакцій
План
Лекція 2
Загальна органічна хімія (2)
- Класифікація органічних реакцій
- Ізомерія
• Структурна ізомерія
• Просторова ізомерія
· Гомолітичні реакції
В процесі реакції відбувається переміщення по одному електрону до кожного з атомів, що утворювали зв’язок. В результаті утворюються вільні радикали.

Для здіснення гомолітичних реакцій необхідна енергія або у вигляді теплоти, або за рахунок опромінювання світлом. Наприклад: хлор піддається гомолітичній реакції при нагріванні або освітленні світлом з певною довжиною хвилі, це призводить до утворення двох вільних радикалів:

Загальне рівняння гомолітичної реакції для зв’язку, що утворений карбоном:

Наприклад метан вступає в гомолітичну реакцію з утворенням метил радикалу і гідроген радикалу:
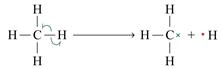
Вільний радикал – електронейтральний атом або група атомів, що містить неспарений електрон і має високу реакційну здатність завдяки нестабільній електронній конфігурації


Хлор радикал Метил радикал Гідроген радикал
В органічних молекулах розрізняють чотири типи атомів карбону:
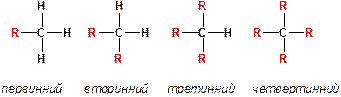 |
Третинні карборадикали більш стабільні завдяки стабілізації електронодонорними алкільними групами, що проявляють позитивний індуктивний ефект і ефект надспряження.
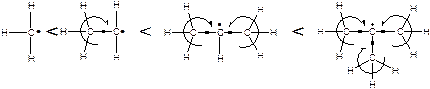 Чим більше алкільних груп, тим стабільніший карборадикал.
Чим більше алкільних груп, тим стабільніший карборадикал.
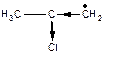 Електроноакцепторні групи дестабілізують карборадикал в результаті підвищення електронного дефіциту на центральному атомі карбону.
Електроноакцепторні групи дестабілізують карборадикал в результаті підвищення електронного дефіциту на центральному атомі карбону.
Якщо карбон з неспареним електроном зв’язаний з атомом в стані sp2-гібридизації або з гетероатомом, що має неподілену пару електронів, карборадикал стабілізується за рахунок делокалізації заряда в спряженій системі (р-π- або р-р-спряження)
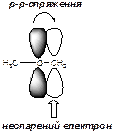

· Гетеролітичні реакції
В результаті реакції відбувається переміщення електронної пари до одного з атомів при цьому утворюються дві заряджені частинки – іони.
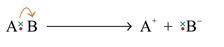
Гетеролітичні реакції відбуваються лише за умови поляризації зв’язку

Чим більше різниця в електронеготивностях атомів тим більша полярність зв’язку
Склад продуктів гетеролітичної реакції залежить від електронегативності атомів, що зв’язані з атомом карбону.
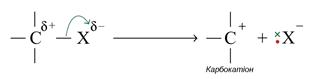
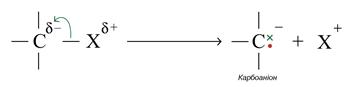
Третинні карбокатіони більш стабільні завдяки стабілізації електронодонорними алкільними групами, що проявляють позитивний індуктивний ефект і ефект надспряження. Як і у разі карборадикалів, чим більше алкільних груп, тим стабільніший карбокатіон.

трет -бутил ізопропіл етил метил
карбокатіон карбокатіон карбокатіон карбокатіон
 Електроноакцепторні групи дестабілізують карбокатіон в результаті підвищення електронного дефіциту на центральному атомі карбону.
Електроноакцепторні групи дестабілізують карбокатіон в результаті підвищення електронного дефіциту на центральному атомі карбону.
Якщо атом карбону, що має вільну орбіталь, зв’язаний з атомом в стані sp2-гібридизації або з гетероатомом, що має неподілену пару електронів відбувається стабілізація карбокатіону завдяки делокалізації заряду в спряженій ситтемі (р-π-спряження або р-р-спряження),
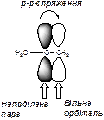

Третинні карбоаніони менш стабільні завдяки дестабілізації електронодонорними алкільними групами, що проявляють позитивний індуктивний ефект і ефект надспряження.
На відміну від карбокатионів і карборадикалів, чим більше алкільних груп, тим менш стабільний карбоаніон.
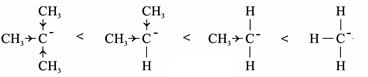
трет -бутил ізопропіл етил метил
карбоаніон карбоаніон карбоаніонкарбоаніон
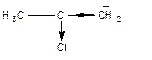 Електроноакцепторні групи стабілізують карбокатіон в результаті зменшення електронної густини на центральному атомі карбону.
Електроноакцепторні групи стабілізують карбокатіон в результаті зменшення електронної густини на центральному атомі карбону.
1.2 Класифікація за електронною природою атакуючого агенту
При розгляді типів механізмів реакцій умовно прийнято одну з реагуючих речовин називати субстратом, а другу – атакуючим реагентом.
Як правило субстратом вважають речовину із складнішою структурою, або молекули які надають атом карбону для утворення нового зв’язку.
Реакція електрофільна у разі коли атакуючий агент – електрофіл. Нуклеофільна – коли атакуючий агент – нуклеофіл.
Електрофіли
• Електрондифіцитні частинки, що мають схильність до приєднання електронів
• Мають вільну орбіталь (катіони), що приймає електронну пару, або неспарений електрон (радикали), що приймають електрон.
Нуклеофіли
• Частинки збагачені електронами, що схильні віддавати електрони в реакціях з електрофілами
• Мають неподілену пару електронів
• До них належать аніони або молекули з неподвленою парою електронів
| Електрофіл | Нуклеофіл | ||
| Катіон | Вільний радикал | Аніон | Молекула з неподіленою парою електронів |
| Br+, Cl+, NO2+, R+, RCO+, SO3H+ | H•, Br•, Cl•, I•, R•, HO•, CH2=CHCH2•, | Cl–, Br–, I–, RO–, CN–, OH–, RCOO– | H2O, ROH, ROR, NH3, RNH2, R2NH, R3N |
|
|
|
|
|
Дата добавления: 2014-01-11; Просмотров: 1228; Нарушение авторских прав?; Мы поможем в написании вашей работы!