
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Производство алюминия
|
|
|
|
Алюминий — один из самый распространенных элементов в пр роде. Его содержание в земной коре составляет около 8 %.
Чистый алюминий — металл серебристо-белого цвета, темпер тура его плавления 660 °С, плотность 2,7 т/м3. Алюминий обладает высокими электро- и теплопроводностью, уступая по этим свойствам только серебру и меди, пластичностью и малой окисляемость Прочность и твердость алюминия относительно невысокие. В прокатанном и отожженном состоянии он очень пластичен, но малопрочен.
Наибольшее применение чистый алюминий получил в электротехнической промышленности для изготовления проводов, кабелей и обмотки. Алюминий и его сплавы широко применяются во многих отраслях промышленности: в авиации, металлургии, пищевой про- мышленности и др.
Алюминий обладает высокой химической активностью и в свободном состоянии в природе не встречается. Он входит в состав большинства горных пород в виде Аl2О3 и А1(ОН)3.
Получают алюминий из горных пород с высоким содержанием глинозема: бокситов, нефелинов, алунитов и коалинов. Основным сырьем для получения алюминия являются бокситы (50...60% глинозема, 1...5% кремнезема, 2...25% оксида железа, 2...4% оксида титана, 10...30 % воды).
Технологический процесс получения алюминия состоит из двух стадий: получения глинозема
(Аl 2Оз) из руды и производства алюминия из глинозема. В зависимости от состава и свойств исходного сырья применяют различные способы получения глинозема: химико-термические, кислотные и щелочные.
Широко распространены щелочные способы получения глинозема. Наиболее эффективным из них является мокрый щелочный способ. Этим способом перерабатываются бокситы с низким содержанием кремнезема (2...3 %). Боксит при этом сушат, дробят, размалывают в шаровых мельницах и обрабатывают концентрированной щелочью для перевода гидрата оксида алюминия в алюминат натрия:
|
|
|
Алюминат натрия (NаА1О2) переходит в водный раствор, а другие примеси, не растворяющиеся в щелочах, выпадают в осадок и отфильтровываются. Часть кремнезема также переходит в осадок, остальная его часть растворяется в щелочи и загрязняет водный раствор. В связи с этим для очищения раствора требуется повышенный расход едкого натра.
Отфильтрованный водный раствор алюмината натрия поступает в специальные аппараты — самоиспарители, где происходит гидролиз алюмината натрия и выделение гидроксида алюминия:
Полученный гидроксид алюминия направляется на фильтрование, а затем промывается и поступает в печь, где при температуре 1200 °С прокаливается. В процессе прокаливания получают чистый глинозем: 2А1(ОН)з=А12О3 + ЗН2О.
Выход глинозема из руды при этом способе составляет около 87 %. На производство 1 т глинозема расходуется 2,0...2, 5 т бокситов, 70...90 кг NаОН, около 120 кг извести, 7...9 т водяного пара, 160...180 кг мазута (в пересчете на условное топливо) и около 280 кВт -ч электроэнергии.
Глинозем представляет собой прочное химическое соединение, температура его плавления — - 2050 °С, кипения -— 2980 °С. В этих условиях восстановление алюминия углеродом или его оксидом весьма затруднительно, так как этот процесс заканчивается образованием карбида алюминия (А13С4).
Не представляется возможным получать алюминий с помощью электролиза водного раствора солей, так как в этом Случае на катоде выделяется только водород. Поэтому алюминий получают электролизом из глинозема, растворенного в расплавленном криолите. Процесс происходит в специальных электролизных ваннах (рисунок 4.3).
Рисунок 4.3 - Технологическая схема получения алюминия из глинозема
|
|
|
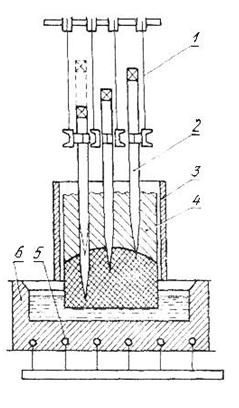 Ванна представляет собой железный корпус, футерованный углеродистыми блоками 6. В них вставляются медные катодные шины 5, соединенные с отрицательным электродом источника тока. Сверху в ванну опускается угольный электрод, представляющий собой непрерывный «самообжигающий» анод 4. Он изготовляется из нефтяного или смоляного кокса и каменноугольного пека, а снаружи заключен в кожух из тонких листов алюминия 3, который но мере необходимости наращивается вверх. В верхних слоях анодной массы температура достигает 100... 140 °С, в нижних — 360 °С. Масса приобретает тестообразное состояние, а при температуре 400...950 °С-твердое. Ток подводится к аноду через стальные штыри 2, забиваемые в анод. С помощью механизма подъема / аноды перемещаются по вертикали.
Ванна представляет собой железный корпус, футерованный углеродистыми блоками 6. В них вставляются медные катодные шины 5, соединенные с отрицательным электродом источника тока. Сверху в ванну опускается угольный электрод, представляющий собой непрерывный «самообжигающий» анод 4. Он изготовляется из нефтяного или смоляного кокса и каменноугольного пека, а снаружи заключен в кожух из тонких листов алюминия 3, который но мере необходимости наращивается вверх. В верхних слоях анодной массы температура достигает 100... 140 °С, в нижних — 360 °С. Масса приобретает тестообразное состояние, а при температуре 400...950 °С-твердое. Ток подводится к аноду через стальные штыри 2, забиваемые в анод. С помощью механизма подъема / аноды перемещаются по вертикали.
Электролизеры питаются током 50 000... 155 000 А при напряжении 4... 4,5 В. Ток используется не только для обеспечения процесса электролиза глинозема, но и для поддержания температуры электролита в пределах 950... 1000°С.
Перед началом процесса ванну подогревают и постепенно добавляют криолит. При толщине слоя расплавленного криолита 200...300 мм в ванну загружают глинозем (10...15% от массы криолита). Под воздействием электрического тока на аноде выделяется кислород. Он взаимодействует с углеродом анода, образуя СО и СО?, которые отводятся из ванны. На дне ванны (катоде) собирается жидкий алюминий, который периодически откачивается с помощью вакуумного ковша, соединенного с вакуумным насосом. По мере необходимости электрод обновляется. Суточная производительность ванны составляет около 350 кг алюминия. Длительность непрерывной работы ванны — 2...3 года. Для производства 1 т алюминия расходуется около 2 т глинозема, 0,7 т анодной массы, 0,1 т криолита и других фторидов и 16... 18 МВт-ч электроэнергии. В структуре себестоимости 1 т алюминия затраты на электроэнергию составляют более 30 %, около 50 % приходится на сырье и основные материалы. В этих условиях рациональное использование сырья и электроэнергии является одним из путей снижения себестоимости производства алюминия.
Для увеличения степени чистоты алюминия его дополнительно подвергают рафинированию. С этой целью алюминий в ковшах вместимостью около 1,25 т подвергают при температуре 650...770оС продувке хлором в течение 10...15 мин. Из алюминия выделяются примеси глинозема, криолита и газы. Рафинированный алюминий разливают в изложницы. Для получения алюминия высокой чистоты применяют электролитическое рафинирование. В этом случае анодом служит подлежащий очистке алюминий, катодом пластины из чистого алюминия. Расплавы хлористых и фтористых солей используются в качестве электролита.
|
|
|
Рафинирование алюминия возможно и другими способами. Некоторые заводы вторичного алюминия применяют, например, магниевый способ рафинирования.
Для получения алюминия особой чистоты широкое применение получил метод его зонной перекристаллизации, в основе которого лежит неодинаковое распределение примесей алюминия (или другого рафинируемого металла) между жидкой и твердой фазой и частичном расплавлении.
В зависимости от степени чистоты алюминия ГОСТ 11069— нормирован выпуск его марок А995, А99, А95 с содержанием примесей не более 0,005...0,5 % и алюминия особой чистоты А5 (не более 0,001 % примесей).
В цветной металлургии в настоящее время применяют новый способ комплексной переработки сырья — плавки в «жидкой ванне».
Суть этого способа заключается в следующем: в печь, где идет плавка и температура шлака достигает 1350 °С, подается через| фурмы кислород. Через свод печи производят загрузку сырья. Размер частиц может быть от нескольких микрометров до десятков сантиметров (особой подготовки шихты новая технология не требует). Попадая в кипящий, перемешиваемый кислородом частицы шихты тонут в нем и быстро расплавляются. Частицы сульфида меди не смешиваются со шлаком, а «плавают» в нем. Разнородные частички металла (меди, никеля и др.) слипаются в тяжелые капли и проходят через шлак, образуя под ним штейн, который непрерывно выпускается из печи. В «жидкой ванне» содержание меди в шлаке даже без специального его обеднения составляет всего 0,5...0,6 %, зато в штейне содержится до 60 %. Использование кислородного дутья позволяет получить в процессе окисления сульфидов тепло достаточное для «самообеспечения» процесса плавки без расхода топлива.
Выброс отходящих газов в 10 раз ниже, нежели при плавке сульфидных руд по обычной технологии. Эти газы содержат 60 % диоксида серы и могут использоваться для получения серы, которая извлекается способами, уже освоенными промышленностью.
Удельная производительность печи для плавки в «жидкой ванне» превышает производительность отражательной печи более чем в 15 раз. При этом резко облегчаются условия труда и уменьшается загрязнение окружающей среды отходами производства цветных металлов.
|
|
|
|
|
Дата добавления: 2014-01-15; Просмотров: 928; Нарушение авторских прав?; Мы поможем в написании вашей работы!