
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Тема 3. Растворы
|
|
|
|
Фотохимические реакции.
К фотохимическим реакциям относятся реакции, протекающие под действием квантов света. Такие реакции многочисленны, а некоторые из них имеют жизненно важное значение.
Фотохимические реакции – реакции выделения кислорода и ассимиляции 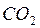 в процессе фотосинтеза, образование озона из кислорода под действием ультрафиолетового излучения солнца, природный синтез хлорофилла,. фотохимическое разложение бромистого Ag.
в процессе фотосинтеза, образование озона из кислорода под действием ультрафиолетового излучения солнца, природный синтез хлорофилла,. фотохимическое разложение бромистого Ag.
,
3.1 Дисперсные растворы. Классификация дисперсных систем. Суспензии. Эмульсии. Коллоидные растворы. Истинные растворы. Общие свойства растворов. Растворимость. Способы выражения концентрации растворов. Энергетика процесса растворения. Разбавленные растворы неэлектролитов. Законы Рауля.
В природе химические соединения в индивидуальном состоянии практически не встречаются. Часто они находятся в виде смеси друг с другом, в виде водных растворов, образуя химические системы.
Классификация дисперсных систем.
Если в какой-либо среде распределено в виде очень мелких частиц другое вещество, то такая система называется дисперсной. При этом в дисперсных системах различают дисперсную фазу – мелкораздробленное вещество и дисперсную среду – однородное вещество, в котором распределена дисперсная фаза.
В качестве примера могут быть названы следующие системы:
1. воздух, где мы можем рассматривать азот как дисперсионную среду (его около 78 %), в которой распределены частицы других газов (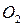 ,
,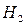 и др.);
и др.);
2. туман – мелкие капельки воды, распределённые в дисперсионной среде – воздухе;
3. дым – мелкие частицы твёрдых веществ, распределённые в воздухе.
Следующие три типа системы являются наиболее важными. Им соответствуют, например:
4. раствор воздуха в воде;
5. раствор спирта в воде;
6. раствор сахара в воде;
7. раствор водорода в палладии;
8. вода в сливочном масле;
9. синяя каменная соль, цвет которой обусловлен тем, что в NaCl
(дисперсионной среде) распределены очень мелкие частицы металлического натрия (дисперсной фазы).
Свойства дисперсных систем, в первую очередь их устойчивость, в очень сильной степени зависят от размеров распределённых частиц.
В зависимости от размера частиц все дисперсные системы подразделяют на группы:
1. Взвеси (суспензии, эмульсии), у которых частицы имеют размер 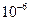 м и более.
м и более.
Например: эмульсия (ж + ж) – молоко, майонез; эмульсия (т + ж) – масло.
2. коллоидные системы, размер частиц 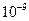 м -
м - 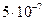 м (1-500 нм).
м (1-500 нм).
Коллоидные частицы состоят из ядра, имеют противоионы и молекулы растворителя. Адсорбированные ионы и противоионы с растворителем образуют адсорбированный слой. Вокруг частиц находится диффузный слой ионов. Коллоидная частица и диффузный слой образуют электронейтральную мицеллу.

AgJ
золь
3. Истинные растворы. Размер частиц дисперсной фазы меньше 1 нм. Например, раствор сахара в воде, раствор солей.
|
|
|
|
|
Дата добавления: 2014-01-15; Просмотров: 445; Нарушение авторских прав?; Мы поможем в написании вашей работы!