
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Атомистическая теория Дальтона
|
|
|
|
Экспериментальное подтверждение атомной гипотезы нашёл английский химик Джон Дальтон. В начале XIX века Дальтон открыл несколько новых эмпирических закономерностей: закон парциальных давлений (закон Дальтона), закон растворимости газов в жидкостях (закон Генри-Дальтона) и, наконец, закон кратных отношений.
Объяснить эти закономерности (прежде всего закон кратных отношений), не прибегая к предположению о дискретности материи, невозможно. Основываясь на законе кратных отношений, открытом в 1803 г., и законе постоянства состава, Дальтон разработал свою атомно-молекулярную теорию, изложенную в вышедшем в 1808 г. труде "Новая система химической философии".
Основные положения теории Дальтона состояли в следующем:
1. Все вещества состоят из большого числа атомов (простых или сложных).
2. Атомы одного вещества полностью тождественны. Простые атомы абсолютно неизменны и неделимы.
3. Атомы различных элементов способны соединяться между собой в определённых соотношениях.
4. Важнейшим свойством атомов является атомный вес.
Уже в 1803 г. в лабораторном журнале Дальтона появилась первая таблица относительных атомных весов некоторых элементов и соединений; в качестве точки отсчёта Дальтон выбрал атомный вес водорода, принятый равным единице. Для обозначения атомов элементов Дальтон использовал символы в виде окружностей с различными фигурами внутри. Впоследствии Дальтон неоднократно корректировал атомные веса элементов, однако для большинства элементов им приводились неверные значения атомных весов.
| Простые атомы | Сложные атомы | ||||

| Водород | 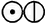
| Аммиак | ||

| Кислород | 5.66 | 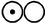
| Вода | 6.66 |

| Азот | 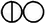
| Монооксид азота | 9.66 | |

| Углерод | 4.5 | 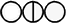
| Диоксид азота | 13.66 |

| Сера |
Таблица Дальтона стала первым шагом на долгом пути, который предстояло пройти химии для того, чтобы величины атомных масс приняли привычные для нас значения. Разрешение проблемы определения атомных весов, потребовавшее усилий многих выдающихся учёных, заняло более пятидесяти лет! И даже после того, как проблема была в основном решена, точное определение атомным масс оставалось настолько важной задачей, что в 1914 г. американский учёный Теодор Ричардс был удостоен Нобелевской премии за уточнение атомных масс некоторых элементов.
|
|
|
|
|
Дата добавления: 2014-01-15; Просмотров: 1014; Нарушение авторских прав?; Мы поможем в написании вашей работы!