
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Химические свойства. Химическая активность металлов II группы побочной подгруппы понижается сверху вниз. Zn Cd Hg ,В –0,762 –0,402
|
|
|
|
Химическая активность металлов II группы побочной подгруппы понижается сверху вниз.
| Zn | Cd | Hg | |
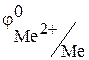 ,В ,В
| –0,762 | –0,402 | +0,853 |
1. Взаимодействие с простыми веществами
Цинк и кадмий устойчивы на воздухе, благодаря оксидной пленки (пленка на поверхности цинка содержит также основный карбонат).
Прим. Пар цинка горит на воздухе, если тонкую пластинку металла накалить в пламени горелки, то она сгорает зеленоватым пламенем с образованием белого дыма оксида. Кадмий и ртуть на воздухе устойчивы и не утрачивают металлического блеска.
В реакцию с кислородом цинк, кадмий и ртуть вступают при нагревании до 350 °С. Например:
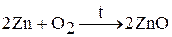
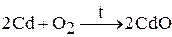
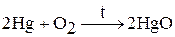 (при дальнейшем нагревании разлагается на ртуть и кислород)
(при дальнейшем нагревании разлагается на ртуть и кислород)
При нагревании цинк и кадмий реагируют с галогенами, серой и фосфором. Ртуть при комнатной температуре реагирует галогенами и серой, с фосфором не взаимодействует. Например:
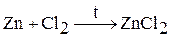
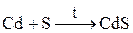
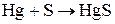
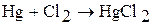
2. Цинк и кадмий взаимодействуют с кислотами-неокислителями. В результате реакций происходит выделение водорода. Например:
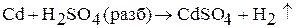
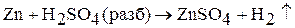
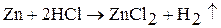
Прим. легко растворяется в кислотах технический цинк, содержащий примеси менее активных металлов (медь, кадмий). Металлы очень высокой чистоты устойчивы к действию растворов кислот по кинетическим причинам. Для ускорения реакции их приводят в контакт с медной проволокой или добавляют в раствор медный купорос.
Ртуть не растворяется в соляной и разбавленной серной кислотах (в ряду напряжения металлов находится после водорода).
3. Цинк и кадмий взаимодействуют с растворами кислот-окислителей: серной и азотной. Состав продуктов восстановления определяется концентрацией раствора:
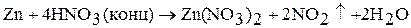
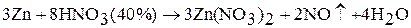
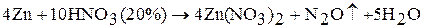
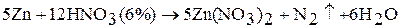
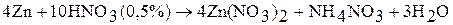
Ртуть легко растворяется в концентрированной азотной кислоте – образуется нитрат ртути (II):
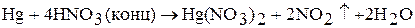
При растворении ртути в разбавленной азотной кислоте на холоду образуется нитрат ртути (I):
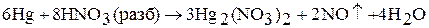
При растворении ртути в горячей концентрированной серной кислоте в зависимости от избытка ртути или кислоты образуются соли одновалентной или двухвалентной ртути:
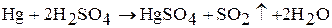
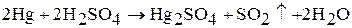
Ртуть растворяется в царской водке:
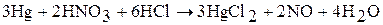
4. Цинк не разлагает воду (хотя должен и может), т.к. в водном растворе он быстро покрывается защитной пленкой оксида, которая предохраняет его от коррозии.
5. Цинк – сильный восстановитель и вытесняет менее активные металлы из растворов их солей. Например:
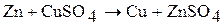
В сильнощелочной среде цинк является очень сильным восстановителем 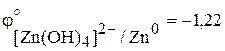 В, способен нитраты и нитриты в аммиак:
В, способен нитраты и нитриты в аммиак:
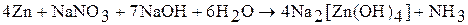
6. Цинк проявляет амфотерные свойства.
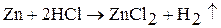
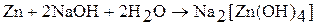 (для кадмия не характерно)
(для кадмия не характерно)
Цинк медленно растворяется за счет косплексообразования в растворах аммиака:
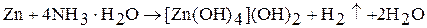
(для кадмия малохарактерно)
Ртуть отличается по химическим свойствам от цинка и кадмия. Это единственный металл, образующий кластерные катионы 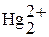 ,
, 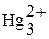 ,
, 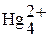 . Ковалентные связи Hg – Hg формируются при участии s-электронов атомов ртути.
. Ковалентные связи Hg – Hg формируются при участии s-электронов атомов ртути.
|
|
|
|
|
Дата добавления: 2014-01-15; Просмотров: 1444; Нарушение авторских прав?; Мы поможем в написании вашей работы!