
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Соединения ванадия в степени окисления +5
|
|
|
|
В ряду V (V) – Nb (V) –Та (V) устойчивость кислородных соединений возрастает. Об этом свидетельствует сопоставление энергий Гиббса, например:
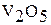
| 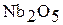
| 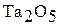
| |
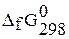 , кДж/моль , кДж/моль
| –1427 | –1776 | –1908 |
Для ванадия (V) известны оксид 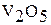 и фторид
и фторид 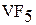 , тогда как для ниобия (V) и тантала (V) известны и все другие галогениды
, тогда как для ниобия (V) и тантала (V) известны и все другие галогениды 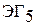 . Для ванадия (V) характерны оксогалогениды типа
. Для ванадия (V) характерны оксогалогениды типа 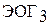 . Все указанные соединения типично кислотные.
. Все указанные соединения типично кислотные.
Оксиды – красный 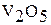 (
(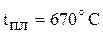 ), белый
), белый 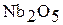 (
(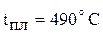 ) и
) и 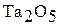 (
(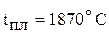 ) – тугоплавкие кристаллические вещества. Оксиды имеют высокие энтальпии образования и энергии Гиббса. Значения
) – тугоплавкие кристаллические вещества. Оксиды имеют высокие энтальпии образования и энергии Гиббса. Значения 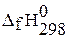 и
и 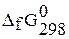 для
для 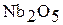 и
и 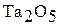 близки (следствие лантаноидного сжатия) и заметно отличаются от таковых для
близки (следствие лантаноидного сжатия) и заметно отличаются от таковых для 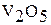 .
.
Оксид ванадия (V) получают термическим разложением 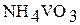 :
:
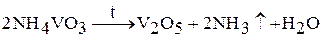
Оксид ванадия (V) плохо растворим в воде (0,007 г/л при 25 °С), образует кислый раствор светло-желтого цвета, довольно легко растворяется в щелочах, а в кислотах – лишь при длительном нагревании.
Оксиды ниобия (V) и тантала (V) химически неактивны, в воде и кислотах практически не растворяются, а со щелочами реагируют лишь при сплавлении:
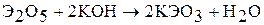
Оксованадаты (V), оксониобаты (V) и оксотанталаты (V) – кристаллические вещества сложного состава и строения. В воде растворимы лишь производные s-элементов первой группы и NH4+. Из ванадатов наибольшее значение имеет 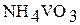 – исходное вещество для получения других соединений ванадия.
– исходное вещество для получения других соединений ванадия.
Пентагалогениды ванадия, ниобия и тантала легкоплавки, летучи, растворяются в органических растворителях, химически активны.
Пентафторид ванадия VF5 – вязкая жидкость (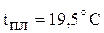 ). Будучи кислотными соединениями, пентагалогениды легко гидролизуются, образуя аморфные осадки гидратированных оксидов:
). Будучи кислотными соединениями, пентагалогениды легко гидролизуются, образуя аморфные осадки гидратированных оксидов:
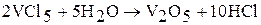
Галогениды Э (V) реагируют с соответствующими основными галогенидами с образованием анионных комплексов 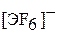 . Например:
. Например:
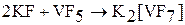
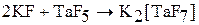
Оксогалогениды легко гидролизуются с образованием гидратированных оксидов 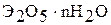 . Например:
. Например:
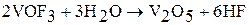
Оксогалогениды вступают также во взаимодействие с основными галогенидами, например:
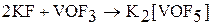
Производные ванадия (V) в кислой среде проявляют окислительные свойства, например, окисляют концентрированную соляную кислоту:
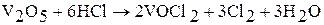
Для перевода же ниобия (V) и в особенности тантала (V) в более низкие степени окисления требуются энергичные восстановители и нагревание.
Соединения ванадия используются в химической промышленности в качестве катализаторов (производство серной кислоты), а также применяются в стекольной и других отраслях промышленности.
|
|
|
|
|
Дата добавления: 2014-01-15; Просмотров: 605; Нарушение авторских прав?; Мы поможем в написании вашей работы!