
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Внутренняя энергия идеального газа. Число степеней свободы молекулы. Закон равномерного распределения энергии по степеням свободы
|
|
|
|
Важной характеристикой термодинамической системы является ее внутренняя энергия U – энергия хаотического (теплового) движения микрочастиц системы (молекул, атомов, электронов, ядер и т.д.) и энергия взаимодействия этих частиц.
К внутренней энергии не относятся кинетическая энергия движения системы как целого и потенциальная энергия системы во внешних полях.
В курсе физики уже встречалось понятие числа степеней свободы i: это число независимых координат, полностью определяющих положение тела (материальной точки, системы материальных точек) в пространстве. Так, например, положение материальной точки определяется тремя координатами (x, y, z), следовательно, i=3. Тонкий стержень имеет 5 степеней свободы (x, y, z, a, b), т.е. 3 поступательные и 2 вращательные, твердое тело имеет 6 степеней свободы (x, y, z, a, b, g), т.е. 3 поступательные и 3 вращательные.
С учетом этого для одноатомных молекул газа (He, Ne, Ar …) i=3, для двухатомных молекул газа (H2, O2, N2 …) с жесткой связью атомов i=5, для трех- и более атомных молекул газа с жесткой связью атомов (CO2, NH3 …) i=6.
Естественно, что жесткой связи между атомами не существует – атомы могут совершать колебания. С учетом этого полное число степеней свободы iå=i+2iколеб. В классической теории рассматривают молекулы с жесткой связью атомов, для них iколеб.=0.
Итак, независимо от числа степеней свободы молекул, три степени свободы всегда поступательные. Ни одна из них не имеет преимущества перед другими, поэтому на каждую из них приходится в среднем одинаковая энергия, равная 1/3 значения <Wk> [см.(16) в лекции 1,2], т.е.
<Wk>/ 3 = kT/ 2.
Важнейший закон классической статистической физики – закон равномерного распределения энергии по степеням свободы – утверждает: на каждую степень свободы молекулы в среднем приходится одинаковая кинетическая энергия, равная kТ/2.
Следовательно, средняя кинетическая энергия молекулы, имеющей i степеней свободы, <Wk> = 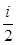 kT. (1)
kT. (1)
Так как в идеальном газе взаимная потенциальная энергия молекул равна нулю (т.е. молекулы между собой не взаимодействуют), то внутренняя энергия U представляет собой кинетическую энергию его молекул.
Для одного моля
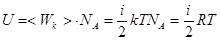 , (2)
, (2)
для произвольной массы m газа
 , (3)
, (3)
где М – масса моля, n=m/M – число молей.
Таким образом, внутренняя энергия идеального газа пропорциональна температуре газа и зависит от числа степеней свободы его молекул.
|
|
|
|
|
Дата добавления: 2014-01-15; Просмотров: 767; Нарушение авторских прав?; Мы поможем в написании вашей работы!