
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Фазовые диаграммы. Тройная точка
|
|
|
|
Фазы и фазовые переходы
Фазой называется совокупность частей системы одинаковых по всем физическим, химическим свойствам и структурному составу. Например, существует твердая, жидкая и газообразная фазы (называемые агрегатными состояниями).
Фазовый переход (фазовое превращение), в широком смысле – переход вещества из одной фазы в другую при изменении внешних условий (Т, Р, магнитных и электрических полей и т.д.); в узком смысле – скачкообразное изменение физических свойств при непрерывном изменении внешних параметров. Будем далее рассматривать фазовые переходы в узком смысле.
Различают фазовые переходы I рода и II рода. Фазовый переход I рода – широко распространенное в природе явление. К ним относятся: испарение и конденсация, плавление и затвердевание, сублимация или возгонка (переход вещества из кристаллического состояния непосредственно, без плавления, в газообразное, например, сухой лед) и конденсация в твердую фазу и др. Фазовые переходы I рода сопровождаются выделением или поглощением теплоты (теплоты фазового перехода q), при этом скачком изменяются плотность, концентрация компонентов, молярный объем и т.д.
Фазовый переход II рода не сопровождается выделением или поглощением теплоты, плотность изменяется непрерывно, а скачком изменяется, например, молярная теплоемкость, удельная электрическая проводимость, вязкость и др. Примерами фазовых переходов II рода могут служить переход магнитного вещества из ферромагнитного состояния (m>> 1) в парамагнитное (m» 1) при нагреве до определенной температуры, называемой точкой Кюри; переход некоторых металлов и сплавов при низких температурах из нормального состояния в сверхпроводящее и др.
Разные фазы одного и того же вещества могут находиться в равновесии, соприкасаясь друг с другом. Такое равновесие наблюдается лишь в ограниченном интервале температур, причем каждому значению температуры Т соответствует свое давление Р, при котором возможно равновесие. Для наглядного изображения фазовых превращений используются фазовые диаграммы состояний, на которых в координатах Р, Т задается зависимость между температурой фазового перехода и давлением. Строятся такие диаграммы на основе экспериментальных данных.
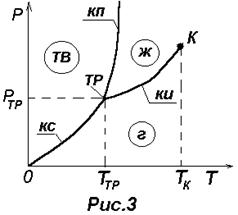
| На рис.3 изображена характерная диаграмма состояния вещества. Три фазы одного и того же вещества (твердая, жидкая и газообразная) могут находиться в равновесии только при единственном значении температуры ТТР и давлении РТР. Эту точку называют тройной (ТР). В тройной точке сходядтся три кривые равновесия фаз, взятых попарно: 1) кривая испарения (КИ) определяет условия равновесия между жидкой и газообразной фазами (например, между водой и водяным паром); |
2) кривая плавления (КП) определяет условия равновесия между твердой и жидкой фазами (например, между льдом и водой); 3) кривая сублимации (КС) определяет условия равновесия между твердой и газообразной фазами (например, между льдом и водяным паром). Каждое вещество имеет только одну тройную точку. Тройная точка воды имеет ТТР =273,16 К (или tТР =0,01°С) и РТР =611 Па, что соответствует 1/166 физической атмосферы. При такой температуре и давлении вода, лед и водяной пар находятся в равновесии, т.е. могут оставаться в таком состоянии сколь угодно долго.
Уравнение Клапейрона-Клаузиуса выражает связь наклона кривой равновесия двух фаз с теплотой фазового перехода q и изменением фазового объема V2-V1:
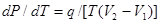 . (6)
. (6)
|
|
|
|
Дата добавления: 2014-01-15; Просмотров: 593; Нарушение авторских прав?; Мы поможем в написании вашей работы!