
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Водородный показатель
|
|
|
|
Лекция 12. Диссоциация воды. Диссоциация кислот и оснований.
Ключевые слова: ионное произведение воды, водородный показатель (рН), гидроксильный показатель (рОН), кислота, основание, расчеты рН в растворах кислот и оснований.
Вода в очень малой степени находится в диссоциированном состоянии (очень слабый электролит): H2O H+ + OH –
H+ + OH –
 |
К её диссоциации можно применить закон действующих масс:
При столь малой константе диссоциации (КД) концентрация воды остается практически неизменной и равной [H2O]=1000/18=55.6 моль/л. Произведение постоянных величин - также постоянная величина: Kд∙[H2O] = [H+]∙[OH–].
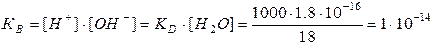 |
Таким образом, произведение молярных концентраций ионов водорода [H+] и гидроксильных групп [OH–] в любом водном растворе есть величина постоянная (при данной температуре) и называется ионным произведением воды (КВ). Диссоциация воды – процесс эндотермический, поэтому ионное произведение воды (КВ) зависит от температуры. С повышением температуры увеличиваются концентрации [H+] и [OH–] ионов и величина ионного произведения: так, при 100оС: КВ = [H+][OH–] = 59∙10-14, при 0оС: КВ = [H+][OH–] = 0,139∙10-14.
В соответствии с теорией электролитической диссоциации ионы H+ являются носителями кислотных свойств, а ионы OH– - носителями основных свойств. Поэтому раствор будет нейтральным, при условии: [H+] = [OH–] =
10–7 моль/л; при [H+] > [OH–] – кислым; при [H+] < [OH–] – щелочным.
Концентрация катионов водорода [H+] обычно выражается очень малыми величинами. Для большего удобства принято пользоваться отрицательным значением десятичного логарифма молярной концентрации ионов [H+], который назван водородным показателем, и обозначается рН:
рН = –lg [H+], где [H+] - молярная концентрация ионов H+. Следовательно: [H+]= 10–pH
Если реакция среды нейтральная, то [H+] = 10–7 [моль/л], и рН=7. Если реакция среды кислая, то [H+]>10–7 [моль/л], и рН<7. Если среда щелочная, то [H+]<10–7 [моль/л], и рН>7. По аналогии рН введен гидроксильный показатель (рОН):
рОН = –lg [ОH- ], где [ОH- ] - молярная концентрация ионов ОH-. А также показатель константы воды: рКВ = –lg КВ. Логарифмируя ионное произведение воды, получаем выражение: –lg [H+][OH–] = –lg 10–14 и далее: pH + pOH = 14.
Кислота (определение по Аррениусу) – это химическое соединение, которое в водном растворе полностью или частично диссоциирует на положительные ионы водорода и отрицательные ионы кислотного остатка.
|
|
|
|
|
Дата добавления: 2014-01-20; Просмотров: 389; Нарушение авторских прав?; Мы поможем в написании вашей работы!