
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Эквивалентность теплоты и работы. Историческая справка
|
|
|
|
В механике работа всегда измерялась как произведение силы на расстояние. В системе СИ работа измеряется в Джоулях:
1 Дж = 1 Н · 1 м.
Энергия материального объекта, по определению, является мерой механической работы, которую этот объект может совершить при определённых условиях. Поэтому размерность энергии и механической работы совпадают. То есть по определению энергия в системе СИ измеряется в Джоулях.
Изначально теплота в физике не считалась энергией и никак с ней не сопоставлялась. Считалось, что теплота проявляется при изменении температуры тел. Количественное измерение теплоты стало возможно после изобретении первого термометра (около 1590 года), позволявшего измерять температуру тел в градусах. Изменение температуры тел объясняли «впитыванием» этими телами флюидов теплорода – невесомой жидкости, подобно тому, как вода впитывается губкой.
Исторически теплота измерялась в калориях (от латинского calor – тепло). Одна калория определялась как количество теплорода, которое необходимо передать воде для повышения температуры одного грамма воды на один градус.
Физики всегда отмечали, что между Джоулями и калориями существует какая-то связь. Например, когда молот бьёт по наковальне, то кинетическая энергия молота, измеряемая в Джоулях, исчезает, но зато увеличивается температура и молота, и наковальни. Такое повышение температуры, в те времена объяснялось поступлением к этим объектам т е п л о р о - д а из окружающей среды. Аналогичным образом дело обстояло при совершении механической работы против сил трения.
Постепенно в физике был поставлен вопрос об экспериментальном определении количественных соотношений между калориями и Джоулями в различных процессах.
Первые исследователи этого вопроса были несколько удивлены, когда выяснилось, что в отличающихся процессах при «превращении» Джоулей в калории пропорция между ними примерно сохраняется.
В 1844 – 1854 гг. английский физик Д.Джоуль провёл опыты, которым было суждено сыграть большую роль в науке. Цель опытов состояла в том, чтобы установить соотношение между работой, затрачиваемой при выделении теплоты, и количеством выделившейся теплоты. Схема опыта Джоуля приведена на рис. 6.1.
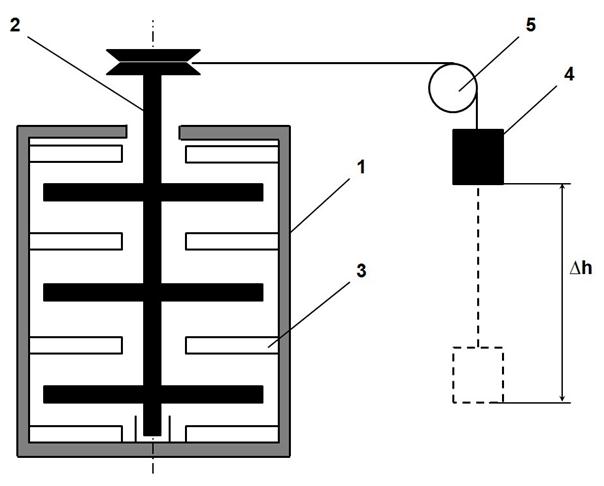
Рис. 6.1. Схема опыта Джоуля:
1 – сосуд; 2 – мешалка; 3 лопатки
В теплоизолированный медный сосуд 1, заполненный водой, погружена мешалка 2, снабжённая лопатками. К стенкам сосуда также прикреплены лопатки 3, затрудняющие движение воды при вращении мешалки. Мешалка приводится во вращение посредством опускания связанного с ней тросом через блок 5 груза 4 массой М, кг. Благодаря механической передаче скорость вращения лопаток мешалки составляет порядка 700 мин –1 [2]. При опускании на высоту Δ h работа L, Дж, производимая грузом и, следовательно, мешалкой, равняется убыли потенциальной энергии груза:
L = M · g · Δ h, Дж,
где g – ускорение свободного падения, м/с2.
Теплота Q, выделившаяся в сосуде с водой вычисляется в калориях по повышению температуры воды, измеряемой термометром. Масса воды была заранее измерена. Учитывалось поглощение теплоты стенками сосуда, лопатками и мешалкой. Усредняя данные своих экспериментов Джоуль приходит у выводу: «Для получения количества тепла, которое в состоянии нагреть один фунт воды на один градус Фарингейта, необходимо употребить механическую силу, которая может быть представлена падением 772 фунтов с высоты в один фут». Из этих данных следует, что найденный Джоулем механический эквивалент калории J дж равен [3]:
 , Дж/кал. (6.1)
, Дж/кал. (6.1)
Впоследствии производились многочисленные эксперименты определения этой «универсальной постоянной», как её называл Гельмгольц. Например, опыты Г.Грина, который, исследуя в 1860 – 1861 гг. соударения двух свинцовых тел, нашел значение эквивалента равным 4,166 Дж/кал. А также опыты Роуланда (1880 г.) который методом Джоуля получил значение эквивалента 4,186 Дж/кал, что считается достаточно точным и по настоящее время.
Впоследствии значение эквивалента, полученного Джоулем, было несколько уточнено. В соответствии с результатами наиболее точных современных измерений [4] механический эквивалент теплоты J равен:
 Дж/кал. (6.2)
Дж/кал. (6.2)
Другими словами:
1 кал = 4,1868 Дж. (6.3)
Определяемая (6.3) калория называется Международной. Её значение установлено в 1948 году на IX Генеральной конференции по мерам и весам как точное равенство [2].
Теплоёмкость воды несколько зависит от температуры. Международная калория определяется как количество теплоты, расходуемой на нагревание 1 грамма воды при нормальном атмосферном давлении от 14,5 до 15,5 °С. Иногда её называют 15-градусная калория.
Если нагрев на один градус производится при исходной температуре воды, соответствующей нормальным условиям (нормальному давлению р о = 760 мм рт. ст. = 101325 Па и нормальной температуре t o = 0 °С), то такая калория называется термохимической:
1 кал (термохимическая) = 4,14 Дж.
Установленная таким образом однозначная для всех процессов связь между Джоулями и калориями впервые позволила аналитически сформулировать закон сохранения энергии, который был назван «Первое начало термодинамики».
|
|
|
|
Дата добавления: 2014-01-20; Просмотров: 1310; Нарушение авторских прав?; Мы поможем в написании вашей работы!