
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Теория кислот и оснований Льюиса
|
|
|
|
Существуют, однако, реакции, которые по здравому смыслу должны относиться к кислотно-основным, но на самом деле не подпадают под определение Брёнстеда-Лоури. К ним относятся, например, взаимодействия:
СаО+SO3 ®CaSO4 NH3+BF3®NH3BF3
Для описания реакций подобного типа Г. Льюис (в 1923 г.) предложил новое определение кислот и оснований. Согласно его определению:

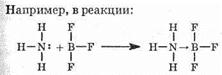
аммиак выступает в роли основания, а трифторид бора в роли кислоты. Определение основания, данное Льюисом, включает основания Брёнстеда-Лоури. Такие кислоты Льюиса, как BF3 и SO3, не являются кислотами Брёнстеда-Лоури, а такие кислоты, как НСl, H2SO4 и СН3СООН, не являются кислотами Льюиса.
Теория кислот и оснований Брёнстеда-Лоури позволяет количественно определять их силу, что нельзя сказать о теории Льюиса. Следует остановиться на электронной теории кислот и оснований, предложенной Г. Льюисом. Как было отмечено выше, согласно этой теории основанием является вещество, поставляющее пару электронов для образования химической связи, а кислотой — вещество, принимающее электронную пару (см. выше).
Определение Г. Льюиса включает кислоты и те соединения, которые не содержат протонов, но удовлетворяют тем критериям, которые он сформулировал для характеристики кислот и оснований:
1. Взаимодействие кислот с основаниями происходит быстро.
2. Кислота или основание вытесняют более слабую кислоту или основание из соединений.
3. Кислоты и основания можно титровать одно другим в присутствии индикаторов.
4. Кислоты и основания являются хорошими катализаторами химических реакций.
Примером кислотно-основного взаимодействия будут (по протонной теории):

Как видно из этих примеров, в некоторых случаях характеристики вещества по теории Льюиса и по протонной теории кислот и оснований совпадают (NH3 и ОН- — основания, Н3О+, НСl — кислоты). Вещества же, которые являются кислотами или основаниями только по теории Льюиса, называются основаниями и кислотами Льюиса. Итак, BF3 — кислота Льюиса.
|
|
|
|
|
Дата добавления: 2014-01-20; Просмотров: 1332; Нарушение авторских прав?; Мы поможем в написании вашей работы!