
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Кондуктометрия и кондуктометрическое титрование
|
|
|
|
Вольтамперометрия. Сущность метода. Принципиальная схема установки. Электроды. Качественный и количественный полярографический анализ.
Кулонометрия. Законы Фарадея. Варианты кулонометрии. Прямая кулонометрия и кулонометрическое титрование. Возможности метода и области применения.
Потенциометрические методы анализа: сущность метода, системы электродов. Требования к индикаторным электродам и электродам сравнения. Потенциометрия с ионселективными электродами (ионометрия), потенциометрическое титрование.
ЛЕКЦИИ 8–10. ЭЛЕКТРОХИМИЧЕСКИЕ МЕТОДЫ АНАЛИЗА
Вопросы:
1. Сущность электрохимических методов анализа. Основные понятия: электрохимическая ячейка, индикаторный электрод, электрод сравнения. Электродный процесс, стадии электродного процесса. Классификация электрохимических методов анализа.
1. Электрохимические методы анализа основаны на существовании зависимости между составом анализируемого вещества и его электрохимическими свойствами. Электрохимические методы анализа, основанные на измерении электрической проводимости, потенциалов и других свойств, включают методы кондуктометрии, потенциометрии, полярографии, кулонометрии и др.
В электрохимии выделяют ряд основных понятий:
Электродный процесс (электрохимическая реакция) – гетерогенная реакция, протекающая между компонентами электропроводящих фаз (электрод – раствор), в ходе которой ионы или электроны проходят через границу раздела фаз, и на межфазной границе устанавливается разность электрических потенциалов, называемая электродным потенциалом.
Электродный процесс включает две обязательные стадии: массоперенос – доставку вещества к электроду за счет диффузии, миграции (движения ионов под действием электростатических сил) и конвекции и собственно электрохимическую реакцию (разряд-ионизацию).
При равновесии электрохимическая реакция протекает в обоих направлениях с одинаковыми скоростями, ток в замкнутой гальванической цепи отсутствует, электродный потенциал достигает равновесного значения. В отсутствие равновесия в результате электрохимической реакции через ячейку протекает электрический ток, при этом электродный потенциал отклоняется от равновесного – электрод поляризуется.
Электрохимическая ячейка чаще всего состоит из двух или трех электродов (индикаторного или рабочего электрода, электрода сравнения и вспомогательного), погруженных в раствор электролита.
Индикаторный электрод – это электрод, на котором протекает собственно электрохимическая реакция окисления или восстановления. Это легкополяризуемый электрод, он должен реагировать на изменение концентрации определяемого вещества.
Электрод сравнения – неполяризуемый электрод, потенциал его должен быть устойчивым во времени. Электрод сравнения служит для создания измерительной цепи и поддержания постоянного значения потенциала индикаторного электрода.
Используемый в трехэлектродной ячейке вспомогательный электрод (противоэлектрод ) вместе с рабочим электродом включен в цепь, через которую проходит электрический ток. В состав электролитической ячейки могут входить два идентичных электрода, выполняющих одинаковую функцию.
Электрохимические методы анализа можно классифицировать в зависимости от процессов, происходящих на электродах:
· методы, не связанные с электродной реакцией, измеряемый сигнал является откликом на изменения электрохимических свойств в объеме раствора (кондуктометрия);
· методы, основанные на электродной реакции, в результате которой ток через границу раздела не протекает, и на границе раздела фаз устанавливается равновесный потенциал, величина которого зависит от активности (концентрации) компонентов, участвующих в электродной реакции (потенциометрия);
· методы, основанные на электродной реакции между электродом и приэлектродной частью раствора, в ходе которой электроны или ионы переходят через границу раздела фаз, обусловливая возникновение тока (вольтамперометрия, амперометрия, кулонометрия, электрогравиметрия).
Если электродная реакция не приводит к заметному изменению объемной концентрации раствора, электрохимический метод может быть использован для индикации конечной точки титрования в титриметрии.
Так же электрохимические методы анализа делятся на группы, основанные на:
1) использовании законов Фарадея (электролиз, кулонометрия);
2) измерении электродного потенциала системы (потенциометрия);
3) измерении тока системы (вольтамперометрия);
4) измерении электрической проводимости растворов (кондуктометрия).
В свою очередь 1) Кондуктометрия: 1 – прямая, 2 –косвенная, 3 – кондуктометрическое титрование;
2) Вольтамперометрия:1 – классическая полярография, 2 – исследование поляризационных кривых, 3 – амперометрическое титрование;
3) Кулонометрия: 1 – потенциостатическая, 2 – гальваностатическая;
4) Потенциометрия: 1 – редоксометрия, 2 – монометрия, 3 – рН-метрия, 4 – катионометрия, 5 – анионометрия, 6 – потенциометрическое титрование, 6а – прямое, 6б – дифференциональное;
5) Диэлектрометрия.
2. В основе потенциометрических измерений лежит зависимость равновесного потенциала электрода от активности (концентрации) определяемого иона практически в отсутствие тока между индикаторным электродом и электродом сравнения (гальванический элемент), погруженными в анализируемый раствор, при замыкании гальванической цепи.
Измеряемое напряжение, таким образом, равно:
E = E инд – E ср
Возникновение электродного потенциала связано с электродным процессом на границе «индикаторный электрод – раствор, содержащий окислительно-восстановительную пару»:
Ox + п е  Red,
Red,
либо восстановленную форму обратимой окислительно-восстановительной системы
Мn+ + п е  M 0
M 0
При установлении динамического равновесия электрод приобретает равновесный потенциал. Реакции, протекающие на границе раздела «электрод – раствор», называются потенциалопределяющими, а ионы Ox, Red – потенциалопределяющими ионами. Потенциал индикаторного электрода зависит от активности потенциалопределяющих ионов по уравнению Нернста:

Еº ‑ стандартный электродный потенциал, В.
Потенциометрию применяют как для непосредственного определения концентрации (активности) вещества, находящегося в растворе (прямую потенциометрию), так и для определения точки эквивалентности при титровании (потенциометрическое титрование), измеряя потенциал индикаторного электрода в зависимости от добавленного титранта.
Индикаторные электроды в потенциометрии. Для потенциометрических измерений используют два основных типа индикаторных электродов: металлические и мембранные (ионоселективные) электроды.
Ионоселективные электроды (ИСЭ) – это сенсоры (чувствительные элементы, датчики), потенциал которых линейно зависит от логарифма активности определяемого иона в растворе, они позволяют избирательно определять активность одних ионов в присутствии других.
Потенциал мембранного электрода возникает за счет обмена заряженными частицами (ионами) между раствором и мембраной электрода. Полупроницаемая мембрана отделяет внутреннюю часть электрода (внутренний раствор) от анализируемого (внешнего) раствора и обладает способностью пропускать преимущественно ионы одного вида. Активность ионов, к которым мембрана проницаема, во внутреннем растворе постоянна.
При потенциометрических измерениях с использованием ИСЭ измеряют ЭДС следующей ячейки:
| Электрод сравнения 1 | Внешний (анализируе- мый) раствор [А+] = а1 | Мембрана | Внутренний раствор [А+] = а2 | Электрод сравнения 2 |


Е1 ЕМ Е2
После погружения электрода в анализируемый раствор начинается движение иона А+, проникающего через мембрану, в направлении его более низкой активности. Так как ионы несут заряд, то из-за различия активностей ионов А+ в растворе и мембране на обеих сторонах мембраны возникают граничные потенциалы Е1 и Е2, препятствующие дальнейшему перемещению ионов. С помощью двух электродов сравнения, помещенных во внешний и во внутренний растворы можно измерить разность граничных потенциалов, или так называемый мембранный потенциал Ем:
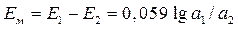
Так как активность ионов А+ во внутреннем растворе постоянна, потенциал мембранного электрода Ем линейно зависит от логарифма активности иона А+ в анализируемом растворе:

Если раствор кроме определяемого иона А содержит посторонние ионы K, потенциал ионоселективного электрода описывается уравнением Никольского (модифицированным уравнением Нернста):
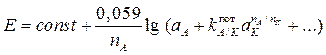 ,
,
где const – константа, зависящая от значений стандартных потенциалов Е0 внутреннего и внешнего электродов сравнения и от природы мембраны электрода; a A и n A, a K и n K – активности и заряды основного (потенциалопределяющего) и постороннего ионов соответственно; 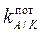 – потенциометрический коэффициент селективности электрода по отношению к потенциалопределяющему иону A в присутствии постороннего иона K. Коэффициент селективности можно определить экспериментально, чем меньше его величина, тем более селективен электрод по отношению к определяемому иону.
– потенциометрический коэффициент селективности электрода по отношению к потенциалопределяющему иону A в присутствии постороннего иона K. Коэффициент селективности можно определить экспериментально, чем меньше его величина, тем более селективен электрод по отношению к определяемому иону.
В соответствии с природой активного материала мембраны различают: первичные ИСЭ - а) электроды с жесткой матрицей – стеклянные; б) электроды с твердой мембраной; ИСЭ с подвижными носителями - электроды с жидкими мембранами на основе ионообменников и нейтральных переносчиков; сенсибилизированные (активированные) – газочувствительные, ферментные электроды. При этом классические электроды с внутренним раствором и электродом сравнения являются электродами первого поколения, а электроды с твердым токоотводом (твердотельные) – электродами второго поколения
Электроды с жесткой матрицей. Стеклянный электрод. Самым известным примером стеклянного электрода является электроддля измерения рН растворов. Он состоит из стеклянного шарика, который является тонкой рН-чувствительной мембраной, изготовленной из стекла особого состава. Например, стекло марки «корнинг» имеет следующий состав: 22% Na2O, 6% СаО, 72% SiO2.
Внутренним раствором служит раствор соляной кислоты с определенным значением рН (обычно 0,1 М НСl), насыщенный хлоридом серебра. Внутрь помещается серебряная проволочка, образуя хлоридсеребряный электрод сравнения (рис.1). Чувствительностью к ионам водорода обладает только хорошо вымоченная мембрана. Ионообменная реакция сводится к обмену ионами водорода между внешним раствором и стеклом.

Рис. 1. Стеклянный электрод для измерения рН:
1 – стеклянная рН-чувствительная мембрана; 2 – 0.1 М раствор HCl, насыщенный AgCl; 3 – серебряная проволочка; 4 – стеклянная трубка; 5 – изоляция; 6 – токоотвод
Поскольку активность ионов водорода во внутреннем растворе постоянна, потенциал стеклянного электрода становится мерой активности ионов водорода во внешнем растворе, т.е. электрод обладает водородной функцией:
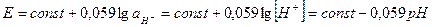
В величину const входят потенциалы внешнего и внутреннего электродов сравнения и так называемый потенциал асимметрии, возникающий в результате различных механических и химических воздействий на внешнюю и внутреннюю поверхность мембраны, величина его меняется в процессе эксплуатации электрода. Правильные результаты можно получить при регулярной градуировке стеклянного электрода по стандартным буферным растворам. Для точных измерений необходимо градуировать электрод по двум растворам.
Изменяя состав стекла, можно получить мембраны, обладающие пониженной селективностью к ионам Н+ и высокой селективностью к другим ионам. Созданы электроды для определения ионов натрия, калия и др.
Твердые электроды. В качестве мембран в твердых электродах используются монокристаллы (LaF3, Ag2S) и мембраны, полученные прессованием или плавлением порошкообразных соединений или их смесей (Ag2S, Ag2S – AgCl, Ag2S – CuS), с ионной проводимостью по катиону или аниону. Для кристаллических мембран характерна высокая специфичность, обусловленная тем, что размер, форма и распределение заряда вакансии решетки позволяет занять это место только определенному подвижному иону. Наиболее совершенным электродом с кристаллической мембраной является фторид-селективный электрод, широкое распространение получил сульфид-серебряный электрод для определения ионов серебра и сульфид-ионов. В настоящее время среди электродов с кристаллическими мембранами распространение получили твердотельные электроды (электроды с твердым контактом), изготовленные без внутреннего раствора.
Жидкостные электроды имеют в качестве мембраны раствор ионообменника или «нейтрального переносчика» в органическом растворителе, не смешивающемся с водой; жидкость мембраны удерживается на пористом полимере и селективно реагирует с определяемым ионом. Электроды с жидкими мембранами позволяют проводить прямое потенциометрическое определение некоторых катионов: К+, Са2+, смеси Са2+ и Mg2+ и т. д., а также ряда анионов: Сl‾, NО3‾, СlО4‾ и т. д. Разработан ряд ИСЭ для определения ионных поверхностно-активных веществ.
Газочувствительные электроды имеют газопроницаемую мембрану из пористого гидрофобного пластика для отделения анализируемого раствора от тонкой пленки промежуточного раствора электролита. Он взаимодействует с определяемым газом, при этом изменяется какой-то параметр промежуточного раствора, например рН, что и фиксирует ионоселективный электрод. Отклик ионоселективного электрода пропорционален парциальному давлению определяемого компонента в анализируемом газе. Известны электроды для определения SO2, H2S, СO2, NH3. Газочувствительные электроды не относятся к истинно мембранным электродам, поскольку через мембрану не протекает электрический ток.
Ферментные электроды – это датчики, в которых ионоселективный электрод покрыт пленкой, содержащий фермент, способный вызвать реакцию органического или неорганического вещества (субстрата) с образованием веществ (ионов, молекул), на которые реагирует электрод. Существуют электроды для определения глюкозы, мочевины и др.
Металлические электроды. Возникновение потенциала металлического электрода обусловлено электронообменными процессами на межфазной границе. Различают активные и инертные металлические электроды.
Активные металлические электроды изготовляют из металлов, образующих восстановленную форму обратимой окислительно-восстановительной системы (Ag, Pb, Cu, Cd), это электроды первого рода.
Электроды первого рода представляют собой металлическую пластинку или проволоку, погруженную в раствор хорошо растворимой соли этого металла (серебро в растворе нитрата серебра, медь в растворе сульфата меди). Потенциал такого электрода зависит от активности собственных ионов в растворе, непосредственно участвующих в электродной реакции переноса электронов, например:
Ag+ + e → Ag°
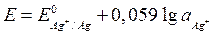
Такие электроды можно использовать лишь в тех растворах, где они не участвуют в химических реакциях с растворителем или электролитом фона, поэтому для селективного определения ионов металлов их используют реже, чем ИСЭ.
Инертные металлические электроды изготовляют из благородных металлов (Pt, Au, Ir и др.). Они служат переносчиками электронов от восстановленной формы к окисленной, и их потенциалы являются функцией соотношения активностей окисленной и восстановленной форм полуреакции. Эти электроды применяют в потенциометрическом окислительно-восстановительном титровании.
К электронообменным электродам, кроме металлических, относят водородный и хингидронный электроды.
|
|
|
|
|
Дата добавления: 2014-01-20; Просмотров: 1580; Нарушение авторских прав?; Мы поможем в написании вашей работы!