
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Ex vivo терапия рака
|
|
|
|
Противоопухолевые «вакцины».
Иммунная система охраняет от любых изменений в нашем внутреннем содержимом. Особенно эффективно она это делает при вторжении в организм вирусов или бактерий. Но она поразительно беспомощна, когда речь касается раковых клеток, хотя эти клетки несут антигены, не свойственные нормальному организму. Уже более 40 лет тому назад было показано, что многие опухоли иммуногенны. Но до появления генно-инженерных методов трансформации эукариотических клеток все попытки в этом направлении оказались тщетными. По каким-то причинам цитотоксические Т-лимфоциты не возбуждаются при виде раковых клеток и их специфических антигенов и не начинают секретировать цитокины, которые они секретируют при встрече с чужими антигенами. Одной из стратегий борьбы с опухолям могла бы стать стратегия, направленная на стимулирование иммунной системы к узнаванию опухолевых клеток. Многие группы учёных пытаются развивать терапию, использующую создание индивидуальных противоопухолевых вакцин. Это можно было бы воплотить в жизнь по схеме, показанной на Рис 16. Клетки, полученные из опухоли больного, выращивают как культуру клеток, и внедряют в них гены, кодирующие белки-иммуностимуляторы, — например, цитокины. Затем эти клетки облучают, чтобы сделать их неактивными, и вводят обратно пациенту в надежде вызвать системный иммунный ответ, который, с одной стороны, призван уничтожить уже существующие опухолевые клетки, а с другой, предохранить пациента от возникновения новых опухолей данного типа. Это основывается на гипотезе, что повышение концентрации цитокинов в непосредственной близости к опухолевым клеткам будет стимулировать ближайшие к ним Т-клетки к иммунному ответу. Действительно, такие стимуляторные эффекты наблюдались у опытных животных и наблюдаются у пациентов, позволивших подвергнуть себя такой терапии. При этом надеются также, что модифицированные клетки вызовут иммунный ответ и против немодифицированных опухолевых клеток.
Рисунок 16. Иммунизация противораковой вакциной, сконструированной из опухолевых клеток, секретирующих гранулоцит-макрофаг колониестимулирующий фактор.
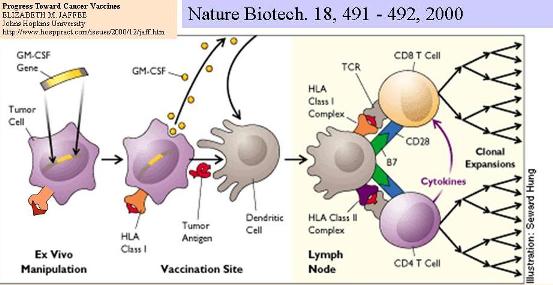
Как всегда, начали на мышах. Клетки опухолей у опытных животных трансформировали генами таких иммуномодуляторов, как цитокины: IL1b, IL-2, IL-4, IL-6, TNFa, GM-CSF, g-интерферон. Действительно, наблюдали, что опухоли у животных, которым вводили модифицированные таким образом клетки этой же опухоли, деградировали. Более того, во многих случаях животные, получившие дозу таких трансдуцированных клеток, становились невосприимчивыми к опухолям при введении опухолевых нетрансдуцированных клеток. То есть, трансдуцированные клетки реально действовали как противоопухолевые вакцины. Это давало основания начать испытания подобных подходов на людях. Пытались включать те же гены иммуностимуляторов с помощью ретровирусных векторов в клетки меланомы, различных карцином, нейробластомы, рака молочной железы.
Ещё один подход к созданию противораковых индивидуальных вакцин показан на Рис. 17—18. Они дают весьма упрощённую схему взаимодействий, которые происходят при узнавании чужих антигенов клетками иммунной системы.
Рисунок 17. Процесс узнавания опухолевых антигенов клетками иммунной системы.
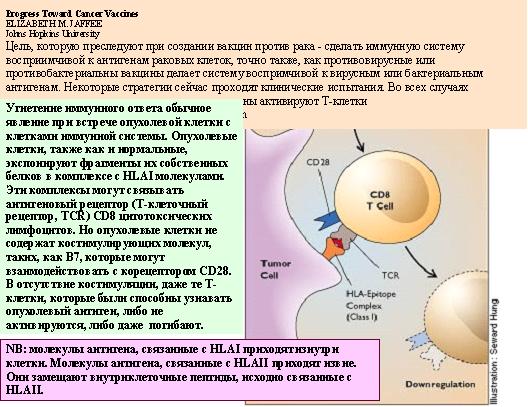
Рисунок 18. Вакцинация, гибель опухолевых клеток.
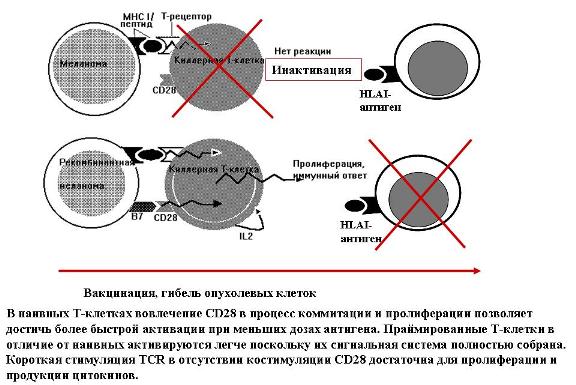
Клетки опухолей, в частности меланомы, представляют специфические опухолевые антигены в виде пептидов, экспонированных на поверхность клеток в виде комплексов с белками главного комплекса гистосовместимости первого типа MHC1. Опухолевые антигены узнаются, как обычно, Т-киллерными клетками или цитотоксическими Т-лимфоцитами. Однако для развития полного иммунного ответа нужно дополнительное взаимодействие ещё одной молекулы на поверхности антигенпредставляющей клетки, костимуляторной молекулы класса В7, и молекулы рецептора, выставленной на поверхность Т-клетки — CD28. Без этого дополнительного взаимодействия Т-клетки не дают той реакции, которая необходима для полноценного иммунного ответа. Иными словами, специфические Т-клетки не начинают продуцировать фактор роста Т-клеток, интерлейкин-2, и не пролиферируют, давая множество специфических к данному антигену Т-клеток, которые затем, в свою очередь, узнают и уничтожают клетки, содержащие на поверхности нежелательный чужой антиген. Кстати, причиной того, что опухолевые клетки не узнаются клетками иммунной системы, может быть то, что опухолевые клетки обычно не содержат на поверхности В7. Поэтому попытались сделать следующее. Взяли клетки меланомы от опытной мыши и ввели в них В7 антиген. Ввели эти клетки здоровой подопытной мыши. Подопытные мыши развивали опухоль, но затем эта опухоль деградировала, и ни одна из мышей, получивших дозу клеток модифицированной меланомы, не погибла. Наоборот, мыши, получившие немодифициованные клетки, погибали. Более того, если мышам, вакцинированным модифицированными меланомными клетками, ввести немодифицированные клетки меланомы, то 89% мышей оказывались защищёнными от развития опухоли. Это означает, что вакцина могла бы предохранять от метастазирования.
Существуют также и другие подходы к созданию противораковых вакцин.
|
|
|
|
|
Дата добавления: 2014-01-20; Просмотров: 1086; Нарушение авторских прав?; Мы поможем в написании вашей работы!