
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Электрохимические методы
|
|
|
|
Валентные, деформационные (маятниковые, ножничные, веерные) колебания. Каждому колебанию соответствует свое волновое число.
Ик спектрометр состоит из источника излучения, щели, диспергирующего элемента (призмы, дифракционные решетки), приемника и различных зеркал.
Лекция 5 (1 час)
Классификация электрохимических методов анализа
Количество вещества, окисленного или восстановленного под действием электрического тока определяют:
1. Выделением на электродах различных веществ при электролизе. Измеряемой величиной является масса выделенного осадка (электрогравиметрия).
2. Измерением количества электричества, израсходованного на электролиз.
3. Измерением предельного тока, величина которого пропорциональна концентрации ионов, восстанавливающихся на катоде. Зависимость силы тока от напряжения выражается кривой с перегибом. Эта зависимость – основа полярографического метода анализа.
4. Измерением электродного потенциала, изменяющегося в результате химических реакций и зависящего от температуры, природы электролита и его концентрации. Возникновение потенциала обусловлено обменом электронами между окислителем и восстановителем на электродах.
Электрические параметры химической системы
Металлическая пластинка, погруженная в раствор соли того же Ме, приобретает относительно раствора определенный электрический потенциал, величина которого зависит от концентрации ионов этого Ме в растворе и от природы электролита.
Два электрода погруженные в раствор, образуют гальванический элемент, напряжение которого равно алгебраической разности потенциалов этих электродов. Напряжение гальванического элемента называется Э.Д.С. и вычисляетсяпо формуле
Э.Д.С. = Еа - Ек
В идеальном случае такая зависимость описывается уравнением Нернста
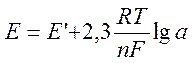
где Е – измеряемая э.д.с. ячейки; Е’ - величина, постоянная при данной температуре; R – газовая постоянная; Т – абсолютная температура; F – постоянная Фарадея; n – взятое с соответствующим знаком число электронов, принимаемых (+) или отдаваемых (-) одной молекулой (ионом) определяемого вещества; а – активность определяемого вещества.
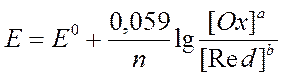
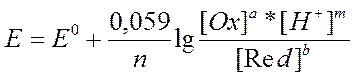
|
|
|
|
|
Дата добавления: 2014-01-20; Просмотров: 341; Нарушение авторских прав?; Мы поможем в написании вашей работы!