
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Стадії горіння різних палив
|
|
|
|
Горіння палива
Горіння - це складний фізико-хімічний процес, який включає в себе ряд послідовно і паралельно здійснюваних фізичних і хімічних стадій. Необхідно створити фізичний контакт між молекулами кисню і палива і довести молекули до стану, коли можлива хімічна реакція між ними.
Процес горіння газу можна умовно розділити на 2 стадії:
- утворення горючої суміші газу і повітря та її початкове нагрівання за рахунок теплоти повітря, що разом з газом надходить в пальник;
- нагрівання до запалювання, запалювання і горіння робочої суміші, що відбувається в топці.
Процес горіння рідкого палива включає такі стадії:
- нагрівання і випаровування рідкого палива;
- змішування пари палива з повітрям;
- нагрівання, запалювання і горіння суміші.
При спалюванні твердого палива відбуваються такі процеси:
- нагрівання палива, його сушіння та виділення летких речовин і утворення коксового залишку;
- утворення суміші летких горючих речовин з повітрям, її нагрівання, запалювання і горіння;
- нагрівання, запалювання і горіння твердого коксового залишку.
Якщо утворення горючої суміші проходить при високій температурі, то відбувається термічний розклад важких вуглеводів палива з утворенням більш легких молекул, які частково окислюються – це, так звана, вогнева чи попередня газифікація палива, яка інтенсифікує процес горіння.
Розрізняють гомогенне горіння, якщо агрегатний стан палива і окислювача один і той же (горіння природного газу), та гетерогенне горіння, яке відповідає умовам спалювання вугілля і мазуту. При цьому гомогенну суміш утворюють летючі речовини твердого палива і повітря, а також пара рідкого палива і повітря.
Горіння палива може бути повним і неповним. В реальних процесах реалізується неповне горіння
Розрізняють механічну і хімічну неповноту згорання. Механічна неповнота згорання полягає в тому, що частина палива, що надійшла для спалювання, не приймає участь в процесі горіння і виходить з топки разом зі шлаками і золою.
Хімічні втрати є результатом хімічно неповного окислення вуглецемістких сполук з утворенням СО (замість СО2), а також в зв’язку з тим, що ряд горючих речовин, які одержуються в процесі випаровування і термічного розкладу рідккого і твердого палива (СО, Н2, СН4 та інші) залишають топку, не завершивши окислювальні процеси.
Кількість повітря, теоретично необхідного для повного спалювання 1 кг палива, визначається з рівняння:
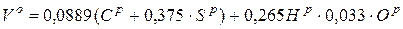 , м3/кг, (2-5)
, м3/кг, (2-5)
де 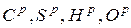 - вміст, відповідно, вуглецю, сірки, водню і кисню в робочому складі палива.
- вміст, відповідно, вуглецю, сірки, водню і кисню в робочому складі палива.
Коефіцієнтом витрати повітря, 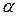 , є відношення дійсного об’єму повітря, яке витрачається на спалювання 1 кг (або 1 м3) палива,
, є відношення дійсного об’єму повітря, яке витрачається на спалювання 1 кг (або 1 м3) палива, 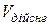 , до теоретично необхідного об’єму, тобто
, до теоретично необхідного об’єму, тобто
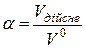 . (2-6)
. (2-6)
Якщо 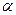 >1 – то це коефіцієнт надлишку повітря.
>1 – то це коефіцієнт надлишку повітря.
Оптимальні значення 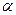 залежать від виду палива і способу його спалювання, зокрема;
залежать від виду палива і способу його спалювання, зокрема;
- для газу 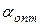 =1,05÷1,15;
=1,05÷1,15;
- для мазуту 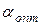 =1,1÷1,4;
=1,1÷1,4;
- для вугільного пилу (камерне спалювання вугілля) 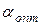 =1,2÷1,25;
=1,2÷1,25;
- для шарового спалювання вугілля 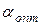 =1,3÷1,7.
=1,3÷1,7.
В результаті повного згорання палива з теоретичного необхідною кількістю повітря утворюються газоподібні продукти, які в основному складаються з СО2, SO2, N2 і Н2О.
Звичайно позначають СО2+SO2=RO2 – кількість 3-х атомних газів.
Для визначення об’ємів газів – продуктів згорання користуються формулами:
- об’єм трьохатомних газів
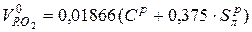 , м3/кг; (2-7)
, м3/кг; (2-7)
- об’єм азоту
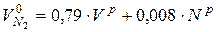 , м3/кг; (2-8)
, м3/кг; (2-8)
- об’єм водяної пари
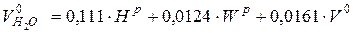 , м3/кг (2-9)
, м3/кг (2-9)
Сумарний теоретичний об’єм продуктів згорання дорівнює
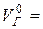
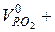
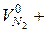
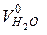 , м3/кг. (2-10)
, м3/кг. (2-10)
Дійсний об’єм продуктів згорання буде більше теоретичного за рахунок О2, N2 і Н2О, що знаходяться в надлишковому повітрі, оскільки 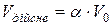 .
.
Оскільки повітря не містить у собі трьохатомних газів, то їх об’єм не залежить від 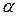 і залишається постійним,
і залишається постійним,  .
.
Збільшується об’єм двохатомних газів і водяної пари, 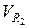 :
:
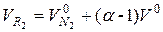 , м3/кг, (2-11)
, м3/кг, (2-11)
та 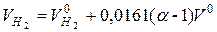 , м3/кг. (2-12)
, м3/кг. (2-12)
Тоді сумарний об’єм продуктів згорання при 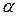 >1 буде:
>1 буде:
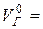
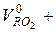
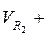
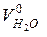 , м3/кг. (2-13)
, м3/кг. (2-13)
2.3. Підготовка палива до подачі його в котельню
|
|
|
|
|
Дата добавления: 2014-01-11; Просмотров: 3033; Нарушение авторских прав?; Мы поможем в написании вашей работы!