
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Контрольні питання до теми 3.4
|
|
|
|
Теорія хроматографічних процесів. Класифікація методів хроматографії за механізмом розділення, агрегатним станом та за технікою розділення. Хроматографічні характеристики. Основні елементи хроматографів. Їх принципи дії. Колонки. Детектори. Високоефективна рідинна хроматографія. Апаратура. Приклади використання.
Хроматографія
Хроматографічний метод аналізу знайшов широке застосування в аналітичній хімії для аналізу промислових продуктів, лікувальних препаратів, об'єктів навколишнього середовища.
Виникнення хроматографії, як наукового методу, пов’язане з ім’ям російського вченого М.С.Цвета(1872-1919), який у 1903 році здійснив розподіл суміші рослинних компонентів та заклав теоретичні основи хроматографії.
Хроматографія - це засіб розподілу речовин, заснований на різниці в їх коефіцієнтах розподілу між двома фазами, одна з котрих нерухома, а інша спрямовано рухається відносно першої. Характерними ознаками хроматографії є наявність достатньо великої поверхні розділу між фазами та динамічний засіб виконання розділу(спрямований рух однієї фази відносно іншої). Сполучення цих двох ознак робить хроматографію високоефективним методом розділу, який дозволяє відокремлювати одна від одної близькі за своїми властивостями речовини, такі як ізотопи елементні та оптично активні ізомери.
Теорія хроматографічних процесів. Хроматографічні методи розділу речовин засновані на сорбційних процесах. Сутність цих методів у тому, що розподіляємі речовини переміщуються скрізь шар нерухомого сорбенту - нерухому фазу (НФ) разом із рухомою фазою (РФ) з неоднаковою швидкістю внаслідок неоднакового сорбування. На відзнаку від деяких інших методів розділу хроматографія характеризується багаторазовим повторенням процесів сорбції та десорбції.
Принципова схема найбільш поширеного варіанту методу зводиться до такого. Перед початком аналізу хроматографічну колонку з нерухомою фазою НФ безперервно промивають рухомою фазою РФ - практично не сорбируємою речовиною (газ-носій, розчинник) і до цієї речовини на початку колонки додають невелику порцію суміші речовин А, В та С, яка підлягає аналізу(рисунок 3.11 а,б).
Кожний сорбційний процес характеризується константою розподілу (Крозд), яка являє з себе відношення рівноважної концентрації речовини в однієї певної формі у НФ (C1) до концентрації речовини у тієї ж формі у рухомій фазі РФ – (С2):
Крозд =
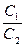 .
.
В хроматографії аналізуєма речовина може бути присутня не тільки в однієї формі. В цьомуразі застосовують коефіцієнт розподілу KD, який відображуєрівноважний розподіл речовини:
КD =  =
= 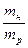
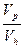 = K’
= K’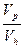 ,
,
де CAн, САр – загальна аналітична концентрація усіх форм речовини А, відповідно у нерухомій і рухомій фазах;
mн, mp – кількість речовини у нерухомій і рухомій фазах;
Vн, Vp – об’єми нерухомої та рухомої фаз;
K’ – коефіцієнт ємності.
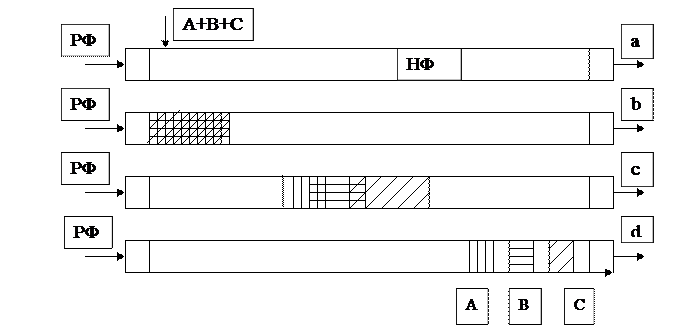
Рисунок 3.11 - Принципова схема хроматографічного розподілу.
Коефіцієнт розподілу залежитьвід природи аналізуємої речовини, походження рухомої та нерухомої фаз, температури, рН, концентрації та іонної сили розчину. Швидкість руху зони речовини зворотно пропорційно KD. При більших значеннях KD більша частка речовини знаходиться у нерухомій фазі і рухається повільно. Якщо KD мало, то речовина швидко пересувається вздовж колонки. Речовини, які мають різні значення KD, будуть пересуватися з різноманітними швидкостями, і потому можна спостерігати формування зон розподіляємих компонентів (рисунок 3.11 в, с, d).
При повному розділу зони компонентів А, В, С відокремлюються між собою чистою рухомою фазою (рисунок 3.11 d). В наслідок дифузійних процесів у рухомій та нерухомій фазах межи зон розмиваються, так що максимальна концентрація кожного компоненту виявляється зосередженою у центрі зони. Якщо на виході колонки реєструвати змінення у часі якої-небудь властивості потоку рухомої фази, то вихідна крива - хроматограма - буде мати вигляд гострих піків, які здіймаються над базовою лінією, рівень котрої по закінченню аналізу відповідає її початковому положенню на початку аналізу (рисунок 3.12). Таким чином у різні моменти часу з виходу колонки реєструється чи чиста рухома фаза (базова лінія), чи суміш – рухома фаза з розподіляємим компонентом.

Рисунок 3.12 - Хроматограма (диференційна).
Час виходу компоненту, відрахований від моменту вводу проби до моменту реєстрації вершини піку, чи інакше, об'єм рухомої фази, витрачений на пересування через колонку кожного компоненту, дають якісну характеристику речовини, яку аналізують.
Порівняння площ або висот хроматографічних піків дозволяє з високою точністю виконувати кількісні визначення.
Класифікація методів хроматографії. Існують різноманітні методи класифікації видів хроматографії. З них основними являються такі:
1.За агрегатним станом рухомої фази відокремлюють рідинну хроматографію(рухома фаза – рідина) і газову хроматографію(рухома фаза – газ). Рідинна хроматографія в залежності від агрегатного стану нерухомої фази може бути твердо-рідинною – ТРХ(нерухома фаза тверда) і рідинно-рідинною – РРХ(нерухома фаза рідина). Останню частіше характеризують як розподільну хроматографію.
Газова хроматографія може бути газ адсорбційною – ГАХ, та газорідинною, чи газорозподільною – ГРХ.
2.В залежності від механізму сорбції розрізняють молекулярну хроматографію та хемосорбційну. В молекулярній хроматографії природа сил взаємодії між нерухомою фазою та компонентами розділяємої суміші – міжмолекулярні сили типу сил Ван-дер-Ваальсу. До хемосорбційної хроматографії відносять іонообмінну, осадову, комплексоутворюючу, окисно-відновну. Причина сорбції у хемосорбційній хроматографії – відповідні хімічні реакції.
3.В залежності від способу хроматографування розрізняють хроматографію фронтальну, проявну(елюєнтну) та витіснення. В аналітичній хімії частіш за усе використовується хроматографія проявна.
4.В залежності від техніки виконання розрізняють хроматографію на колонках(нерухома фаза знаходиться у колонці), та хроматографію площинну – паперову та тонкошарову(ТЩХ), коли нерухомою фазою є лист паперу чи тонкий шар сорбенту, який нанесено на скляну чи металеву пластину.
Таблиця 3.4 - Загальна класифікація хроматографічних методів
| ВИД | НЕРУХОМА ФАЗА | РУХОМА ФАЗА | ФОРМА | МЕХАНІЗМ РОЗПОДІЛУ |
| Газова газ адсорбційна газорідинна | тверда рідина на носії | газ газ | колонка колонка | адсорбційний розподільний |
| Рідинна твердо-рідинна рідинно-рідинна іонно-обмінна осадова комплексоутво- риюча тонкошарова паперова ситова(гель- прониклива) | тверда рідина на носії тверда тверда рідина на носії тверда рідина рідина рідина у порах гелю | рідина рідина рідина рідина рідина рідина рідина рідина рідина | колонка колонка колонка колонка колонка тонкий шар тонкий шар лист паперу колонка | адсорбційний розподільний обмін іонів утворення комплексних сполук адсорбційний розподільний розподільний по розміру молекул |
Параметри утримання. При збереженні у процесі хроматографування постійними температури колонки та швидкості газу-носію, первинними, експериментально вимірюваними, параметрами хроматограми, які звуться параметрами утримання, і які являються засобами відбиття результатів  розподілу є (рисунок 3.13):
розподілу є (рисунок 3.13):
tR - час утримання;,
VR - об'єм утримання аналізуємої речовини;
l R - відстань утримання.
Час утримання характеризує здатність нерухомої фази до розділяємих речовин і визначаться, як час від моменту вводу проби у хроматографічну колонку до моменту виходу з неї максимальної концентрації визначаємої речовини. Об'єм рухомої фази, який пройшов при цьому через шар сорбенту, зветься об'ємом утримання і розраховується згідно з формулою:
VR = tR * 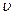 ,
,
де 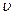 - об'ємна швидкість рухомої фази.
- об'ємна швидкість рухомої фази.
Відстань утримання l R - це відстань, яка вимірюється лінійкою від вводу проби до вершини піку. Символами Vo (t0, 1 0) відзначаються параметри утримання компоненту який не утримується сорбентом. Параметри tR VR, l R, використовуються для якісної характеристики сполуки.
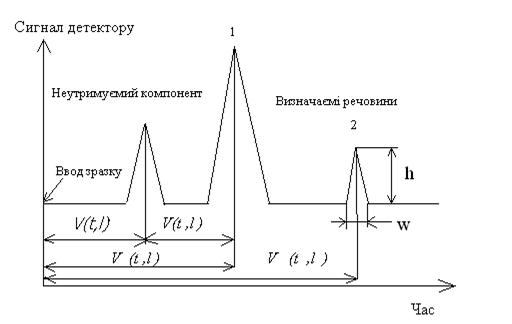
Рисунок 3.13 – Параметри хроматографи
Для порівняння результатів, отриманих на різноманітних приладах, необхідно вводити деякі поправки. Виправлений об'єм утримання V’R - об'єм утримання з урахуванням поправки на об'єм утримання не сорбіруємого газу;
V’ = VR - V0.
Виправлений час утримання:
t’R = tR – t0.
Коефіцієнт ємності може бути розраховано згідно з формулою:
K’ = 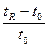 =
= 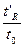 =
= 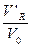 .
.
На підставі первинних, вимірюваних на хроматограмі параметрів, можливо визначити параметри, які характеризують ефективність хроматографічного розділу речовин.
В процесі руху вздовж колонки зона речовини розмивається, що відбивається на ширині хроматографічних піків. Чим більше розмивання зон двох суміжних піків, тим трудніше їх розділити. Мірою ефективності хроматографічної колонки є висота, еквівалентна теоретичній тарілці - ВЕТТ, чи Н і число теоретичних тарілок N. Число теоретичних тарілок можна розрахувати безпосередньо з хроматограми, порівнюючи ширину піку w і час перебування tR компоненту у колонці:
N = 16 .
.
Розрахував N і знаючи довжину колонки L, визначають Н:
H = 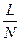 .
.
Критерій селективності Кс характеризує вибірність сорбенту. Його розраховують згідно з формулою:
Kc =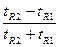 .
.
Критерій розділу R враховує дію на повноту розділу ефективності колонки та селективності сорбенту і може бути визначенеяк:
R = 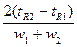 .
.
Вибір та вимірювання основних кількісних параметрів хроматографічних піків. Для кількісного аналізу по хроматограмі вимірюють площу піків, або їх висоту. Вимірювання висот піків точніше, ніж площин піків, особливо для речовин з малим часом утримання і симетричним піком. Все ж частіше вимірюють площини піків, оскільки вони практично не змінюються при нестабільності експериментальних умов. Для вимірювання площ піків запропоновано декілька графічних та інструментальних засобів. Найбільш прогресивним є вимірювання за допомогою інтеграторів та спеціалізованих ЕОМ. Однак, при обробці хроматограм, корисні навички визначення площ з використанням звичайних графічних засобів. На практиці перевагу віддають множенню висоти на полу ширину піку, оскільки цей засіб не потребує виконання допоміжних геометричних побудов, що знижує виграти часу та забезпечує більш високе відтворення і точністьрезультатів.
Методи кількісного аналізу. Основним завданням кількісного аналізу є градуіровка приладу, чи то з’ясування числової відповідності між сигналом детектору і кількістю вимірюваної речовини. Три основних засоби кількісного хроматографічного аналізу передбачають градуіровку приладу чи у прямій формі (засіб абсолютної градуіровки). чи у побічній (засіб внутрішнього стандарту, засіб нормировки).
Виконання аналізів згідно з будь яким з названих засобів включає, як початкову і одну з найважливіших процедур, приготування і хроматографування декількох штучних сумішей, які містять різноманітні кількості кожного з визначаємих компонентів, а в деяких випадках - додаткової еталонної речовини.
Засіб абсолютної градуіровки пов’язан з побудовою графічної залежності одного з кількісних параметрів хроматографічного піку (площі чи висоти) від вмісту речовини у пробі. Частіш за усе, по вісі ординат відкладають розмір висот піків h; (чи S), а по вісі абсцис - вміст речовини у пробі - g. Засобом абсолютної градуіровки частіш за усе користуються у випадках, коли є сумніви що до лінійності детектору, та коли визначаються не усі компоненти аналізуємої суміші, а тільки деякі з них наприклад, при аналізі домішок.
Засіб внутрішнього стандарту. Цей метод передбачає додаток до відомої кількості аналізуїмої проби відомої кількості еталонної сполуки, яка не присутня в пробі - внутрішнього стандарту, і хроматографування цієї суміші. Засіб зводить до мінімуму похибки, які обумовленні випадковими змінюваннями основних параметрів хроматогоафування (температури, швидкості газу-носію), бо відхилення однаково впливає на кількісні параметри хроматографічних піків стандартної та аналізуємоі речовини.
Засіб нормування. Засіб застосовується при умові реєстрації на хроматограмі усіх піків і припущенні, що сума висот усіх піків на хроматоргамі це 100%. Перевага методу міститься в усуненні необхідності точної дозировки зразку та додержанні тотожності умов аналізу при повторних визначеннях.
Основні елементи хроматографів. Розглянемо типову схему газового хроматографу(рисунок 3.14).
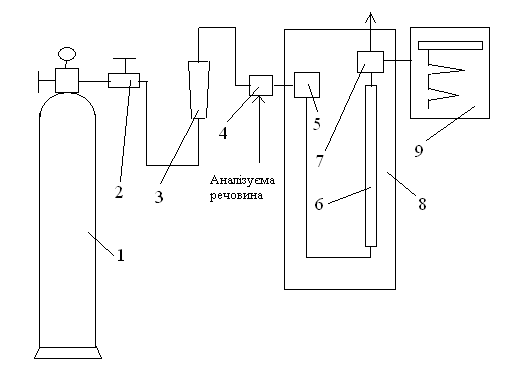
1- балон газу-носію; 2 – регулятор витрат газу; 3 – витратомір; 4 – дозатор; 5 – випаровувач; 6 – колонка; 7 – детектор; 8 – термостат; 9 – регістратор.
Рис. 3.14 - Принципова схема газового хроматографу
В склад хроматографу крім основних елементів(хроматографічна колонка, детектор) також входить ряд допоміжних пристроїв, які забезпечують необхідні умови роботи(ввід аналізуємої суміші у хроматограф, вимірювання і обробку вихідного сигналу та інше). Рухома фаза – газ-носій подається у колонку зазвичай з балону зі стиснутим газом 1. В якості газу-носія використовують гелій, азот, водень. Витрати газу-носія повинні підтримуватися сталими, бо від цього залежить чутність детектору. Витрати газу встановлюють регулятором 2 і контролюють витратоміром 3. Аналізуєма суміш вводиться у хроматограф швидко у вигляді «корки» за допомогою крану-дозатору 4 або мікрошприцем. Рідкі проби переводяться у газоподібний стан у випарувувачі 5. Газ-носій з пробою входить у хроматографічну колонку 6, яка представляє собою трубку зі скла полімерного матеріалу або металу діаметром від 1 до 6 мм і довжиною 0,5-6м. Капілярні колонки виготовляють діаметром 0,2-0,5 мм і довжиною 25-200 м. Колонка заповнюється адсорбентом(вугіль, силікагель, оксид алюмінію, цеоліти, скло). В газорідинній хроматографії використовують у якості нерухомої фази рідину, яка нанесена на твердий носій. Хроматографічні колонки встановлюють у спеціальному термостаті 8, який підтримує сталу температуру з високою точністю. Детектор 7 реагує на присутність компонентів у газі-носії. Сьогодні відомо понад 50 типів детекторів. З них найбільш розповсюджені термокондуктометричний (катарометр), полум’яно-іонізаційний, термоіонний, електронно-захватний, та деякі інші. Сучасні хроматографи як правило обладнані декількома детекторами. Перші два детектори, завдяки своїм властивостям, є найбільш універсальними і використовуються практично у більшості хроматографічних визначень.
Характерними відзнаками високоефективної рідинної хроматографії є: використання колонки з малим внутрішнім діаметром малим діаметром часток сорбенту (3-10 мкм), великим тиском елюенту (розчиннику) на вході у колонку, високою чутністю детекторів, які дозволяють визначити до 10-9-10-10 г речовини. Цей метод дозволяє аналізувати речовини з високою точкою кипіння (> 400o C), а також не стійки сполуки, яки не можна розділити методом газової хроматографії.
В високоефективній рідинній хроматографії застосовуються усі методи хроматографічного розподілу (адсорбція, розподілювальній, іонний обмін). В залежності від полярності нерухомої і рухомої фази існують два варіанти рідино адсорбційної хроматографії: нормально-фазова, та зворотно фазова. В нормально-фазової використовується полярний сорбент (частіш за усе силікагель) і неполярний розчинник (гексан). В зворотно фазової адсорбент неполярний, а розчинник полярний (спирти, вода).
Спрощена блок-схема високоефективного рідинного хроматографу наведена на рисунку 3.15.



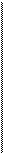
 3
3
 1
1

 |




 4
4
 2
2
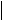




 5 7
5 7
 |
1- резервуар; 2 - насос; 3 - пристрій вводу проби; 4 - колонка; 5 - спектрофотометричний детектор; 6 - регістратор; 7 - блок управління.
Рисунок 3.15 - Спрощена блок-схема рідинного хроматографу
Насос хроматографу забезпечує подачу розчиннику (елюенту) з тиском до 5 МПа з регулюванням. Блок управління забезпечує подачу потрібного об'єму елюенту і проби від 0.1 до 2000 мкл.
Спектрофотометричний детектор забезпечує визначення оптичної густини у спектральному діапазоні 190-360 нм і має у своєму складі джерело випромінювання – дейтерієву лампу ДДС-30, монохроматор та фотометр. Принцип дії фотометра засновано в по черговому проходженні монохроматичного світового потоку через робочу та кювету зрівняння з реєстрацією потоків фото множником. Електронний блок забезпечує керування модулятором, встановлення робочої довжини хвилі та цифрову індикацію оптичної густини. Реєстрація хроматограм здійснюється за допомогою двох координатного приладу ЛКД 4-003, який дозволяє виконувати реєстрацію на звичайному папері.
Колонка для хроматографування являє сталеву нержавіючу трубку з внутрішнім діаметром 2 мм.
1.На чому засновано хроматографічний метод аналізу?
2.Які параметри хроматографи звуться параметрами утримання?
3.Що таке об’єм утримання? За якою формулою він розраховується?
4.Що таке виправлений об’єм утримання?
5.Як розраховується число теоретичних тарілок хроматографічної колонки?
6.Наведіть спрощену схему і поясніть роботу газового хроматографу.
7.Наведіть спрощену схему рідинного хроматографу.
|
|
|
|
|
Дата добавления: 2014-01-11; Просмотров: 1974; Нарушение авторских прав?; Мы поможем в написании вашей работы!