
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Внутренняя энергия: основные понятия
|
|
|
|
Лекция 2
Лекция 2. 1
Внутренняя энергия: основные понятия. 2
Измерение внутренней энергии (калориметрия) 2
Закон сохранения энергии. 3
Работа: основные понятия. 4
Теплота: основные понятия. 4
Эндотермические и экзотермические процессы.. 5
Разница между работой и теплотой (обоснование на молекулярном уровне) 5
Работа расширения идеального газа. 6
Первый закон термодинамики. 6
Работа расширения идеального газа в различных процессах. 7
Работа расширения идеального газа в изобарном процессе (Р=const) 7
Работа расширения идеального газа в изотермическом процессе (T=const) 8
Энтальпия: основные понятия. 10
Применение первого закона термодинамики. 10
Применение первого закона термодинамики в изобарном процессе 10
Применение первого закона термодинамики в изохорном процессе 11
Энтальпия идеального газа. 11
Теплоемкость. 12
Теплоемкость при постоянном объеме. 13
Молярная и удельная теплоемкость. 13
Расчет теплоемкости при постоянном объеме CV. 13
Теплоемкость при постоянном давлении. 14
Разность теплоемкостей CV и CP 15
Зависимость теплоемкости от температуры.. 16
Связь между истинной и средней теплоемкостями. 16
Определение d U и d H.. 17
Зависимость энтальпии от температуры.. 17
Вопросы для самоконтроля. 19
Энергия, U – это аддитивная функция состояния термодинамической системы.
Энергия изолированной системы постоянна.
В закрытой системе энергия может изменяться за счет:
– совершения работы W над окружающей средой (или средой над системой),
– обмена теплотой Q с окружающей средой.
Внутренняя энергия системы складывается из:
– кинетической энергии молекулярного движения
– потенциальной энергии молекул, составляющих систему
|
|
|
Обозначим ΔU – изменение внутренней энергии, если система переходит из начального состояния (U 1) в конечное состояние (U 2):
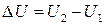
Внутренняя энергия является функцией состояния (переменной состояния). Изменение термодинамических параметров приводит к изменению внутренней энергии.
Напомним, что переменная (функция) состояния – это величина, которая зависит только от состояния системы в начальном и конечном состоянии и не зависит от пути процесса.
В термодинамике энергия процесса считается положительной, если внутренняя энергия системы увеличивается в ходе процесса.
|
|
|
|
|
Дата добавления: 2014-01-11; Просмотров: 645; Нарушение авторских прав?; Мы поможем в написании вашей работы!