
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Флавоноиды
|
|
|
|
Гликозиды различного состава.
По физико-химическим свойствам гликозиды - как правило, кристаллические вещества, часто горького вкуса, бесцветные или окрашенные. В большинстве своем они легко растворимы в воде и спирте, плохо растворимы или нерастворимы в неполярных органических растворителях. Обладают оптической активностью.
Гликозиды широко распространены в растительном мире и могут содержаться во всех частях растений в растворенном виде в клеточном соке.
Важным свойством гликозидов является их способность к спонтантанному ферментативному гидролизу. В случае, если гликозид содержит несколько сахаров (три и более), то под действием эндогенных ферментов происходит ступенчатый гидролиз и из “первичного” гликозида при отщеплении концевого сахара возникает “вторичный”, затем “третичный” и т.д. Тип фармакологического действия при этом не изменяется, так как он детерминирован структурой агликона, но могут существенно изменяться фармакокинетические параметры (скорость наступления эффекта). Это обусловлено тем, что сахарный компонент существенно влияет на растворимость, и, следовательно, на всасываемость гликозида в организме. Для некоторых групп гликозидов это обстоятельство не имеет существенного значения (например, ряда флавоноидов, антрагликозидов и др.), для других же (сердечные гликозиды), оно является весьма важным.
Флавоноидами называется группа природных кислородсодержащих гетероциклических соединений, производных бензо-g-пирона. Они являются одной из самых распространенных групп фенольных соединений растительного происхождения, объединенных общим структурным составом С6-С3-С6 (дифенилпропан).
|
|
|
В зависимости от степени окисленности g-пиранового цикла большинство флавоноидов можно рассматривать как производные хромона или хромана, содержащие в положении 2, 3 или 4 арильный радикал:
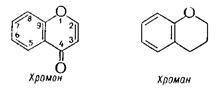
Свое название они получили от латинского слова “flavus” - желтый, поскольку первые выделенные из растений флавоноиды имели желтую окраску.
Основные исследования по выяснению химической природы флавоноидов и их синтезу были проведены на рубеже XIX и XX веков А.Г. Перкиным, С. Костанецким, Р. Робинсоном и др. Начало отечественным работам по изучению флавоноидов растений положено в 1863 г. русским ботаником А.П. Бородиным. В первые годы XX столетия Н.А. Валяшко определил строение ряда флавоноидов, в частности, им была установлена структура такого широко известного в настоящее время флавоноида, как рутин.
Распространение в растительном мире и роль флавоноидов в растениях. Флавоноидные соединения в большем или меньшем количестве содержатся почти во всех растениях; их встречаемость в высших растениях достигает 80%. Флавоноиды присущи в основном высшим растениям, однако встречаются также в водорослях, грибах и мхах. Наиболее богаты флавоноидами растения семейств Fabaceae, Rutaceae, Polygonaceae, Rosaceae, Asteraceae.
Флавоноиды представляют собой группу растительных пигментов, сочетание которых определяет ту или иную окраску цветков и плодов.
В растениях флавоноидные красители играют роль светофильтров, защищающих ткани от отрицательного влияния ультрафиолетовых лучей. Подтверждением этому может служить тот факт, что разбавленный раствор кверцитина или апигенина почти целиком поглощает излучение в ультрафиолетовой части спектра.
Флавоноиды участвуют в процессе дыхания растений: совместно с аскорбиновой кислотой принимают участие в ферментативных окисльно-восстановительных процессах.
Локализуются флавоноиды главным образом в листьях, цветках и плодах, реже в стеблях и подземных органах. В растениях большинство флавоноидов (за исключением катехинов и лейкоцианидинов2) присутствует в виде гликозидов, растворенных в клеточном соке. Сахарная часть в флавоноидных гликозидах представлена D-глюкозой, D-галактозой, D-маннозой, L-арабинозой и L-рамнозой. Из уроновых кислот обычно встречается D-глюкуроновая кислота. Присоединение сахаров происходит обычно по месту расположения гидроксилов в положении С-3 или С-7. Значительно реже возможно присоединение углеводного компонента в положении С-3¢ или С-4¢.
|
|
|
Классификация флавоноидов. Классификацияфлавоноидов производится по следующим признакам. 1. Местоположение бокового фенильного радикала; 2. Структура и степень окисленности пропанового фрагмента.
По пкрвому признаку различают следующие основные группы флавоноидов.
1. Собственно флавоноиды (эуфлавоноиды) с боковым фенильным радикалом у С-2;
2. Изофлавоноиды с боковым фенильным радикалом у С-3;
3. Неофлавоноиды с боковым фенильным радикалом у С-4;
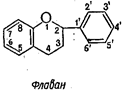
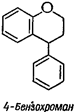
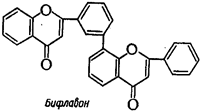
4. Бифлавоноиды - конденсированная система из двух молекул флавоноидов, соединенных по С-5’ - C-8 углеродным атомам:
| 
| 
| 
|
Подробно рассмотрим эуфлавоноиды, поскольку представители этой группы наиболее широко используются в медицинской практике.
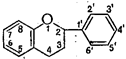
По степени окисленностипиранового кольца (пропанового фрагмента) эуфлавоноиды подразделяют на две подгруппы - производные флавона и производные флавана:
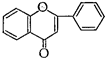
| 
|
Флавон Флаван
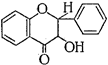
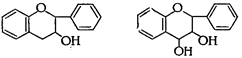
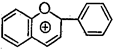
В свою очередь в подгруппе флавона выделяют производные флавонола, а в подгруппе флавана - производные флаванона, флаванонола, катехина, лейкоцианидина и антоцианидина:
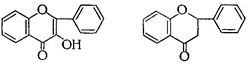
| 
|
Флавонол Флаванон Флаванонол
| 
|
Катехин Лейкоцианидин Антоцианидин
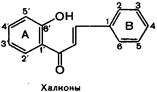
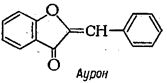
К эуфлавоноидам относятся также соединения с видоизмененным пирановым циклом - халконы и ауроны:
| 
|
Биогенез флавоноидов в растениях. Известны два основных пути образования в растениях фенольных соединений: шикиматный путь – обязательным участником этого процесса является шикимовая кислота; и ацетатномевалоновый путь - связанный с промежуточным синтезом поликетидных (ацетатных) соединений и часто протекающий с участием мевалоновой или малоновой кислот.
|
|
|
Флавоноиды, как группа фенольных соединений, синтезируется по смешанному шикиматно-ацетатномевалоновому пути: кольцо В и трехуглеродный фрагмент – по шикиматному, а кольцо А флавоноидов – по ацетатно-мевалоновому. Необходимо отметить, что конечные продукты синтеза существуют в виде активных форм: кумароилконзима А и малонилкоэнзима А соответственно.
Схематично биосинтез флавоноидов в растениях можно представить следующим образом (некоторые промежуточные продукты биогенеза опущены).
1. Шикиматный отрезок пути биогенеза флавоноидов:
| Крахмал (гликолиз) ® Глюкоза ® Глюкозо-6-фосфат ® … | 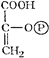 Фосфоенол-пируват
Фосфоенол-пируват
| + |  Эритрозо-4-фосфат[3]
Эритрозо-4-фосфат[3]
| ® | |||||
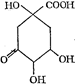 5-дегидрохинная кислота
5-дегидрохинная кислота
| + АТФ ® … + СН3СООН | 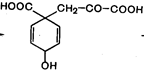 Префеновая кислота
Префеновая кислота
| + NH3 ® … - СО2 |
 Тирозин
Тирозин
| |||||
| - NH3 ® … | 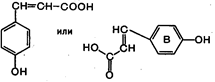 Кумаровая кислота
Кумаровая кислота
| ||||||||
2. Ацетатно-мевалоновый отрезок пути биогенеза флавоноидов:
| Крахмал (гликолиз) ® Глюкоза ® Глюкозо-6-фосфат ® … Фосфоенолпируват ® СН3СОСООН Пировиноград- ная кислота | ||
| + 2СН3СО~S-СоА + 2НООС-СН2-СО~S-Co A ® СН3СО~S-СоА ® ® НООС-СН2-СО~S-Co A ® Ацетилкоэнзим А - 2HSCo A Малонилкоэнзим А | ||
| ® | 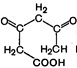
| Триуксусная кислота |
3. Заключительная стадия биогенеза флавоноидов.
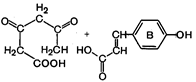
| - Н2О ® | 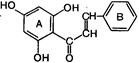 Халкон
Халкон
| ® | Все остальные группы флавоноидов |
Физико-химические свойства флавоноидов. Большинство флавоноидов в чистом виде - кристаллические вещества с фиксированной температурой плавления, горького вкуса, бесцветные или окрашенные в желтый, красный или синий цвет с зависимости от рН среды. Они, как правило, хорошо растворимы в полярных растворителях, в метаноле, бутаноле и растворах щелочей.
Флавоноидные гликозиды растворимы в воде, но агликоны в воде обычно растворяются плохо. Большинство агликонов флавоноидов растворимы в ацетоне, этилацетате, хлороформе и других гидрофобных растворителях.
Наличие фенольных гидроксильных групп обусловливает кислые свойства флавоноидов и их способность к образованию фенолятов в щелочной среде.
|
|
|
Благодаря наличию фенольных гидроксилов флавоноиды легко окисляются. Легкая окисляемость флавоноидов способствует восстановлению других веществ в реакционной смеси или препятствует их окислению. Такое свойство флавоноидов называется антиокислительным или антиоксидантным. Флавоноидные антиоксиданты способны даже в незначительных количествах сильно угнетают процессы окисления.
Флавоноидные гликозиды обладают оптической активностью и способностью избирательно поглощать свет в ультрафиолетовой части спектра в зоне длин волн 250-280 нм, что обусловлено наличием в молекуле фалавоноидов двух или более бензольных колец. Одна из характерных особенностей флавоноидных гликозидов - это способность к кислотному и ферментативному гидролизу, причем условия и скорость гидролиза специфичны для различных групп гликозидов. Например, флавонол-3-гликозиды легко гидролизуются при нагревании с разбавленными (0,2-1%) минеральными кислотами, флавон-7-гликозиды гидролизуются лишь при нагревании с 5-7% минеральными кислотами, а флавоноидные С-гликозиды гидролизуются только смесью концентрированных соляной и уксусной кислот (смесь Килиани).
Выделение флавоноидов из растительного сырья. Для флавоноидов не существует универсального метода выделения из растительного сырья, так как они очень сильно различаются по своей растворимости в воде или органических растворителях. В каждом конкретном случае прибегают к наиболее подходящему методу или сочетанию методов с учетом свойств выделяемых веществ, свойств возможных сопутствующих соединений и особенностей растительного сырья. Наиболее часто применяют избирательную экстракцию, осаждение солями тяжелых металлов и хроматографические методы.
С целью удаления из сырья липофильных примесей, его предварительно обрабатывают петролейным эфиром или четыреххлористым углеродом. Затем проводят экстракцию флавоноидов одним из подходящих растворителей: этанолом, метанолом, горячей водой или смесью хлороформа со спиртом.
Для предварительного суждения о содержании в исследуемых видах растений флавоноидов обычно используют следующий способ их выделения.
Навеску суховоздушных частей растения обрабатывают 70% этанолом или метанолом. Настаивают в течение суток, или проводят извлечение в аппарате Сокслета, или кипятят в течение 30 мин с обратным холодильником. Полученные спиртовые извлечения хроматографируют на бумаге или в тонком слое сорбента, а затем хроматограммы проявляют соответствующим реагентом.
При таком способе извлечения наряду с суммой флавоноидов экстрагируется большое количество сопутствующих веществ, отделение которых производят, как правило, хроматографическими приемами. Наиболее часто с этой целью применяют колоночную хроматографию, используя в качестве носителя полиамид, целлюлозу или силикагель. Элюирование проводят с помощью водных растворов метанола или этанола в различных концентрациях или смесью этилацетата и этанола (метанола).
Контроль за ходом разделения флавоноидов проводят методом хроматографии в тонком слое или на бумаге.
Качественный анализ сырья, содержащего флавоноиды. Флавоноидные соединения в растительном сырье обнаруживают качественными реакциями в водных или спиртовых извлечениях. Общие реакции, специфичные для всех групп флавоноидов, отсутствуют. Наиболее часто используют следующие реакции.
1. Цианидиновая проба или проба Chinoda - реакция восстановления препарата атомарным водородом в кислой среде в присутствии магния. При этом развивается окраска от оранжевой до красно-фиолетовой, что зависит от количества и местоположения оксигрупп.
Если заменить магний на цинк, то это приводит к изменению окраски, кроме того, отрицательной оказывается реакция на флавононы. Цианидиновую пробой не обнаруживаются халконы и ауроны.
2. Взаимодействие со щелочами. Эта реакция проводится для определения основного структурного типа флавоноидов, для определения числа и ориентации гидроксильных групп. Так например, с раствором аммиака флавоны, флавонолы, флаваноны и флаванонолы дают желтое окрашивание, при нагревании переходящее в оранжевое или красное. Халконы и ауроны дают красное или пурпурное окрашивание. Антоцианы - синее или фиолетовое.
3. Реакция с минеральными кислотами. При действии на флавоны и флавонолы минеральных кислот образуются интенсивно-желтые соли оксония.
4. Реакция с солями тяжелых металлов. Флавоны, халконы, ауроны, содержащие свободную ортогидроксильную группу в кольце В, при обработке их ацетатом свинца окрашиваются в ярко-желтый цвет.
Флавоноидные соединения, содержащие эти группировки, образуют ярко окрашенные комплексы с ионами таких металлов, как алюминий, цирконий, причем эти комплексы часто имеют яркую флуоресценцию в УФ свете, что используется при исследовании флавоноидных соединений методом хроматографии на бумаге и в тонком слое.
5. Проба с треххлористой сурьмой. Халконы с раствором треххлористой сурьмы в четыреххлористом углероде окрашиваются в красный или красно-фиолетовый цвет, флавоны - в желтый или желто-оранжевый.
6. Реакция с реактивом Вильсона (борная и лимонная кислота, растворенные в безводном ацетоне). С реактивом Вильсона флавоны и флавонолы образуют желтую окраску с красноватой флуоресценцией в УФ свете.
Флавоноиды можно обнаружить путем просмотра результатов хроматографии на бумаге в ультрафиолетовом свете. При этом флавоны, флавонол-3-гликозиды, флаваноны и халконы обнаруживаются в виде коричневых пятен; флавонол-7-гликозиды - желтых или желто-зеленых пятен.
Количественное определение флавоноидов. Для определения количественного содержания флавоноидов в сырье используют различные методы: химические, физические, физико-химические.
Наличие фенольных гидроксилов, обусловливающих слабокислотные свойства флавоноидов, позволяет использовать для анализа метод кислотно-основного титрования в неводных средах.
Флавоноиды обладают значительной интенсивностью поглощения в УФ-области спектра. Это свойство используется при спектрофотометрических методах количественного определения.
Широко применяются фотометрические методы, основанные на измерении интенсивности окрашивания продуктов реакции флавоноидов с различными реагентами. Наиболее часто для этой цели используются соли алюминия, хрома, циркония и т.д. Метод дает стабильные результаты, однако он не обладает специфичностью и требует предварительного разделения флавоноидов.
Существуют и другие методы количественного определения флавоноидов - флуориметрические, полярографические, комплексонометрические, но используются они довольно редко.
Наиболее точным, приемлемым методом количественного определения флавоноидов является хроматоспектрофотометрический, основанный на разделении этих веществ хроматографией на бумаге или в тонком слое с последующим установлением их содержания в элюатах.
|
|
|
|
|
Дата добавления: 2014-01-11; Просмотров: 3006; Нарушение авторских прав?; Мы поможем в написании вашей работы!