КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Химические свойства. Кислота Метиловые эфиры Этиловые эфиры Т пл, оС Т кип, оС
|
|
|
|
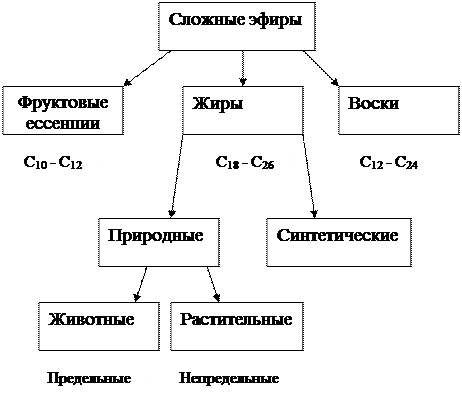
Сложные эфиры
| Кислота | Метиловые эфиры | Этиловые эфиры | |||||||||
| Т пл, оС | Т кип, оС |
| Т пл, оС | Т кип, оС |
| ||||||
| Муравьиная (Ткип= + 100,5оС) | - 99,0 | + 31,8 | 0,975 | - 78,9 | + 54,3 | 0,923 | |||||
| Уксусная (Ткип= + 118,5оС) | -98,1 | + 57,0 | 0,934 | - 83,4 | + 77,2 | 0,901 | |||||
| Пропионовая (Ткип= + 141,1оС) | - 87,5 | + 80,6 | 0,915 | -73,9 | + 99,1 | 0,888 |
1. Реакции с нуклеофильными реагентами.
2. Восстановление.
3. Реакции подвижного атома водорода в a-положении по отношению к карбонильной группе
1. Реакции с нуклефильными реагентами (Н2О, ROH, NH3 и т.д.)
1.1. Гидролиз
1.1.1. Гидролиз в кислой среде
Гидролиз сложных эфиров активизируется кислотами за счет протонирования карбонильной группы, что приводит к усилению ее поляризации и повышению электрофльноости ключевого атома углерода:
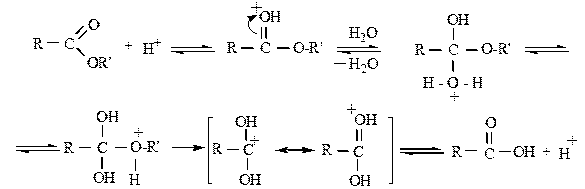 |
С точки зрения механизма гидролиз сложных эфиров аналогичен этерификации карбоновых кислот.
Основное условие полного гидролиза – избыток воды, что позволяет обеспечить необходимое смещение равновесия на соответствующих стадиях процесса /10/.
1.1.2. Гидролиз в щелочной среде.
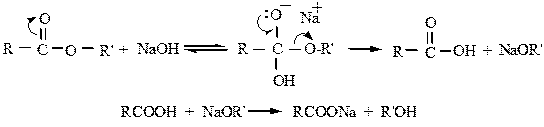 |
Исторически первым примером такой реакции было щелочное расщепление эфиров высших жирных кислот, что приводило к получению мыла. Отсюда появился термин – «омыление», используемый и до сегодняшнего дня.
1.2. Переэтерификация.
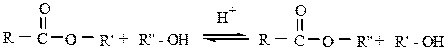 |
Если заменить воду на спирт (или другой нуклеофил), то гидролиз не будет происходить, а один эфир будет превращаться в другой. Этот процесс называется переэтерификацией.
1.2.1. Переэтерификация спиртами протекает и в кислой среде
Реакция ацилирования – введение в молекулу нуклеофила ацильного остатка.
Механизм аналогичен механизму гидролиза в кислой среде.
Оставить место – написать самостоятельно.
1.2.2. Переэтерификация спиртами в щелочной среде.
Здесь атакующий спирт под действием основания превращается в алкоксид-ион – более сильный нуклеофил:
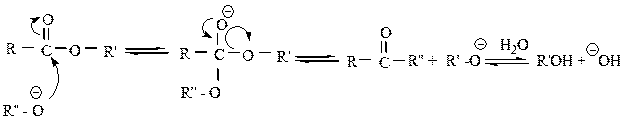 |
1.2.3. Переэтерификация кислотами.
1.2.4. Переэтерификация эфирами.
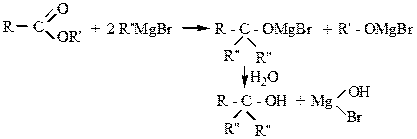 |
2. Примером восстановления является реакция с реактивом Гриньяра, при этом сложные эфиры образуют третичные спирты:
3. Сложноэфирная конденсация или конденсация Кляйзена.
Карбонильная группа сложных эфиров за счет -I – эффекта своего атома углерода и s -p - сопряжения придает кислотность a - водородным атомам. Депротонирование сложных эфиров может осуществляться под действием алкоголятов:
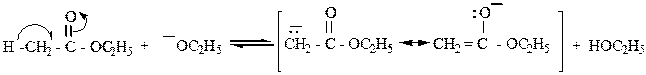
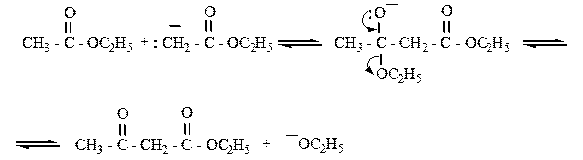 |
Образующийся катион из-за своей нуклеофильности атакует вторую молекулу сложного эфира; при этом возникает связь С-С и образуется оксоэфир:
Реакция обратима: равновесие модно сдвинуть вправо путем отгонки образующегося этанола, что технически трудно. Поэтому применяют избыток этилата натрия, который реагирует с оксоэфиром и тем самым выводит его из равновесия.
 |
|
|
|
|
Дата добавления: 2014-01-11; Просмотров: 375; Нарушение авторских прав?; Мы поможем в написании вашей работы!