
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Фізичні основи теорії корозії металів
|
|
|
|
Як уже зазначалося, за типом корозійного процесу розрізняють електрохімічну і хімічну корозію. За видом корозійного середовища корозія буває атмосферна, ґрунтова чи в морській воді. На рис. 13.1 зображено види корозійного руйнування (суцільне, поверхневе, міжкристалічне і корозійні тріщини).

Рис. 13.1. Види корозійного руйнування:
а - суцільне; б - поверхневе; в - міжкристалічне; г - тріщини
З точки зору фізичної природи процесу корозії електрохімічною корозією називають таку корозію, яка супроводжується появою електричного струму і наявністю рідини - електроліту. Електролітами можуть бути електропровідні рідини: луги, розчини кислот, солей, газів.
При контакті металу та електроліту іони з поверхні металу переходять в електроліт, і спричиняють виникнення між ними електрорушійної сили (ЕРС).
При розчиненні металу в електроліт переходять лише позитивно заряджені іони. Тому електроліт, що контактує з металічною пластинкою, заряджається позитивно, а сама пластинка - негативно за рахунок електронів, що залишилися на ній. Якщо порівняти метали за здатністю "переходити в розчин", то вона різна. Тому якщо пластинки різних металів опустити в один електроліт, то вони будуть мати різні потенціали, причому чим більше іонів металу перейде в розчин, тим більшим буде негативний потенціал цього металу. Значення потенціалів розчинення деяких елементів наведено в табл. 13.1 (вимірювання зроблено по водневому електроду, потенціал якого прийнятий рівним нулю).
Таблиця 13.1
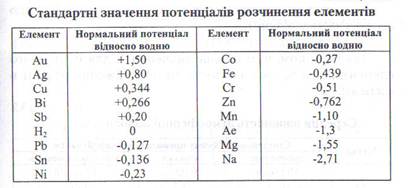 |
Якщо з'єднати провідником різні металічні пластинки, що знаходяться в електроліті, то утворюються гальванічні пари, де анодом є метал з нижчим потенціалом, а катодом - метал з вищим, тобто більш електронегативним потенціалом відносно Н2.
З точки зору термодинаміки напрямок проходження будь-якої хімічної реакції, в тому числі між металом і середовищем, визначається зміною вільної енергії Гіббса, АС.
Чим більше від'ємне значення АС, тим більша реакційна взаємодія:
02
Мg+Н2О → Мg(ОН)2; ∆G = -598 Дж (-142,600 кал),
02
Аu+Н2О → Аu(ОН)3; ∆G = +66 Дж (15,700 кал).
Велике від'ємне значення АС вказує на "здатність" металу до взаємодії з водою і киснем. Позитивне значення АС в Аи вказує на те, що в даних умовах реакція не пройде.
З точки зору електрохімічного механізму корозії спорідненість металу до корозії виражається через ЕРС корозійних елементів:
∆G = - Е ·п · F,
де Е - ЕРС;
п - кількість електронів (або хімічних еквівалентів, що беруть участь у реакції);
Р - число Фарадея (96500 кулонів на хімічний еквівалент).
Таким чином, чим більше значення Е для будь-якого елемента, тим більша здатність до проходження реакції в елементі.
Таблиця 13.2
Середня швидкість атмосферної корозії *, мм/рік
| Метал | Середовище, в якому проводяться випробування | ||
| промислове | морське | сільська місцевість | |
| 10 років | 10 років | 10 років | |
| А1 | 0,84 | 0,7 | 0,02 |
| Сu | 1,19 | 1,32 | 0,58 |
| РЬ | 0,43 | 0,41 | 0,48 |
| Sn | 1,19 | 2,31 | 0,46 |
| Ni | 3,25 | 0,10 | 0,15 |
| Zn | 5,10 | 1,60 | 0,86 |
| Сталь | 12,19 | 1,75 | 1,07 |
* Фактори впливу: температура, час, середовище, склад металу (наявність захисної плівки).
3. ВИДИ КОРОЗІЙНОГО РУЙНУВАННЯ
За характером руйнування поверхні металів або зміною механічних властивостей корозію класифікують на 5 основних типів:
І. Рівномірна корозія - втрата маси на одиницю площі за одиницю часу, виражається у мм/рік, мг/дм2 за добу.
У випадку рівномірної корозії метали відповідно до швидкості корозії поділяються на три групи:
1) менше 0,127 мм/рік - метали із хорошою корозійною стійкістю. Із них виготовляють вали насосів, пружини тощо;
2) від 0,127 до 1,127 мм/рік - із задовільною стійкістю (цистерни, трубопроводи, вентилі);
3) більше 1,27 мм/рік - із незадовільною стійкістю проти корозії.
II. Пгтингова, або острівкова корозія - це корозія на невеликих ділянках, є місцевою корозією.
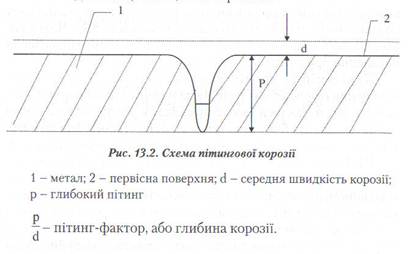 |
Цей пітинг-фактор - відношення найглибшого пітингу до середньої швидкості корозії, що визначається за втратами маси.
Таблиця 13.3
Корозія сталей, міді, цинку, свинцю в ґрунтах після витримки х років, мг/дм2 за добу
| Ґрунт | Сталь, х=12 років | Мідь, х=8 років | Свинець, х=12 років | Цинк, х=11 років |
| Ґрунт (середні дані) | 4,5 | 0,7 | 0,52 | 3,0 |
| Глина | 13,7 | 0,7 | 0,6 | - |
| Суміш із гравієм | 0,9 | 0,2 | 0,13 | - |
Залізо, що знаходиться в землі, кородує з утворенням неглибоких пітингів, а для нержавіючих сталей, що знаходяться в морській воді, характерна корозія з утворенням глибоких пітингів. Багато металів схильні до пітингової корозії через вплив рідин, які швидко перемішуються. Цей різновид впливу називається ударною корозією або корозійною ерозією.
Мідні і латунні конденсаторні трубки піддаються пітинговій корозії. Фретинг-корозія виникає внаслідок пересування двох контактуючих тіл або хоча б одного металевого тіла. Частинки оксидів металу заповнюють утворені пітинги, і тому тільки після видалення продуктів корозії їх можна побачити.
Кавітаційна ерозія виникає внаслідок утворення і зникнення газоподібних пузирів на поверхні розділення метал-рідина, що рухається (як наприклад, у роторі насоса чи на гребному гвинті з боку руху рідини). Вона утворює ряд пітингів у вигляді тріщин малої глибини, розташованих немов стільники.
III. Вибіркова корозія - це корозія, при якій розчиняються переважно один компонент сплаву. Знецинкування - це тип корозійного руйнування, що спостерігається у цинкових сплавів. Наприклад, латунь: у цьому випадку цинк розчиняється, і залишається пориста мідь. Кородуючи таким чином, метал часто зберігає свій початковий вигляд і може здаватися незруйнованим (якщо не брати до уваги тьмяну поверхню). Однак його міцність при розтягненні, особливо пластичність, значно знижуються.
Знецинковані латунні трубки можуть зберігати достатню стійкість і протидіяти внутрішньому тиску води до того часу, поки не буде необхідності роз'єднати трубки або не виникне удар водою, що може викликати їх розтріскування.
Вибіркова корозія спостерігається у сплавів благородних металів: Аu-Сu, Аu-Аq. Це використовується при очищенні золота. Наприклад, сплав Аu-Аq що містить більше 65% Аu, стійкий у концентрованій НNО3 і утворює АqNО3 і пористу губку (або чистий порошок золота).
Мідні сплави, які містять алюміній, схильні до корозії, що нагадує знецинкування, з переважним розчиненням алюмінію.
IV. Міжкристалгчна корозія - це місцева корозія, що виникає на межі зерен металу, внаслідок неї метал втрачає стійкість і пластичність. Межі зерен, що мають малу площу і діють як анод, контактують з більшою поверхнею зерен, які діють як катоди. Процес відбувається швидко, проникаючи в глибину металу, і інколи викликає катастрофічні руйнування. Неправильно термооброблені нержавіючі сталі або сплави типу дюралюмінію є сплавами, схильними до цієї корозії. Прикладом неелектрохімічного впливу на межі зерен може бути руйнування нікелю, нагрітого в атмосфері, яка містить сполуки сірки, внаслідок проникнення сірки по межах зерен.
V. Розтріскування. Якщо метал, який перебуває в коро
зійному середовищі під впливом повторних або змінних
напружень при розтягненні, розтріскується, то кажуть, що він
руйнується внаслідок корозійного старіння.
4. СПОСОБИ ЗАХИСТУ ВІД КОРОЗІЇ
Способи захисту від атмосферної корозії:
1) нанесення органічних, неорганічних або металевих покриттів;
2) зменшення відносної вологості (до 50%);
3) використання інгібіторів і мастил;
4) легування металів.
Лакофарбові покриття, що часто використовуються для захисту від атмосферної корозії, в ґрунтах руйнуються впродовж кількох місяців.
Для захисту від підземної корозії доцільно наносити пластмасові покриття на основі кам'яновугільної смоли з доданням армувальних пігментів або неорганічних волокон для зменшення розм'якшення покриттів при звичайних температурах. Ці покриття мають помірну вартість і тому широко використовуються.
Приклади інших покриттів:
• з каучуку (вони захищають сталь від корозії приблизно на 11 років);
• із цементу на сталь (ці покриття на багато років зберігають від корозії);
• із склоподібної емалі. Це і попереднє покриття характеризуються крихкістю;
• із цинку (але не можна, щоб вони контактували з незахищеними поверхнями сталі або міді, тому використовують ізолюючі прокладки).
Як правило, всі сучасні підземні трубопроводи і резервуари захищають від корозії за допомогою катодного захисту в поєднанні з армованими покриттями на основі кам'яновугільної смоли. При цьому досягається ефективний і економічно доцільний захист сталі від корозії в усіх ґрунтах. :
Види антикорозійних покриттів:
1) металеві (Nі, Zu, Рb, Сd, Sn, Аl, Сu);
2) неорганічні (склосилікатні, цементні, фосфатні, оксидні, хромові);
3) органічні (пластмасові, епоксидні, гумові).
Інгібітор - речовина, при додаванні якої в середовище, де знаходиться метал, значно зменшується швидкість корозії металу.
Класифікація інгібіторів:
1) пасиватори;
2) органічні мастила і травильні присадки (віск, парафін, тощо);
3) парофазні інгібітори.
Пасиватори - окисники (хромати, нітрати, молібдати), що пасивують (облагороджують) потенціал корозії на кілька десятих вольта.
Травильні присадки - наприклад, 0,01-0,1% уротропін, сечовина та інші домішки.
В Україні є досвід попередження корозії обладнання в природних та інших водах за допомогою методів, які базуються на видаленні кисню із води (застосуванні речовин, що утворюють плівки). Для захисту від корозії апаратів, які обігріваються гарячою водою, ефективне використання силікатної обробки води та хімічної пасивації обладнання. Є перспективними методи, які ґрунтуються на іонному осадженні та іонній імплантації.
Надійність усіх технологічних систем підвищиться, якщо вибір оптимальних засобів протикорозійного захисту буде проводитися на стадії проектування підприємств. В Україні питаннями корозійного руйнування та захисту металів займається Фізико-механічний інститут НАН України (м. Львів).
Література
1. Томашев Н.Д. Теория коррозии й защитьі металлов. -М.: АН СССР, 1960. - 591 с.
2. Колотьіркин Я.М., Каспарова О.В. Коррозия й защита от коррозии. - М.: ВИНИТИ, 1978. - Т. 6. - С. 180-217.
3. Андресюк Е.Й. й др. Микробная коррозия й ее воз-будители. - К.: Наукова думка, 1980. - 287 с.
4. Жук Н.П. Курс теории коррозии й защитьі металлов. -М.: Металлургия, 1976. - 472 с.
5. Корозійно-механічне руйнування зварних конструкцій / В.І. Пахмурський, Р.К. Мелахов, Г.М. Круцан, В.Г. Зданов-ський. - К.: Наукова думка, 1995. - 260 с.
6. Техника борьбьі с коррозией / Под ред. А.М. Сухотина. - Л.: Химия, 1980.
7. Аскользин А.П., Жуков А.П. Кислородная коррозия оборудования химических производств. - М.: Химия, 1985. - 240 с.
|
|
|
|
Дата добавления: 2014-01-11; Просмотров: 1249; Нарушение авторских прав?; Мы поможем в написании вашей работы!