
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Строение металлов и сплавов, их кристаллизация
|
|
|
|
"V/ о ' Внутренним строением металлов называется строение
и взаимное расположение их атомов, а также более крупная структура, видимая в микроскоп или невооруженным глазом.
Металлы по внутреннему строению представляют собой совокупность нейтральных атомов, положительно или отрицательно заряженных ионов и свободных электронов, образующих так называемый «электронный газ». Наличие «электронного газа» обусловливает высокую электро- и теплопроводность металлов, а взаимосвязь свободных электронов между собой и с ионами создает прочную связь, называемую металлической. Специфика металлической связи делает металлы пластичными (ковкими).
Кроме природы атомов на свойства металлов влияют характер связи между атомами, расстояние между ними и порядок их расположения.
Все металлы в твердом состоянии имеют кристаллическое строение, т. е. их атомы (ионы) расположены в строгом, периодически повторяющемся порядке, образуя,'в пространстве атомно-кристаллическую решетку (в противоположность аморфным твердым телам, атомы которых расположены в пространстве хаотично).
Порядок расположения атомов у различных металлов неодинаков. Обычно он определяется простыми ха-
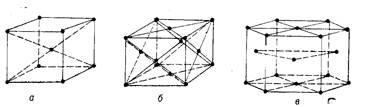
Рис. 6. Порядок расположения атомов в простых реше-ках:
а— объемно-центрированной кубической (9 атомов); б— гранецентрирован-ной кубической (14 атомов); в — гексагональной плотноупакованной (17 атомов).
рактерными для большинства металлов (рис. 6) или сложными кристаллическими решетками. Линии на рис. 6 условные. Атомы 'в действительности колеблются возле положений равновесия, т. е. в узлах кристаллической решетки. Расстояние между атомами в кристаллической решетке измеряется в ангстремах (1А==10~9 нм). У большинства металлов расстояние между атомами находится в пределах 0,28—6,8 нм.
Наименьший объем кристалла, дающий представление об атомной структуре металла во всем объеме, называется элементарной кристаллической ячейкой.
Получаемые обычным способом металлы представляют собой поликристаллические тела, состоящие из множества элементарных ячеек, ориентированных относительно друг друга самым различным образом. Ячейки имеют неправильную форму и называются кристаллитами, или зернами. Если сочетание элементарных ячеек правильное, по расположению атомов повторяющее элементарную ячейку, то образовавшееся тело называется монокристаллом.
Металлические сплавы, как и металлы, имеют кристаллическое строение. При этом в зависимости от взаимодействия компонентов они подразделяются на твердые растворы, химические соединения и механические смеси.
Твердые растворы образуются тогда, когда при сплавления атомы одного элемента в разных количествах входят в кристаллическую решетку другого элемента, не изменяя в значительной мере ее формы. Элемент, сохранивший форму своей решетки, называется растворителем, а элемент, атомы которого вошли в эту решет- • ку,—растворенным. По размещению атомов растворенного элемента в решетке растворителя различают твер-
дые растворы замещения (атомы растворенного элемента располагаются в узлах решетки растворителя) и твердые растворы внедрения (атомы растворенного элемента находятся между атомами растворителя и узлами его решетки).
Если входящие в состав твердого раствора замещения компоненты имеют близкое строение решеток и атомов, то такие элементы могут образовывать непрерывный ряд твердых растворов, т. е. количество замещенных атомов может изменяться от 0 до 100 %.
При этом считается, что растворителем является тот элемент, содержание которого в сплаве более 50 %.
Растворы внедрения образуются элементами, сильно отличающимися строением решетки и размерами атомов.Твердые растворы являются гомогенными (однородными) сплавами, так как их структура представляет собой одинаковые по составу и свойствам зерна. Свойства твердых растворов ib значительной степени могут отличаться от свойств входящих в него компонентов. Все металлы в той или иной степени могут растворяться один в другом, образуя твердые растворы.
Химические соединения образуются при химическом взаимодействии атомов компонентов сплава, сопровождающемся значительным тепловым эффектом. При этом кристаллическая решетка химического соединения и все его свойства могут резко отличаться от решетки и свойств компонентов. В огличие от твердых растворов химические соединения обычно образуются между компонентами, имеющими большое различие в электронном строении атомов. Типичными примерами химических соединений являются соединения магния с оловом, свинцом, сурьмой, висмутом, серой, селеном, теллуром и др. По своей структуре они гомогенны.
Химические соединения металлов называются интерметаллическими (интерметаллидами), а соединения металлов с неметаллами (нитридами, гидридами, борида-ми, карбидами), обладающие металлической связью,— металлическими соединениями.
Механические смеси образуются тогда, когда при затвердении расплава атомы его компонентов не перемешиваются, а кристаллизуются в характерную каждому решетку. Структура таких сплавов гетерогенна (неоднородна) и представляет собой смесь кристаллов компонентов сплава, сохранивших свою структуру.
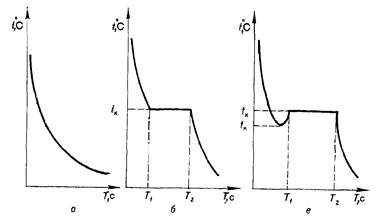
Рис. 7. Кривые охлаждения аморфного (а), кристаллического тела (б) и металлов (в), где /„ fn— температура кристаллизации и переохлаждения, "С; (Ti—Та) —время кристаллизации, с.
Строение кристаллического тела обусловливает следующие особенные их свойства по сравнению с аморфными:
различие свойств монокристаллов в различных направлениях, т. е. анизотропность, или векториальность, свойств;
наличие плоскостей скольжения, приложение внешних сил приводит к скольжению (сдвигу) одной плоскости относительно другой;
•существование критической температуры при затвердевании или плавлении, при которой происходит переход из жидкого (расплавленного) состояния в твердое или наоборот.
Переход металла из жидкого состояния в твердое называется кристаллизацией, а из твердого в жидкое — плавлением. Если образование кристаллов происходит из жидкости при ее охлаждении, то этот процесс называется первичной кристаллизацией, если образование кристаллов идет в твердом состоянии тела,—вторичной кристаллизацией.
Процессы кристаллизации графически изображают кривыми, строящимися в координатах температура — время (рис. 7).
Явление переохлаждения в кристаллизующемся металле объясняется тем, что в период затвердевания про-
исходит резкие снижение подвижности атомов, вследствие чего скачкообразно изменяется его внутренняя энергия. Это сопровождается выделением тепла, которое подогревает жидкую ванну и некоторое время (7'!— Тч) удерживает ее температуру постоянной, пока жидкость полностью не закристаллизуется.
Степень переохлаждения тем больше, чем больше скорость охлаждения.
Русский ученый-металлург Д. К. Чернов в 1878 г. установил, что процесс кристаллизации состоит из нескольких стадий. Первая стадия — образование зародышей (центров) кристаллизации. На последующих стадиях из этих центров образуются дендриты (древовидные образования), которые, срастаясь, образуют зерна (кристаллиты). При этом они не имеют правильной геометрической формы, так как в местах соприкосновения растущих кристаллов рост граней прекращается.
Величина зерна металла — важнейшая характеристика, которая определяет все основные его свойства. Мелкозернистый металл имеет более высокие характеристики твердости, прочности, ударной вязкости, но у него пониженная электропроводность, хуже магнитные свойства.
Размер зерна зависит от количества центров кристаллизации и скорости роста кристаллов (скорости охлаждения). Чем больше центров кристаллизации и меньше скорость их роста, тем меньше будет зерно.
Образование центров кристаллизации может происходить самопроизвольно или на имеющихся в жидком металле частицах примесей, что используется при модифицировании — введении в жидкий металл примесей (модификаторов).
На образование центров кристаллизации, а следовательно, и величину зерна влияет степень переохлаждения tv—i-n (см. рис. 7). Чем больше степень переохлаждения, тем больше центров кристаллизации и мельче образующееся зерно.
|
|
|
|
Дата добавления: 2014-01-11; Просмотров: 504; Нарушение авторских прав?; Мы поможем в написании вашей работы!