
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Диаграммы фазового равновесия (диаграммы состояния)
|
|
|
|
Химические соединения.
Химические соединения – фазы, которые имеют свою кристаллическую решетку, отличающуюся от решеток компонентов. Это определяет резкое отличие свойств соединений от свойств образующих его компонентов. Для химических соединений характерны высокая твёрдость, хрупкость, высокая температура плавления и др.
Валентные соединения имеют постоянный состав, соответствующий законам нормальной валентности. Это могут быть соединения между металлами (интерметаллиды), а также соединения металлов с неметаллами: MgS, Al2O3, Ni3Ti, и др.
Фазы внедрения образуют переходные металлы с неметаллами малого атомного радиуса (Rнм/Rм<0,59), например, карбиды и нитриды: Mo2C, TiC, Fe4N, VN и др.Фазы внедрения отличаются от твёрдых растворов внедрения более высокой концентрацией неметалла и простой кристаллической решёткой типа К8, К12, Г12. Фазы внедрения тугоплавки и обладают высокой твёрдостью. Их используют в легированных сталях и сплавах для упрочнения.
Электронные соединения – это химические соединения с определённой электронной концентрацией, т.е. отношением числа валентных электронов к числу атомов. Наиболее распространены соединения с электронной концентрацией 3/2: СuZn, CuBe; 7/4: CuSn3 и 21/13: Cu5Zn8 и др. Их используют как упрочняющие фазы в сплавах меди.
Фазовое состояние сплавов зависит от концентрации компонентов и температуры, при которой находится сплав. Для изучения фазового состояния сплавов пользуются диаграммами фазового равновесия (диаграммами состояния), которые строятся в координатах «температура–концентрация компонентов». Линии диаграммы показывают температуры фазовых превращений, области диаграммы – фазовый состав сплавов в условиях равновесия. Ниже рассмотрены основные типовые диаграммы состояния, характерные для металлических сплавов.
4.2.1. Диаграмма состояния сплавов с неограниченной растворимостью компонентов в твёрдом состоянии
На рис.4.1 показана диаграмма состояния сплавов с неограниченной растворимостью компонентов в твердом состоянии. Такой тип диаграммы соответствует сплавам Cu-Ni, Ag-Au и др. В таких сплавах при охлаждении происходит только одно фазовое превращение – кристаллизация.
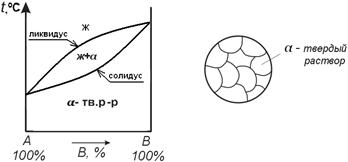
Рис.4.1. Диаграмма состояния сплавов с неограниченной растворимостью в твердом состоянии
Кристаллизация сплавов начинается при температурах tН, образующих линию ликвидус. Выше этой линии все сплавы находятся в жидком состоянии. Кристаллизация чистых компонентов А и В идет при постоянных температурах (tA и tB соответственно), тогда как кристаллизация твердых растворов – в интервале температур (tН-tК). Окончанию кристаллизации соответствуют температуры tК - линия солидус. Ниже этой линии все сплавы находятся в твердом состоянии, в виде α-твёрдого раствора. В области между линиями ликвидус и солидус находятся в равновесии две фазы: жидкий раствор и α-твердый раствор.
Диаграммы состояния позволяют определить структуру сплавов после завершения всех фазовых превращений при охлаждении. В данном случае структура любого сплава после охлаждения представляет собой зерна a-твердого раствора (рис. 4.1).
|
|
|
|
|
Дата добавления: 2014-01-11; Просмотров: 567; Нарушение авторских прав?; Мы поможем в написании вашей работы!