
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Форми автотрофної асиміляції
|
|
|
|
Послідовності реакцій у процесі дихання і їхній енергетичний вихід
| Послідовності реакцій | Вихідні сполуки | Кінцеві сполуки | Кількість утворених молекул АТР на молекулу глюкози |
| Гліколіз | Глюкоза (С6), NAD+, АДР, P | Піруват (С3), NAD-H + Н+ | 2 (8)* |
| Підготовка до ЦТК | Піруват (С3), (Со-А), NAD+ | СО2, Ацетил- СоА (С2), NAD-H +Н+ | (6)* |
| ЦТК | Ацетил- СоА (С2), NAD+, АDP, P, FAD | NAD-H +Н+, СО2, АТР, FАD-Н2 | (24)* |
| ЦПЕ | NAD-H +Н+, FАD-Н2, О2 | Н2О, АТР | (34)* |
* – у дужках показана кількість АТР, утвореної при дихальному метаболізмі
Таблиця 4.4
| Фотосинтез | Хемосинтез | ||
| Організми | Зелені рослини, синьо-зелені водорості | Зелені бактерії, пурпурні бактерії | Деякі (хемолітоавтотрофні) безбарвні бактерії |
| Джерело енергії | Світло | Світло | Окислення неорганічних речовин (H2S, NH3 та ін.) |
| Донори електронів | Н2О | Сполуки сірки (H2S, елементарна сірка та ін.) | Неорганічні речовини (H2S, Н2, NH3 та ін.) |
до менш окислених продуктів, таких як вуглеводи [(СН2О)n]. У зелених рослин і синьо-зелених водоростей джерелом необхідних для відновлення електронів служить вода (Н2О), що при відібранні електронів окисляється. Автотрофні бактерії не здатні до окиснювання води, їм потрібні інші донори електронів - S0, H2S, NH3, NO2-, Fe2+. Потребу в енергії задовольняє світло (фотосинтез, або окиснювання неорганічних сполук - хемосинтез).
4.4.1 Фотосинтез (загальний огляд)
Фотосинтез - це перетворення енергії світла в хімічну енергію. Таке перетворення відбувається в тілакоїдах. Хімічна енергія накопичується насамперед у формі АТР й [Н2] (водень, пов'язаний з коферментом).
Для облігатних автотрофів (зелені бактерії, пурпурні сіркобактерії, більшість синьо-зелених водоростей) фотосинтез - єдине джерело енергії. У зелених клітинах вищих рослин у цитоплазму переходять великі кількості АТР й [Н2]. Значна частина останнього (у формі NAD-H +H+) попадає в мітохондрії й там окислюється в ланцюзі дихання для додаткового синтезу АТР.
У вищих рослин більша частина АТР й [Н2] використовується для синтезу вуглеводів із СО2. Таким чином, фотосинтез включає перетворення енергії (світловий процес) у тілакоїдах хлоропластів і перетворення речовин (асиміляція вуглецю - темновий процес) у стромі хлоропластів:
| Світло 12Н2О ® 12 [Н2]+6О2 +Енергія АТР (світловий процес) (4.20) 6СО2 + 12 [Н2] + Енергія АТР ® С6Н12О6 + 6Н2О (темновій процес) (4.21) |
| Світло 6СО2 + 12Н2О ® C6H12O6 + 6H2О + 6О2; (DG0' = +2875 кДж/моль) (4.22) |
Відновник [Н2] (е- +Н+) утворюється при розщепленні води за рахунок енергії світла (фотоліз), при якому виділяється О2. АТР синтезується при проходженні електронів по ланцюзі транспорту електронів. Переносником водню служить NADP (нікотинамідаденіндинуклеотидфосфат), що у порівнянні з NAD містить на один фосфатний залишок більше. NADP-H ++H+ й АТР направляються в темновий процес, де водень й енергія використовуються для синтезу вуглеводів із СО2, а потім NADP+ й ADP знову використовуються у світловому процесі.
Інші органічні речовини (жирні кислоти або амінокислоти) можуть бути побічними продуктами фотосинтезу або ж удруге утворюватись з вуглеводів.
На кожні 6 молей поглиненого СО2 виділяється 6 молей О2. Коефіцієнт асиміляції AQ - відношення О2/СО2 - при біосинтезі вуглеводів дорівнює 1.
Для відновлення однієї молекули СО2 необхідно близько 9 квантів світла, так що на 1 моль СО2 повинне доводитися 9 молей квантів. Тому що 1 моль квантів червоного світла містить 172 кДж, витрата енергії дорівнює близько 9×172 кДж на 1 моль СО2, тобто 6×9×172 кД=9288 кДж на 1 моль С6Н12О6. Відповідно до наведеного вище рівнянню, із цієї кількості 2875 кДж зв'язується у формі хімічної енергії (у вуглеводи); залишок (близько 70%) - втрати.
4.4.2 Перетворення енергії у фотосинтезі (світловий процес)
Розраховуючи на 1 молекулу О2 (або 1 молекулу СО2) світловий процес можна представити так:
2Н2О + Світлова енергія ® О2 + 2[Н2] + Енергія АТР,
або докладніше:
Світло
2Н2О+ 2 NADP + + n (ADP + фосфат) ® О2 + 2(NADP-H + Н+) + nАТР (4.23)
Таким чином, світловий процес являє собою перенос водню (електронів і протонів) з однієї окислювально-відновної системи (Н2О/0,5·О2+2Н++ 2е–; Е¢0 =+0,81В) на іншу (NADP-H +/ NADP+ +2H++ 2e–; E0 = -0,32В). Однак перенос електронів від позитивного потенціалу до негативного - процес ендергонічний, він вимагає витрати енергії. Тільки для цього й потрібна при фотосинтезі енергія світла. Таким чином, первинна фотохімічна подія - це перенос електронів проти градієнта окислювально-відновного потенціалу (ОВП) за рахунок енергії світла.
Для цього переносу використовується ланцюг транспорту електронів. На більшості етапів електрони переміщаються тут "униз" за градієнтом ОВП без витрати енергії й без світла. І тільки два етапи здійснюються проти градієнта ОВП за рахунок світлової енергії; будучи фотохімічними реакціями.
Фотохімічну дію можуть робити тільки ті кванти світла, які поглинаються пігментами. Світло поглинають всі пігменти, але тільки фотосинтетично активні пігменти (хлорофіл а в рослин і синьо-зелених водоростей, бактеріохлорофіл у бактерій) виконують при цьому фотохімічну роботу (транспорт електронів). Додаткові пігменти (хлорофіл b, каротиноїди, фікобіліпротеїди) передають поглинену енергію активним пігментам без істотних втрат.
При поглинанні світлового кванта молекула пігменту збуджується, тобто на короткий час переходить у високоенергетичний, збуджений стан. При її поверненні у вихідний стан виділяється енергія, за рахунок якої може відбуватися різна робота. Хлорофіл може мати різні збуджені стани. При поверненні у вихідний стан енергія може виділятися у вигляді флуоресценції або тепла, передаватися як збудлива енергія іншим молекулам або використовуватися для фотохімічної роботи.
У тілакоїдних мембранах молекули пігментів розташовані разом з білками й іншими компонентами у двох різних комплексах - фотосистемі І і фотосистемі ІІ (ФС І і ФС ІІ) (рис. 4.11). Кожна фотосистема містить, по-перше, 1 молекулу "пігменту реакційного центра" (ПРЦ, хлорофіл а), що після поглинання світла (збудження) виконує фотохімічну роботу (перенос електронів), і, по-друге, безліч молекул "пігментів-антен" або "колекторів" (хлорофіли а й b, каротиноїди), що передають поглинену енергію ПРЦ і збуджують його.
Кожна частка ФС І і ФС ІІ містить 200-400 молекул хлорофілу. ФС І має в якості ПРЦ пігмент 700 (хлорофіл а1): дві молекули хлорофілу, які завдяки взаємодії диполь-диполь збуджуються легше, ніж хлорофіл-мономер. ПРЦ у ФС ІІ являє собою пігмент 680 (хлорофіл а2). ФС ІІ містить особливо багато хлорофілу b. Фотохімічна робота пігменту реакційного центра здійснюється в такий спосіб: збуджена молекула пігменту (Хл) віддає валентний електрон акцептору електронів з негативним окислювально-відновним потенціалом (ОВП); пігментний катіон (Хл+), що утворюється при цьому, віднімає електрон від

Рис. 4.11. Фотопереніс електронів. Лінійний і циклічний ланцюги транспорту електронів
донора електронів з позитивним ОВП. Таким чином, електрони переходять із більш низького енергетичного рівня на більш високий проти градієнта ОВП: ФС І переводить електрони з Е'0 + 0,4 В на Е'0 - 0,4 В (фотореакція І), а ФС ІІ - з Е'0 +0,8 В на Е'0 -0,15 В (фотореакція ІІ).
Ланцюг транспорту електронів іде від Н2О (Е'0 =+0,81 В) через обидві фотосистеми до NADP (Е'0 = - 0,32 В). У фотореакції ІІ (у ФС ІІ) і фотореакції І (у ФС І) електрони послідовно два рази піднімаються "у гору", щораз за рахунок енергії одного кванта світла (ендергонічні процеси); на проміжному етапі вони спускаються "під гору" (екзергонічний процес), при цьому утворюється АТР. Цей шлях називається лінійним (нециклічним) фотопереносом електронів або Z -фотосинтезом.
Донор електронів Н2О віддає електрони переноснику електронів Z (Mn -протеїду), від якого вони через пігмент 680 переходять до акцептора електронів у ФС ІІ - "гасителеві" Q невідомої хімічної природи (фотореакція ІІ). Наступний переносник електронів пластохінон (Pq) у хімічному й функціональному відношенні подібний з убіхіноном й, так само як й останній, розчинений у ліпідній фазі мембрани. Далі йде цитохром b559 - залізопорфірин, як і всі цитохроми; він є ще компонентом часток ФС ІІ, тоді як пластоціанин (Рс - Сu -протеїд, що переносить електрони) перебуває в електронотранспортних частках тілакоїдної мембрани. Від Рс електрони через пігмент 700 передаються ще акцептору електронів у ФС І - речовині X (фотореакція І) - і далі ферредоксину (Fd - білку, що містить залізо й сірку) і здобувають досить високу енергію, тому що Fd має надзвичайно низький окислювально-відновний потенціал (Е'0 = -0,43 В). Флавопротеїд (Fp) з FAD як кофермент здійснює потім перенос електронів на NADP.
При лінійному фотопереносі електронів використовуються кванти світла й Н2О. У результаті відриву електронів під дією світла (фотоокислювання) відповідні молекули води розпадаються (фотоліз води), утворюючи протони й О2. Цей кисень, що звільняється при фотосинтезі, походить із Н2О, а не із СО2.
Лінійний фотопереніс електронів поставляє два продукти: АТР й NADP-H + H+. Звільнення протонів при фотолізі Н2О урівноважується використанням їх при утворенні NADP-H + H+.
Циклічний фотопереніс електронів. Фотосистема І може бути скорочена. Тоді виникає круговий струм електронів при участі цитохрому b6, що разом із цитохромом f (і Рс) є присутнім в електроннотранспортних частках тілакоїдних мембран. Електрони перекачуються "у гору" за допомогою одиночних квантів світла, а при їх зворотному "спуску" утворюється АТР. Циклічний фотопереніс електронів не включає фотолізу Н2О и не служить джерелом NADP-H. Тут тільки один продукт - АТР. Синтез АТР у цьому випадку називають циклічним фотофосфорилюванням на відміну від нециклічного при лінійному фотопереносі електронів. Циклічний ланцюг є у всіх ділянках тілакоїдів - і в гранах, і між гранами, а фотосистема ІІ й, отже, лінійний ланцюг, - імовірно, тільки в гранах.
4.4.3 Перетворення речовин при фотосинтезі (темновой процес)
У темновому процесі при використанні продуктів світлового процесу (NADP-H й АТР) із СО2 синтезується вуглевод (рис. 4.12). Розраховуючи на 1 молекулу СО2 (або О2)
СО2 + 2[Н2] + Енергія АТР ® (СН2О) + Н2О,
Або докладніше:
СО2 + 2(NADP-Н + Н+) + 3 АТР ® (СН2О) + 2 NADP + + Н2О +3(ADP +фосфат) (4.24)
де (СН2О) – означає 1/6 молекули глюкози.
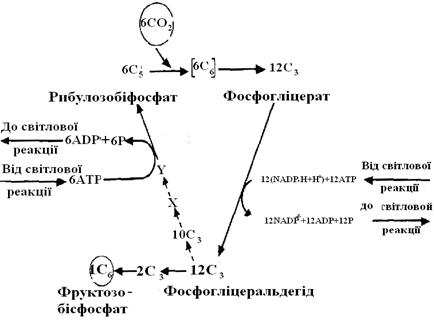
Головний шлях асиміляції СО2 - цикл Кальвіна - циклічний процес, у який уводиться СO2 і з якого виходить вуглевод (рис. 4.12, А). Процес можна розділити на три фази.
| |
| А | |
| |
| Б | |
| |
| В | Г |
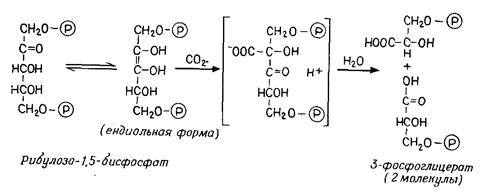
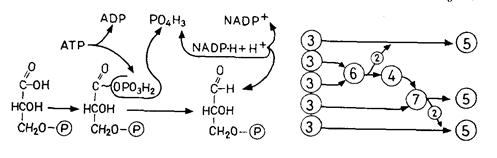
Рис. 4.12. Цикл Кальвіна. А. Сумарна схема. Угорі - фаза карбоксилювання; праворуч - фаза відновлення; ліворуч - фаза регенерації. Б. Фаза карбоксилювання; нестабільний проміжний продукт (С6) піддається гідролізу. В. Фаза відновлення (з 1,3-дифосфогліцератом як проміжним продуктом, порівн. рис. 4.4, В). М. Фаза регенерації. Більші кружки - проміжні продукти; маленькі кружки - фрагменти молекул, що переносяться; цифрами в кружках зазначене число атомів
Фаза карбоксилювання (рис. 4.12, Б). СО2, зв'язуючись із рибулозобіфосфатом (фосфатом цукру з п'ятьма атомами С), утворює дві молекули фосфогліцерата (по 3 атоми С - С3). Цю реакцію каталізує рибулозобіфосфаткарбоксилаза.
Фаза відновлення. Фосфогліцерат при участі NADP-H (відновник) і АТР (донор енергії) відновлюється до 3-фосфогліцеральдегіда. Ця послідовність реакцій (рис. 4.12, В) являє собою обіг окисних етапів гліколізу.
Фаза регенерації. Кожна шоста молекула фосфогліцеральдегіда виходить із циклу (рис. 4.12, Г), і із цієї речовини утворюється фруктозо-1,6-біфосфат (С6); з останнього у свою чергу синтезуються глюкоза, сахароза, крохмаль і т.д. З інших молекул фосфогліцеральдегіда (С3) при участі нових молекул АТР регенерується рибулозобіфосфат (5С3®С5); як проміжні продукти утворюються різні фосфати цукрів наприклад, С4 - еритрозо-, С6 - фруктозо-, С7 - седогептулозофосфат.
4.4.4 Хемосинтез
Крім фотосинтезу існує ще одна форма автотрофної асиміляції - хемосинтез, властивий деяким бактеріям). На відміну від фотосинтезу джерелом енергії тут служить не світло, а окислювання неорганічних речовин. Хемосинтез, як і фотосинтез, включає перетворення енергії й речовини. При перетворенні речовин із СО2 утворюються (в основному таким же шляхом, як при фотосинтезі) органічні асиміляти, зокрема вуглеводи. Необхідні для цього продукти перетворення енергії ті ж, що й при фотосинтезі: використовуваний для відновлення водень (у формі NADP-H) і енергія (у формі АТР). Вони утворюються в результаті окислювання неорганічних речовин, наприклад H2S.
Частина електронів, віднятих у неорганічних речовин (окислювання), переноситься на NAD (наприклад, H2S + NAD+ ®S + NAD-H + H+) і використовується при перетворенні речовин для відновлення. Інша частина через ланцюг транспорту електронів направляється до кисню й доставляє енергію для синтезу АТР подібно тому, як це відбувається в ланцюзі дихання.
Неорганічні речовини, що окислюються, видоспецифічні. Відомі наступні окисні процеси, у результаті яких утворюється АТР:
Сірчані бактерії S2- + 2H+ + 0,5O2 →S0 + H2О або
S2- +2O2 →SO42
Нітрифікуючі
(амонійокислюючі) бактерії 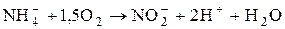
Нітрифікуючі
(нітритокислюючі) бактерії 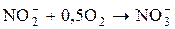
Водневі бактерії Н2 +0,5 О2 → Н2О
Метанутворюючі бактерії СО2 + Н2 → СН4 + Н2О
Бактерії, що використовують
окис вуглецю СО + 0,5·О2 → СО2
Залізобактерії (ацидофільні) 2FeCО3+О2+3H2О→2Fe(OH)3 + CО2
Такі субстрати, як NО2–, CO, Fe2+, звичайно, не можуть поставляти водень для відновлення NAD, але вони служать джерелами електронів, тоді як протони виходять при дисоціації Н2О. Продукти окислювання майже завжди виділяються в зовнішнє середовище.
Багато хто з хемосинтезуючих бактерій мають народногосподарське значення: нітрифікуючі бактерії беруть участь в очищенні стічних вод, затримують у ґрунті азот аміаку, що виділяється при гнитті; сірчані бактерії й ацидофільні залізобактерії є збудниками найбільш активної мікробіологічної корозії будівельних конструктивів.
4.4.5 Гетеротрофна асиміляція
Гетеротрофні клітини повинні споживати як їжу органічні речовини. Гетеротрофна асиміляція зводиться в основному до процесів перебудови молекул. Наприклад, спожиті білки розщеплюються до амінокислот, з яких знову синтезуються білки, властиві даному організму. Необхідну для цього енергію доставляють процеси дисиміляції. При високій здатності до перебудови речовин (різноманітті шляхів метаболізму, як, наприклад, у багатьох цвілевих грибів) організму досить однієї єдиної органічної речовини, щоб синтезувати всі необхідні сполуки. При цьому представники різних класів речовин перетворюються один в одного: амінокислоти у вуглеводи, вуглеводи в жири й т.д.. На відміну від цього більшість інших організмів через обмежену здатність до синтезу повинне одержувати зовсім певні (так називані незамінні) органічні речовини, наприклад амінокислоти (рис. 4.13).
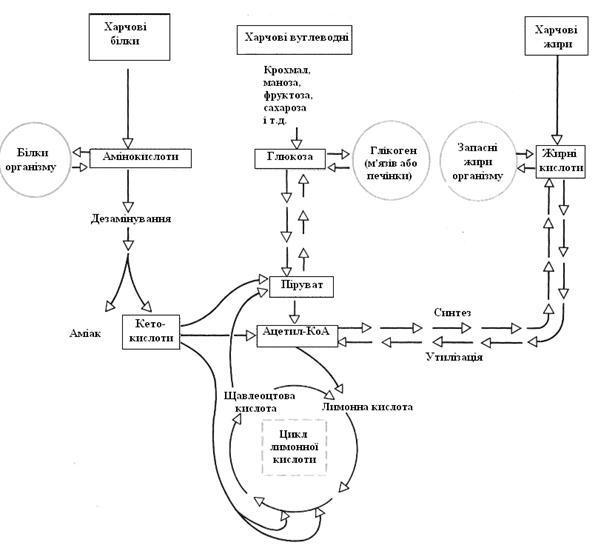
Рис. 4.13. Шляхи перетворення (розщеплення або запасання) білків, жирів і вуглеводів, споживаних організмом
4.5 Обмін жирів і білків
Жири - відмінні субстрати для дихання. Вони гідролізуються до гліцерину й жирних кислот. Гліцерин (НОСН2СНОН-СН2ОН) перетворюється в дигідроксиацетонфосфат (НОСН2СО-СН2-О-РО3Н2), що використовується у процесі гліколізу. Жирні кислоти в процесі окислювання поступово розщеплюються до ацетильних залишків (С18®9С2, С16®8С2), які у формі ацетил- СоА надходять у цикл лимонної кислоти:
С17Н38СООН + 9CoA-SH + 7Н2О ® 9CoА-S ~CO-CH3 + 16[Н2] (4.25)
Біосинтез жирних кислот починається з ацетил- СоА (але йде не тими шляхами, за якими вони розщеплюються), а біосинтез гліцерину - з дигідроксиацетонфосфата.
Білки розщеплюються протеазами. Вивільнювані амінокислоти у випадку, якщо вони не використаються для синтезу нових білків, різними шляхами розпадаються й зрештою перетворюються в піруват, ацетил- СоА й проміжні продукти циклу лимонної кислоти (a-кетоглутарат, сукцинат, фумарат, малат, оксалоацетат). Продукти розщеплення амінокислот можуть також використатися для синтезу вуглеводів (глюконеогенезу) або виділятися в органічній формі. Мікроорганізми й рослини здатні синтезувати всі 20 амінокислот. Аміногрупи утворюються з поглиненого азоту, найчастіше неорганічного.
4.6 Регуляція активності ферментів
Різноманітні шляхи й реакції обміну речовин повинні бути скоординовані між собою. Це впорядковане протікання метаболічних процесів досягається шляхом регуляції. Сюди відноситься й пристосування метаболізму до умов зовнішнього середовища. Ферменти як каталізатори обмінних реакцій грають у цьому регулюванні ключову роль. Існують наступні види внутрішньоклітинної регуляції:
1) регуляція метаболітами, пов'язана зі змінами концентрацій метаболітів (проміжних продуктів обміну) без зміни кількості ферментів й їхньої активності;
2) ферментна регуляція, пов'язана зі змінами активності ферментів без зміни їхніх кількостей, - регулюючі фактори впливають на ферментні молекули;
3) генна регуляція, пов'язана зі зміною кількості ферментів, - регулюючі фактори впливають на біосинтез або руйнування ферментів.
Ферментна й генна регуляція використається не для всіх ферментів; вона найбільш ефективна для тих з них, які лімітують швидкість певних процесів або діють біля місць розгалуження метаболічних шляхів.
Ферменти, що лімітують швидкість, діють на самому повільному етапі того або іншого шляху й тому обмежують швидкість усього процесу. Наприклад, швидкість гліколізу лімітує фосфофруктокіназа - фермент, що перетворює фруктозо-6-фосфат (шляхом його фосфорилювання) у фруктозо-1,6-бісфосфат.
Особливо важливі ферменти контролюються звичайно декількома різними механізмами. Регуляція обміну речовин спрямована на його раціоналізацію, вона створює селективні переваги в еволюції.
4.6.1 Внутрішньоклітинна ферментна регуляція
Неактивні білки, з яких у результаті ферментативного відщіплення частини молекули (процесінга білків-попередників) утворюється функціонуючий білок, називаються про протеїнами. При процесінгу білка-попередника фермент активується за допомогою другого ферменту, що грає роль регулятора. У деяких ферментів активність змінюється при хімічній модифікації, наприклад, ковалентному оборотному приєднанні фосфату. При регуляції такого типу активність одного ферменту (конвертованого) змінюється під дією іншого (конвертуючого). Завдяки тому, що одна молекула конвертуючого ферменту може модифікувати багато молекул першого, досягається ефект посилення.
Відомі й інші хімічні модифікації: оборотне приєднання AMP, аденозиндифосфорибози, приєднання залишку жирної кислоти й ін.
Модуляція - це оборотна зміна ферментативної активності в результаті нековалентних взаємодій з невеликими молекулами - так називаними ефекторами, більшість із яких являють собою проміжні метаболіти. Ізостеричні ефектор в хімічному відношенні подібні із субстратом і тому зв'язуються каталітичним центром ферменту й блокують його, тому що не піддаються ферментативному перетворенню (ізостерична модуляція) (рис. 4.14, А). Субстрат й ефектор конкурують за молекулу ферменту залежно від їхньої концентрації; у цьому випадку говорять про конкурентне гальмування, а ізостеричні ефектори називають конкурентними інгібіторами.
Гальмування продуктом реакції являє собою рід зворотного зв'язку, коли продукт ферментативної реакції діє як негативний ефектор (інгібітор) безпосередньо на фермент. Це веде до раціоналізації обміну речовин: якщо кількість якоїсь речовини надмірно зростає (у результаті його синтезу або поглинання), те його подальший синтез блокується.
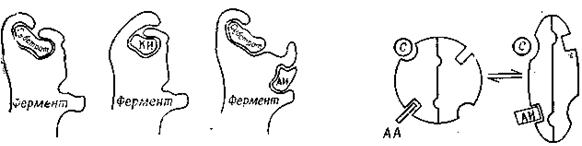
| |
| А | Б |
Рис. 4.14. Модуляція ферментів (модельні подання). А. Активний, ізостерично інгібований й алостерично інгібований фермент. Б. Алостерична модуляція за Моно. КИ - конкурентний інгібітор; АИ - алостеричний інгібітор; АА - алостеричний активатор; С - субстрат
Алостерична модуляція заснована на зміні конформації ферменту, що веде до зміни його активності. Таку модуляцію викликають алостеричні ефектори. Алостеричні ферменти - це білки з декількох субодиниць (протомерів), що мають поза своїм каталітичним центром додаткову ділянку, так званий регуляторний (алостеричний) центр. Алостеричні ефектори не подібні із субстратом. Вони зв'язуються регуляторним центром й у такий спосіб викликають зміну конформації алостеричного ферменту і його каталітичного центра. Відповідно до гіпотези, обоє конформаційних стани ферменту перебувають у рівновазі, але під дією позитивних ефекторів (активаторів) фіксується більше активний стан, а під дією негативних (інгібіторів) - менш активний.
Запитання для самоперевірки
1. Які класи ферментів відомі?
2. Чим відрізняються біологічні каталізатори від хімічних?
3. Як відбувається полегшена дифузія речовин через клітинну мембрану?
4. Як відбувається активний транспорт через клітинну мембрану?
5. Чим процес горіння відрізняється від процесу біологічного окислення органічних речовин?
6. Які етапи можна виділити в процесі окислення глюкози при диханні?
7. Що являє собою гліколіз?
8. Як функціонує ланцюг дихання?
9. Які види автотрофної асиміляції відомі і хто їх здійснює?
10. Які особливості процесів в фотосистемі І і в фотосистемі ІІ?
11. Як відбувається синтез органічної речовини при фотосинтезі?
12. Які особливості має гетеротрофна асиміляція?
|
|
|
|
|
Дата добавления: 2014-01-11; Просмотров: 593; Нарушение авторских прав?; Мы поможем в написании вашей работы!