
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Предотвращение образования минеральных отложений. Продувка. Подкисление. Фосфатирование
|
|
|
|
Образование и характер отложений
В оборотной системе охлаждения вследствие упаривания некоторой части воды происходит повышение ее солесодержания. Кроме того, процесс охлаждения воды в градирнях сопровождается десорбцией СО2, приводящей к повышению рН, частичной диссоциации ионов НСО-3 и обогащению воды ионами СОз. При соответствующей концентрации ионов Са2+ в охлаждающей воде создаются условия для образования отложений по тракту охлаждающей воды в форме СаСО3, т. е. вода становится нестабильной по содержанию карбоната кальция.
Для образования СаСО3 необходимо некоторое пересыщение раствора. Однако в процессе образования твердой фазы СаСО3 оказывают ингибирующее действие присутствующие в воде органические вещества. Поэтому условия осаждения СаСО3 в охлаждающих системах в каждом конкретном случае определяют экспериментально. Из сказанного выше следует, что основным мероприятием для предотвращения образования отложения СаСО3 является стабилизация воды.
Наиболее распространенным методом стабилизации охлаждающей воды является продувка систем водяного охлаждения, т. е. отвод части оборотной воды с заменой ее свежей. При продувке происходит общее понижение концентрации всех примесей, в том числе хлоридов и сульфатов, что, в частности, способствует ослаблению процессов коррозии в оборотной системе охлаждения. Вывод солей из оборотной системы осуществляется за счет организованной продувки и потерь при капельном уносе из градирни. Унос солей в результате испарения воды ничтожен и во внимание не принимается. Так как основным назначением продувки является поддержание карбонатной жесткости оборотной воды ниже предельно допустимой Жкп„, значение этой продувки можно определить из уравнения баланса
Жк.п р (рун +Рпрод) = Жк доб (рисп +рун +рпроа), (1)
откуда
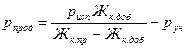 (2)
(2)
где Жк.доб—карбонатная жесткость добавляемой воды, мг-экв/кг; рисп, рун, р прод—потери воды, оборачиваемой в цикле охлаждения за счет испарения, уноса и продувки, %.
Потери воды на испарение, %, определяются из выражения
рисп = 0,16х∆t, (3)
где х —доля теплоты, отдаваемой охлаждающей водой за счет ее испарения в градирне (летом 1,0, зимой 0,5, весной и осенью 0,75); ∆t — снижение температуры воды в градирне.
Потери воды в результате уноса составляют 0,25—3,5% объема оборотной воды и зависят от наличия и эффективности работы брызгоуловителей в градирнях.
Продувка является простейшим противонакипным мероприятием, однако она целесообразна лишь в случае, когда затраты на перекачку воды и оборудование для продувки не превышают затрат на другие способы коррекции оборотной воды
Обычно стабилизация охлаждающей воды совмещает комплекс мероприятий, включающих как продувку, так и обработку воды химическими реагентами. К химическим методам обработки охлаждающей воды относятся подкисление, рекарбонизация, фосфатирование.
Подкисление воды проводится с целью частичного снижения карбонатной жесткости воды до значения, равного или несколько ниже Жкпр. Для этого используется серная кислота как наиболее дешевый и доступный реагент.
|
|
|
|
Дата добавления: 2014-01-13; Просмотров: 1302; Нарушение авторских прав?; Мы поможем в написании вашей работы!