
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Общий тепловой эффект неполной реакции
|
|
|
|
Лекция 5
Запишем выражение для суммарного теплового эффекта полной реакции:
 (22)
(22)

Тепловой эффект, выраженный через теплоемкость, запишется:
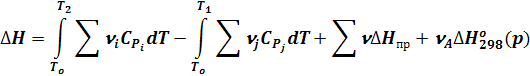 (23)
(23)
Эти уравнения подходят для случая, когда в исходном состоянии имеется смесь только реагентов, а в конечном - только продуктов.
Обычно реакция не завершается полностью, а достигает состояния химического равновесия, и мы имеем равновесную смесь реагентов и продуктов реакции.
Кривая зависимости энтальпии от температуры для равновесной смеси проходит выше кривой зависимости для продуктов реакции, так как тепловой эффект незавершенной реакции DН2 меньше, чем тепловой эффект завершенной реакции DН1.
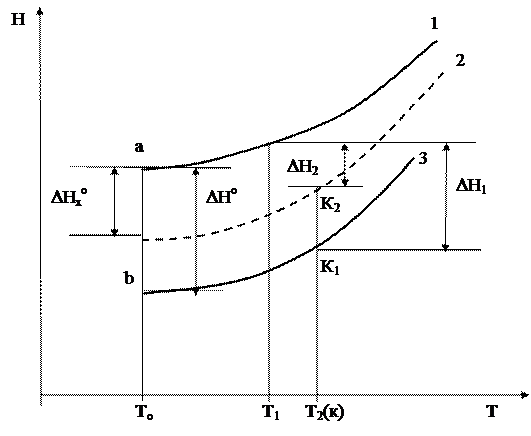
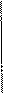 1- исходные вещества
1- исходные вещества
2- незавершенная реакция (суммарная энтальпия продуктов реакции, т.к. реакция неполная)
3- продукты
Степень завершения реакции определяется величиной константы равновесия и, следовательно, зависит от температуры. Связь между мерой реакции, степенью превращения, степенью диссоциации и константой равновесия дается уравнениями (11), (14), (15).
Заменяя в уравнении (23) n на число моль реагентов и продуктов n и N и учитывая степень превращения Х можно записать:
 (24)
(24)
Х - степень превращения вещества А, к которой отнесен тепловой эффект реакции DНо298.
Если вещества вступают в реакцию в стехиометрическом соотношении, то N равны n, а если степень превращения равна единице Х = 1, то уравнение (24) превращается в уравнение (22).
Тепловой эффект незавершенной реакции можно выразить следующим образом:
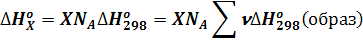
или

Для определения теплового эффекта по уравнению (24) при заданных начальной и конечной температурах Т1 и Т2 необходимо знать состав равновесной смеси - число моль ni и степень превращения Х.
Однако, число моль ni можно выразить через степень превращения Х по уравнению (12). В свою очередь, степень превращения Х определяет константу равновесия по уравнению (14).
Таким образом, если известна конечная температура равновесной смеси, то по значению константы равновесия для этой температуры, используя уравнения (12) и (14) определяют соответственно степень превращения и состав равновесной смеси, а по уравнению (24) общий тепловой эффект, т.е. количество теплоты, которой обменивается система.
Адиабатная реакция
В общем случае, когда условия отличаются от изотермических, определению подлежат состав равновесной смеси и ее температура.
Для определения степени превращения и температуры необходимо решить два уравнения с двумя неизвестными. Одно из этих уравнений f1(X, T) = 0 получается из уравнения (24), которое для адиабатического случая имеет вид:

Второе уравнение f2(X, T) = 0 можно составить, выражая константу равновесия через степень превращения по уравнению (14) и используя зависимость константы равновесия от температуры (DG = -RTlnKP).
 Решение системы уравнений
Решение системы уравнений
f1(X, T) = 0
f2(X, T) = 0
обеспечивает определение температуры равновесной смеси и степени превращения и, следовательно, состава равновесной смеси.
Равновесная температура сгорания
Теоретическая адиабатическая температура сгорания фактически не достигается, так как реакция сгорания никогда не завершается полностью, часть продуктов диссоциирует. Проблема определения температуры усложняется. В результате реакции мы имеем смесь продуктов полного сгорания и продуктов диссоциации. Состав равновесной смеси зависит от степени диссоциации продуктов.
В этом случае существует два способа определения состава равновесной смеси и температуры:
1. по степени диссоциации всех продуктов диссоциации,
2. по закону сохранения массы элементов.
|
|
|
|
|
Дата добавления: 2014-01-13; Просмотров: 314; Нарушение авторских прав?; Мы поможем в написании вашей работы!