
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Азотосодержащие пятичленные гетероциклы
|
|
|
|
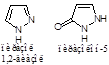
Antipyrinum (Антипирин)
1-Фенил-2, 3-диметилпиразолон-5.
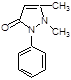
Получение: Синтез антипирина был осуществлен впервые Кнорром в 1883 г. Сырьём служат: фенилгидразин и ацетоуксусный эфир (реакция Кляйзена).

Реакцию ведут в нейтральной среде, т.к. в кислой фенилгидразин вступает в рекацию в другой таутомерной форме, в результате чего при циклизации получается побочный продукт снижающий выход и качество основного продукта – антипирина. Щелочная среда также непригодна, т.к. в этом случае образуется сильное осмоление. Полученный фенилметилпиразолон метилируют, затем обрабатывают щёлочью и выделяют свободный антипирин:
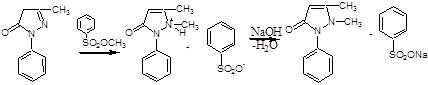
Описание: Бесцветные кристаллы или белый кристаллический порошок без запаха, слабогорького вкуса. Температура плавления = 110 – 113°С.
Растворимость: Очень легко растворим в воде (1:1), легко - в спирте, хлороформе, трудно растворим в эфире.
Подлинность:
1. Нитрозирование – образование нитрозоантипирина (изумрудно-зелёного цвета):
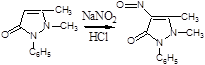
2. С FeCl3 – интенсивно красное окрашивание (у Татьяны Юрьевны в лекциях – коричневое), обусловленное образованием комплексной соли феррипирина: 3C11H12ON2•2FeCl3.
Нефармакопейная:
1. (В ГФ10 нет, но в лекциях отнесена к фармакопейным) Образование фиолетово-красного пиразолонового красителя (в отличие от амидопирина). Для этой цели сначала нитрозируем антипирин в присутствии уксусной кислоты (см. реакцию выше, вместо HCl тут будет уксусная кислота). Избыток HNO2 разрушают азидом натрия, после чего вводят α-нафтиламин – образуется азокраситель:
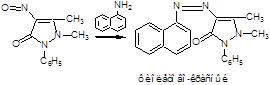
реакция является специфичной для антипирина!
2. Обрабатываем разбавленный раствор антипирина конц. раствором 2-нитроиндандиона в результате образуется оранжевая окраска, исчезающая при добавлении аммиака. Эта реакция специфична для антипирина.
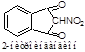
Чистота:
1. Температура плавления = 110 – 113°С.
2. Прозрачность и цветность.
3. Общие допустимые примеси: хлориды, сульфатная зола, органические примеси.
4. Специфические недопустимые: бензосульфонат натрия – раствор в 10 мл дихлорэтана должен быть бесцветным и прозрачным.
Количественное определение:
Используют обратную йодометрию в слабокислой среде:
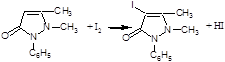
I2 + 2Na2S2O3 à 2NaI + Na2S4O6
HI + CH3COONa -> NaI + СН3СООН
Реакцию ведут в присутствии ацетата натрия, чтобы связать выделяющийся HI и предотвратить обратимость процесса. Образующийся в процессе реакции йодопирин может адсорбировать на своей поверхности некоторое количество йода, поэтому добавляют спирт или хлороформ, которые растворяют образующийся йодопирин.
Нефармакопейные:
1. Броматометрия в кислой среде:
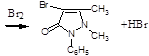
2. Йодхлорметрия:
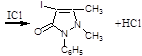
Хранение: список Б. В хорошо укупоренной таре, предохраняющей от действия света.
Применение: Как и другие производные пиразолона, антипирин оказывает болеутоляющее, жаропонижающее и в той или иной степени противовоспалительное действие. По анальгезирующей и жаропонижающей активности препараты этой группы близки к производным салициловой кислоты. Производные пиразолона уменьшают проницаемость капилляров и препятствуют развитию воспалительной реакции.
Форма выпуска: порошок и таблетки по 0,25 г.
Amidopyrinum (Амидопирин)
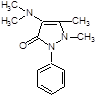
1 -Фенил-2, 3-диметил-4-диметиламино-пиразолон-5.
Получение:
Сначала получают нитрозопирин (по реакциям получения антипирина), затем его восстанавливают и получают аминопирин, который метилируют и получают амидопирин:
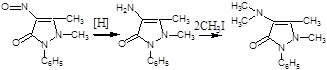
Описание: Белые кристаллы или белый кристаллический порошок без запаха, слабогорького вкуса.
Растворимость: Медленно растворим в воде (1:20), растворим в спирте, очень легко растворим в хлороформе.
Подлинность:
1. + FeCl3 à сине-фиолетовое окрашивание, не исчезающее от добавления минеральной кислоты (отличие от анальгина).
2. + AgNO3 à вначале появляется сине-фиолетовое окрашивание, затем выпадает серый осадок восстановленного серебра.
3. При прибавлении K3Fe(CN)6 в кислой среде, а затем FeCl3 – синее окрашивание вследствие образования берлинской лазури:
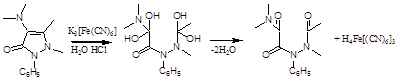
H4Fe[(CN)6]3 + 4FeCl3 à Fe4[Fe(CN)6]3 + 12HCl
Чистота:
1. Температура плавления.
2. Прозрачность и цветность.
3. Общая недопустимая примесь: хлориды.
4. Общая допустимая примесь: сульфатная зола и тяжелые металлы.
Специфическая допустимая в пределах эталона – аминоантипирин, который можно обнаружить по помутнению водного раствора препарата при добавлении раствора бензальдегида:
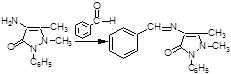
Количественное определение:
ГФ10 рекомендует метод кислотно-основного титрования в неводных средах. Амидопирин как слабое основание титруется в ледяной уксусной кислоте хлорной кислотой:
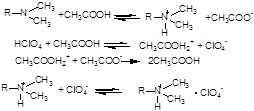
Индикатор тропеолин-ОО в точке эквивалентности наблюдается ярко-фиолетовое окрашивание. Параллельно проводим контрольный опыт. f=1/2.
Хранение: список Б. В защищенном от света месте.
Применение: Оказывает жаропонижающее, болеутоляющее и противовоспалительное действие. По фармакологическим свойствам амидопирин близок к антипирину, но активнее его. Применяют при головной боли, невралгиях, артритах, миозитах, хорее, иногда при остром суставном ревматизме.
Форма выпуска: порошок; таблетки по 0,25 г и таблетки, содержащие амидопирина 0,25 г и кофеин-бензоата натрия 0,1 г.
Analginum (Анальгин)
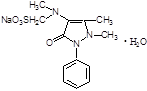
1-Фенил-2, 3-диметил-4-метиламинопиразолон-5-N-метансульфонат натрия.
Получение:
Аминоантипирин обрабатывают бензальдегидом. Полученный бензилиденаминоантипирин метилируют диметилсульфатом, в результате получают монометиламиноантипирин. При обработке монометиламиноантипирина смесью водных растворов формальдегида и бисульфита натрия получается анальгин:
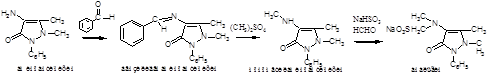
Описание: Белый или белый с едва заметным желтоватым оттенком крупноигольчатый, кристаллический порошок без запаха. В присутствии влаги быстро разлагается. Водные растворы при стоянии желтеют.
Растворимость: Легко растворим в воде (1: 1,5), трудно - в спирте, нерастворим в эфире, хлороформе и ацетоне.
Подлинность:
1. Реакция на Na+.
2. При нагревании с минеральными кислотами анальгин выделяет сернистый газ и формальдегид, определяют по запаху:
R-N(CH3)CH2SO3Na + HCl 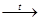 R-NH-CH3 + SO2↑ + HCHO↑ + NaCl
R-NH-CH3 + SO2↑ + HCHO↑ + NaCl
При добавление к подкисленному раствору препарата в спиртовой среде йодата калия наблюдается малиновое окрашивание (промежуточные продукты окисления). При дальнейшем добавлении реактива окраска усиливается и выделяется бурый осадок (I2):
5SO2 + 2KIO3 à I2 + K2SO4 + 4SO3
Чистота:
1. Прозрачность раствора.
2. Кислотность и щёлочность.
3. Потеря в массе при высушивании.
4. Общие допустимые примеси: тяжелые металлы, As.
5. Специфическая недопустимая: аминоантипирин (см. выше).
Количественное определение:
Методом прямой йодометрии в слабокислой среде:

NaHSO3 + I2 à NaHSO4 + 2HI
КТТ: избыток I2 – жёлтое окрашивание.
f=1/2 (это точно!)
Хранение: анальгин и содержащие его комбинированные препараты хранят по списку Б. В хорошо укупоренных банках оранжевого стекла в защищенном от света месте.
Применение: Применяют анальгин при болях различного происхождения (головная боль, невралгия, радикулиты, миозиты), лихорадочных состояниях, гриппе, ревматизме, хорее.
Форма выпуска: порошок, таблетки по 0,5 г; 25 % и 50 % растворы в ампулах по 1 и 2 мл.
Butadionum (Бутадион)
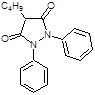
1,2-Дифенил-4- бутилпиразолидиндион- 3, 5.
Получение:
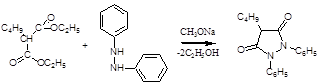
Описание: Белый или белый со слегка желтоватым оттенком порошок.
Растворимость: Практически нерастворим в воде, трудно растворим в спирте; легко растворим в хлороформе, эфире, растворе едкого натра.
Подлинность:
1. Осаждение аниона тяжелыми металлами:
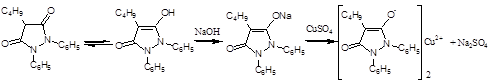
С Сu2+ - осадок сероватого цвета переходящий в голубой.
2. При действии нитрита натрия в конц. серной кислоте появляется оранжевое окрашивание переходящее в вишневое одновременно наблюдается выделение пузырьков газа.
3. ТСХ.
Чистота:
1. Температура плавления.
2. Общие допустимые примеси: хлориды, сульфаты, сульфатная зола и тяжелые металлы.
3. Недопустимая специфическая примесь – гидразобензол. Его можно обнаружить действием 10% раствора FeCl3 в присутствии конц. H2SO4 à вишнёво-красное окрашивание.
Количественное определение:
Прямая алкалиметрия (навеску растворяем в ацетоне):

Хранение: список Б. В хорошо укупоренной таре, предохраняющей от действия света.
Применение: Применяют для лечения ревматизма в острой форме, острых, подострых и хронических ревматоидных полиартритов, инфекционных неспецифических полиартритов, болезни Бехтерева, подагры, псориатических артритов, узловатой эритемы, малой хореи.
Форма выпуска: таблетки по 0,15 г.
|
|
|
|
|
Дата добавления: 2014-01-13; Просмотров: 1461; Нарушение авторских прав?; Мы поможем в написании вашей работы!