
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Управление свойствами и размерами покрытий
|
|
|
|
Назначение металлических покрытий металлами и сплавами
Электрохимические металлические покрытия широко используются с целью:
- получения на поверхности металла слоев, имеющих специальные функциональные свойства (например, повышение износостойкости для трущихся поверхностей);
- получение декоративных покрытий;
- в ремонтном производстве (восстановление деталей машин);
- защиты от коррозии;
- получения металлических порошков;
- применения в электронике и микроэлектронике (нанесения контактов, получения микроэлектронных схем и т.д.).
Использование металлических покрытий постоянно расширяется вследствие открытия все новых возможностей их применения. Наиболее широкие возможности использования у электрохимических покрытий, так как при их получении имеются дополнительные методы управления свойствами покрытий вследствие изменения тока или потенциала электрода.
Указанные выше преимущества управления свойствами покрытий можно в общем виде продемонстрировать, если рассмотреть зависимость скорости восстановления от потенциала, представленную на рис. 9.2.
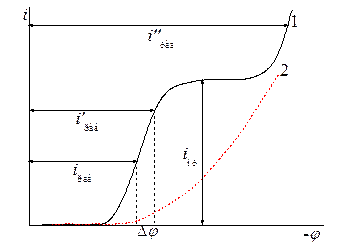
Рис. 9.2 Схема, поясняющая возможности управления свойствами получающихся металлов при электроосаждении
Электролитическое осаждение металлов из растворов, содержащих его простые гидратированные ионы можно осуществить различным путем (рис. 9.2). Если осуществлять процесс при рабочей плотности тока  , то можно получить на поверхности металла плотный, хорошо сцепленный с основой осадок. Изменяя рабочую плотность тока
, то можно получить на поверхности металла плотный, хорошо сцепленный с основой осадок. Изменяя рабочую плотность тока 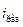 в пределах, схематически представленных на рис 9.2, можно регулировать не только скорость осаждения, но и в известной мере структуру осадка, поскольку она зависит от потенциала электрода, который будет меняться в пределах D j, а также от плотности тока, так как скорость процесса определяет скорость образования зародышей и многие особенности кристаллизации.
в пределах, схематически представленных на рис 9.2, можно регулировать не только скорость осаждения, но и в известной мере структуру осадка, поскольку она зависит от потенциала электрода, который будет меняться в пределах D j, а также от плотности тока, так как скорость процесса определяет скорость образования зародышей и многие особенности кристаллизации.
Если рабочая плотность тока будет превышать значение i пр ( ), осаждение будет происходить иначе. При этом, как правило, образуются мелкокристаллические порошки.
), осаждение будет происходить иначе. При этом, как правило, образуются мелкокристаллические порошки.
Таким образом, знание величин предельных токов, которые, как правило, являются катодными предельными токами, имеющими диффузионную природу (их достижение определяется скоростью ионного массопереноса в растворе, см. раздел I). Повышение i пр (а, следовательно, увеличение скорости осаждения) достигается увеличением концентрации, повышением температуры и скорости перемешивания. Кажется очевидным, что все эти факторы являются определяющими для повышения скорости электроосаждения, поскольку позволяют повысить рабочую плотность тока  (рис. 9.2).
(рис. 9.2).
Структура покрытий, а, следовательно, их физико-механические свойства зависят от потенциала электроосаждения. Потенциал осаждения можно изменять в широких пределах, изменяя состав раствора. В частности, для этого широко используются растворы комплексообразователей, например, цианидные растворы. В этом случае зависимости скорости электроосаждения от потенциала может определяться кривой 2 на рис. 9.2.
Очень часто электроосаждение идет с выходом по току, отличающимся от 100%. Одной из основных побочных реакций является реакция восстановления иона гидроксония до газообразного водорода.
Достигаемая плотность тока (с учетом выхода по току) определяет скорость электроосаждения, а, следовательно, задаваемую толщину покрытий. При этом следует учитывать, что, как правило, на поверхности электрода имеет место распределение локальных плотностей тока (а, следовательно, неравномерность толщины покрытия). Методы повышения равномерности (рассеивающей способности электролитов) рассмотрены в лекции 2 настоящего раздела.
Как правило, электролиты для электроосаждения содержат ряд различных компонентов, играющих свою роль в процессе, а не только источник металлических ионов для осадка. Некоторые из них играют роль буферирующих добавок, обеспечивая поддержание pH, другие служат для повышения электропроводности, а, следовательно, уменьшения напряжения на электролитической ванне, третьи играют роль катализатора электроосаждения. Очень часто применяются блескообразующие добавки, в качестве которых используются различные органические (специально разработанные для каждого конкретного случая) добавки.
|
|
|
|
Дата добавления: 2014-01-13; Просмотров: 317; Нарушение авторских прав?; Мы поможем в написании вашей работы!