
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Выход по току и удельный расход энергии при электролизе расплавов
|
|
|
|
При электролизе водных растворов катодный выход по току чаще всего определяется возможным выделением водорода одновременно с получаемым металлом. При электролизе обезвоженных расплавленных сред снижение выхода по току по сравнению с теоретическим значением обусловлено специфическими для расплавов причинами, вследствие которых выход по току в отдельных случаях может быть даже ниже, чем в водных растворах. Основной причиной снижения выхода металла по току является взаимодействие анодных и катодных продуктов электролиза с электролитом и друг с другом с образованием исходных соединений. Существенно снижается выход по току, например, за счет взаимодействия выделившегося на катоде металла с расплавленным электролитом – образуются соединения низшей валентности, так называемые субсоединения, например AlCl, Mg 2 Cl 2, AlF.
Субсоединения могут достигать анода и там окисляться. Они могут окисляться, реагируя с образовавшимися на аноде продуктами, например, с растворенным в электролите СО 2. Достигнув поверхности электролита, они могут испаряться или взаимодействовать с окружающей средой, что также снижает выход по току.
Определенное количество металла теряется в виде металлического «тумана» - золя металла, который образуется в результате реакций диспропорционирования или диспергирования катодного металла в электролите.
Растворимость металла в расплаве увеличивается с температурой и иногда достигает весьма больших значений. Взаимодействие продуктов электролиза между собой и с электролитом зависит от плотности тока на катоде.
В практических условиях для проведения электролиза выбирают параметры, зависящие от ряда условий. Между параметрами электролиза – составом электролита, плотностью тока, температурой, межэлектродным расстоянием – и их влиянием на выход по току обычно существует сложная зависимость.
Работу электролизных цехов в первую очередь оценивают показателем, который характеризует расход электроэнергии на единицу массы продукции (кВт·ч/т):
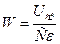 , (14.3)
, (14.3)
где Uср – напряжение на лектролизере, В; C – электрохимический эквивалент, г/(А·ч); e – выход по току, доли единицы.
На практике, например, в производстве алюминия, часто пользуются величиной, обратной удельному расходу и условно называемой выходом по энергии ВЭ. Эта величина измеряется количеством металла, выделяемого при расходе 1 кВт·ч энергии:
ВЭ = 1/W =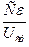 (14.4)
(14.4)
|
|
|
|
Дата добавления: 2014-01-13; Просмотров: 1211; Нарушение авторских прав?; Мы поможем в написании вашей работы!