
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Закон Бугера-Ламберта-Бера
Практическое применение
Практическое применение спектрального анализа
- анализ исходного сырья и готовой продукции в металлургии
- анализ геологических проб при поиске полезных ископаемых
- анализ природных и сточных вод, почвы, атмосферы
- анализ медицинских и биологических объектов
- анализ чистых материалов в электронной технике, анализ реактивов
- анализ образцов в космических исследованиях и др.
Атомно-абсорбционный спектральный анализ.
При поглощении кванта света h ν атом А переходит в возбужденное состояние А*:
А + h ν → А*
Возбуждение атома связано с переходом его электронов на более высокие энергетические уровни. Тогда, если на невозбужденный атом направлять излучение с энергией, равной энергии такого электронного перехода, то это излучение в виде квантов будет поглощаться атомами, а интенсивность самого внешнего излучения будет падать. Эти явления составляют основу метода атомно-абсорбционной спектроскопии. Таким образом, если в эмиссионной спектроскопии концентрация вещества связывалась с интенсивностью излучения, которое было прямо пропорционально числу возбуждённых атомов, то здесь аналитический сигнал (уменьшение интенсивности излучения) связан с числом невозбужденных атомов.
К абсорбционной спектроскопии относятся такие широко используемые анализы, как:
– спектрофотометрический анализ – основан на определении спектра поглощения или измерении светопоглощения при строго определенной длине волны (λ). Эта спектральная линия соответствует максимуму кривой поглощения данного вещества;
– фотоколориметрический анализ – основан на измерении интенсивности окраски исследуемого окрашенного раствора или сравнении ее с интенсивностью окраски стандартного раствора.
- определение небольших содержаний около 70 элементов таблицы Менделеева
- анализ металлов, сплавов, продуктов гидрометаллургии, концентратов и др.
- определение содержания микроэлементов в почве, удобрениях, растениях
- анализ крови на свинец, ртуть, висмут.
Это основной закон фотометрии, устанавливающий количественную зависимость светопоглащения (уменьшение интенсивности света, проходящего через раствор окрашенного вещества) и концентрации раствора окрашенного вещества.
Если на окрашенный прозрачный раствор падает свет интенсивности (I0), то часть его (IА) поглощается молекулами растворенного вещества, а часть излучения (It) проходит через раствор, т.е. I0= It+ IА
На основании экспериментальных данных было установлено, что:
| Слои вещества одинаковой толщины, при прочих равных условиях (Т, Р, V, pH = const), всегда поглощают одну и ту же часть падающего на них светового потока |
It= I0·10-kl,
где l – толщина поглощающего слоя в см, k – коффициент поглощения, I0– интенсивность падающего светового потока,It – интенсивность светового потока после прохождения через слой жидкости.
Коэффициент поглощения k зависит от природы растворенного вещества, длины волны падающего света и пропорционален концентрации растворенного вещества:
k=ε·Cm
где Сm – молярная концентрация вещества, моль/л, ε – молярный коэффициент поглощения, не зависящий от концентрации (справочная величина).
Тогда закон фотометрии принимает вид:
It= I0·10-ε·С·l
Логарифм отношения 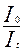 называется оптической плотностью D:
называется оптической плотностью D:
lg 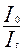 = D = ε·c·l (*)
= D = ε·c·l (*)
Отсюда главное следствие закона Бугера-Ламберта-Бера: оптическая плотность раствора прямо пропорциональна концентрации вещества и толщине поглощающего слоя
Отношение интенсивности светового потока, прошедшего через раствор (It), к интенсивности падающего светового потока (I0), выраженное в процентах, называют пропусканием и обозначают буквой Т:
Т =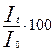 , %
, %
Величина Т, отнесенная к толщине слоя раствора в 1 см, называется коэффициентом пропускания.
|
Дата добавления: 2014-01-14; Просмотров: 3333; Нарушение авторских прав?; Мы поможем в написании вашей работы!