
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Вопрос 3. Постулаты Бора и объяснение происхождения линейчатых спектров.Закономерности в атомных спектрах
|
|
|
|
Опытные данные об атоме водорода. Естественно начинать изучение структуры атомов с самого простого атома – атома водорода. Ко времени создания теории Бора об атоме водорода имелись следующие экспериментальные сведения. Атом водорода состоит из ядра (протона), несущего положительный заряд, равный по величине заряду электрона, и одного электрона, который согласно планетарной модели Резерфорда, движется вокруг ядра по круговой или эллиптической орбите. Размеры атома водорода определяются диаметром орбиты электрона и составляют несколько больше 10-10 м.
Наиболее важные для создания теории атомов сведения были получены из спектра излучения водорода. Спектр водорода оказался наиболее простым по сравнению со спектрами других элементов. В нем были обнаружены удивительно простые и в то же время выполняющиеся с очень большой точностью закономерности в расположении спектральных линий, так называемые спектральные серии (спектральные серии найдены были также и в спектрах других элементов, но формулы для их описания оказались более сложными, а совпадение этих формул с опытом значительно менее точным). Оказалось, что частоты всех линий, которые наблюдаются в спектре излучения водорода, определяются формулой:
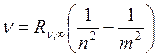 . (19.2)
. (19.2)
Это обобщенная формула Бальмера. Здесь ν – частота световой волны, 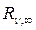 – постоянная Ридберга (
– постоянная Ридберга (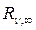 =3,293 · 1015 c -1, n =1,2,3 …, m =2, 3, 4 …).
=3,293 · 1015 c -1, n =1,2,3 …, m =2, 3, 4 …).
Ядерная модель атома в сочетании с классической механикой и электродинамикой оказалась неспособной объяснить ни устойчивость атома, ни характер атомного спектра. Выход из создавшегося тупика был найден в 1913 г. датским физиком Нильсом Бором, правда, ценой введения предположений, противоречащих классическим представлениям. Допущения, сделанные Бором, содержатся в двух высказанных им постулатах.
1. Первый постулат Бора (постулат стационарных состояний) гласит: из бесконечного множества электронных орбит, возможных с точки зрения классической механики, осуществляются в действительности только некоторые дискретные орбиты, удовлетворяющие определенным квантовым условиям. Электрон, находящийся на одной из этих орбит, несмотря на то, что он движется с ускорением, не излучает электромагнитных волн (света).
Согласно первому постулату атом характеризуется системой энергетических уровней, каждый из которых соответствует определенному стационарному состоянию. Стационарным состояниям соответствуют стационарные орбиты, по которым электрон может вращаться вокруг ядра неопределенно долго, не излучая энергию. Энергия атома может измениться лишь при скачкообразном переходе электрона из одного энергетического состояния в другое.
2. Второй постулат Бора ( правило частот ) формулируется следующим образом: излучение испускается или поглощается в виде светового кванта энергии 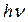 при переходе электрона из одного стационарного (устойчивого) состояния в другое (рис. 19.4). Величина светового кванта равна разности энергий тех стационарных состояний, между которыми совершается квантовый переход электрона:
при переходе электрона из одного стационарного (устойчивого) состояния в другое (рис. 19.4). Величина светового кванта равна разности энергий тех стационарных состояний, между которыми совершается квантовый переход электрона:
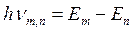 . (19.3)
. (19.3)
Отсюда следует, что изменение энергии атома, связанное с излучением при
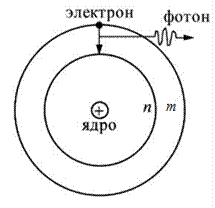
Рис. 19.4
поглощении фотона, пропорционально частоте ν:
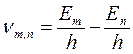 , (19.4)
, (19.4)
т.е. частота излучаемого света может быть представлена в виде разности двух величин, характеризующих энергию излучающей системы.
Второй постулат Бора также противоречит электродинамике Максвелла. По Бору частота излучения определяется только изменением энергии атома и никак не зависит от характера движения электрона. А согласно Максвеллу (т.е. с точки зрения классической электродинамики) частота излучения зависит от характера движения электрона.
Важную роль в развитии планетарной модели сыграли эмпирические закономерности, полученные для линейчатого спектра атома водорода.
В 1858 г. швейцарский физик И. Бальмер установил, что частоты девяти линий в видимой области спектра водорода удовлетворяют соотношению
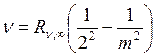 , (19.5)
, (19.5)
m =3,4, 5, …, 11.
Открытие водородной серии Бальмера (4.5) послужило толчком для обнаружения других серий в спектре атома водорода в начале 20 века.
Из формулы (19.5) видно, что по мере увеличения m частота 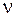 линий спектра возрастает, при этом интервалы между соседними частотами уменьшаются, так что при
линий спектра возрастает, при этом интервалы между соседними частотами уменьшаются, так что при 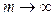 частота
частота 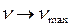 . Максимальное значение частоты в серии Бальмера, полученное при
. Максимальное значение частоты в серии Бальмера, полученное при 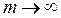 , называется границей серии Бальмера, за пределами которой находится непрерывный спектр.
, называется границей серии Бальмера, за пределами которой находится непрерывный спектр.
В ультрафиолетовой области спектра водорода находится серия Лаймана:
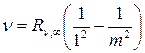 , m =2,3,4… (19.6)
, m =2,3,4… (19.6)
В инфракрасной области расположены еще четыре серии:
Серия Пашена, 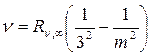 , m = 4,5,6…
, m = 4,5,6…
Серия Брэкета 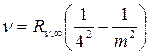 , m = 5,6,7… (19.7)
, m = 5,6,7… (19.7)
Серия Пфунда 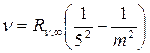 , m = 6,7,8…
, m = 6,7,8…
Серия Хэмфри 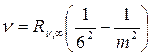 , m = 7,8,9…
, m = 7,8,9…
Как уже отмечалось, частоты всех линий спектра атома водорода представляются одной формулой (19.2).
Частота линии в каждой серии стремится к предельному максимальному значению 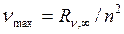 , которое называется границейсерии. Спектральные серии Лаймана и Бальмера обособлены, остальные серии частично перекрываются. Например, границы (длины волн) первых трех серий (Лаймана, Бальмера, Пашена) соответственно равны 0,0912 мкм,
, которое называется границейсерии. Спектральные серии Лаймана и Бальмера обособлены, остальные серии частично перекрываются. Например, границы (длины волн) первых трех серий (Лаймана, Бальмера, Пашена) соответственно равны 0,0912 мкм,
0,3648 мкм, 0, 8208 мкм (λ min = c / ν max).
Бором было введено правило квантования орбит, которое гласит: в стационарном состоянии атома электрон, двигаясь по круговой орбите
радиуса r, должен иметь дискретные, т.е. квантованные, значения момента импульса, удовлетворяющие условию
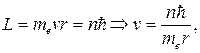 n =1, 2, 3…, (19.8)
n =1, 2, 3…, (19.8)
где n – главное квантовое число.
|
|
|
|
|
Дата добавления: 2014-11-06; Просмотров: 1316; Нарушение авторских прав?; Мы поможем в написании вашей работы!