
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Электрический ток в жидкостях
|
|
|
|
Водные растворы солей, кислот, щелочей хорошо проводят электрический ток. Прохождение тока через эти жидкости вызывает выделение их составных частей на электродах. Это явление называется электролиз, а жидкости, в которых наблюдается электролиз, называются проводниками второго рода или электролитами. Носителями зарядов в электролите являются ионы (рис. 50), которые появляются за счет диссоциации молекул.
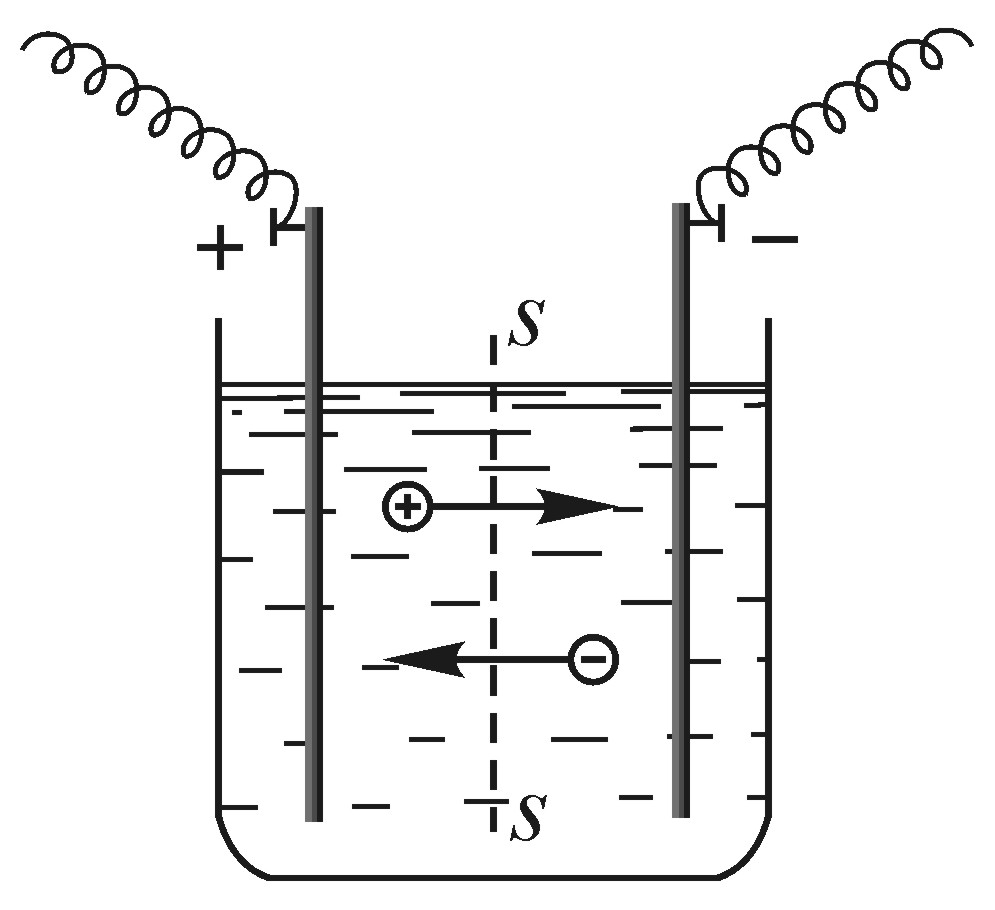 Рис. 50
Рис. 50
|
Законы электролиза установлены М. Фарадеем.
Первый закон: Масса выделившегося на электроде вещества прямо пропорциональна электрическому заряду, прошедшему через электролит:
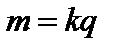
Коэффициент k называется электрохимическим эквивалентом вещества. Учитывая, что 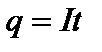 , получим
, получим
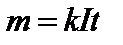
Второй закон: Электрохимические эквиваленты веществ прямо пропорциональны их химическим эквивалентам
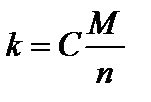 ;
; 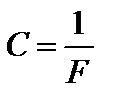 ;
;
F – называется постоянной Фарадея; М – молярная масса; n – валентность; 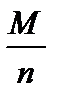 – химический эквивалент.
– химический эквивалент.
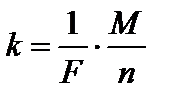 ;
;
Подставляя k в первый закон Фарадея, получим:
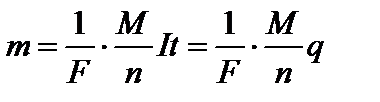 – это объединенный закон Фарадея.
– это объединенный закон Фарадея.
Пусть m = M, n = 1, тогда F = q. Из этого следует физический смысл постоянной Фарадея и ее численное значение. Постоянная Фарадея равна электрическому заряду, который необходимо пропустить через электролит для выделения на электроде одного моля вещества. В одном моле вещества NA зарядов величиной, равной заряду электрона. Поэтому
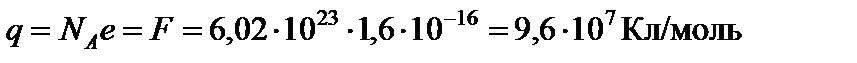 .
.
|
|
|
|
|
Дата добавления: 2014-11-07; Просмотров: 489; Нарушение авторских прав?; Мы поможем в написании вашей работы!