
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Диаграмма состояния для сплавов, образующих химические соединения
|
|
|
|
Рекомедации К Самостоятельному ИЗУЧЕНИЮ ОСНОВНЫХ РАЗДЕЛОВ ДИСЦИПЛИНЫ
1.1. СТРОЕНИЕ МЕТАЛЛОВ
Металлы, их классификация и основные физические свойства. Различные агрегатные состояния и кристаллическое строение металлов. Реальное строение металлов и дефекты кристаллических решеток. Строение сплавов.
Рассмотрите типы связей в твёрдых телах, основное внимание обратите на особый тип металлической связи, который обуславливает отличительные свойства металлов: высокую электропроводность и теплопроводность, высокую пластичность и металлический блеск. Металлические тела характеризуются кристаллическим строением.
Однако свойства реальных кристаллов определяются известными несовершенствами кристаллического строения. В связи с этим необходимо разобраться в видах несовершенств, особенно в строении дислокаций, причинах их легкого перемещения в кристаллической решетке и их влиянии на механические свойства.
Вопросы для самопроверки
1. В чем сущность металлического типа связи? 2. Каковы характерные свойства металлов и чем они определяются? 3. Какие металлы относятся к группе черных, цветных? 4. Какие свойства характерных для твёрдых, жидких и газообразных состояний веществ? 5. Что такое элементарная ячейка? 6. В чем сущность анизотропии? 7. Что такое параметр кристаллической решетки, плотность упаковки и координационное число? Виды дислокаций и их строение. 8. Что такое вектор Бюргерса? 9. Приведите объяснение твёрдого раствора, механической смеси, химического (металлического) соединения. 10. Что представляют собой твердые растворы замещения и внедрения?
1.2. КРИСТАЛЛИЗАЦИЯ И СТРУКТУРА МЕТАЛЛОВ И СПЛАВОВ
Энергетические и температурные условия процесса кристаллизации. Механизм и основные закономерности процесса кристаллизации. Превращения в твердом состоянии. Полиморфизм.
Термодинамические причины фазовых превращений являются одним из частных случаев общего закона природы – стремления любой системы к состоянию с наименьшим запасом энергии (в данном случае свободной энергии или энергии Гиббса). Уясните теоретические основы процесса кристаллизации, состоящего из двух элементарных процессов – зарождения и роста кристаллов, их влияние на эти параметры степени переохлаждения. В процессе кристаллизации при формировании структуры литого металла решающее значение имеет реальная среда, а также возможность воздействия на строение путем модифицирования. Изучите превращения металлов в твердом состоянии на основе явления полиморфизма железа.
Вопросы для самопроверки
1. В чем физическая сущность процесса кристаллизации? 2. В чем физическая сущность процесса плавления? 3. Каковы параметры процесса кристаллизации? 4. Что такое переохлаждение? Какова связь между величиной зерна, скоростью зарождения, скоростью роста кристаллов и степенью переохлаждения? 5. Формы кристаллов и влияние реальной среды на процесс кристаллизации. 6. Образование дендритной структуры. 7. Что такое полиморфизм? Расскажите о полиморфизме на примере железа.
1.3. МЕХАНИЧЕСКИЕ СВОЙСТВА МАТЕРИАЛОВ
Механические свойства материалов. Деформации и напряжения. Испытания материалов на растяжение и на ударную вязкость. Испытания на твердость. Упругая и пластическая деформации, разрушение. Упрочнение и разупрочнение материалов, наклеп и рекристаллизация.
Рассмотрите основные группы механических свойств материалов. Физическую природу деформации и разрушения.
Изучите основные методы оценки механических свойств металлов и физический смысл характеристик, определяемых при различных методах испытаний. Обратите внимание, что свойства, оцененные на гладких образцах, не совпадают со свойствами готового изделия. Это обусловлено наличием в реальных деталях концентраторов напряжений (отверстия, канавки и т. д.), а также различием в характере напряженного состояния образца и детали. Отсюда вытекает важность испытаний образцов с надрезами, позволяющих приблизить условия испытаний к условиям эксплуатации материала и получить результаты, характеризующие его конструкционную прочность. Внимание уделите механизму пластической деформации, ее влиянию на микро- и субмикроструктуру, а также на плотность дислокаций. Уясните связь между строением и механическими свойствами.
Необходимо знать сущность рекристаллизационных процессов: возврата первичной рекристаллизации, собирательной рекристаллизации, протекающих при нагреве деформированного металла. Уясните, как при этом изменяются механические свойства и размер зерна. Установите влияние состава сплава и степени пластической деформации на протекание рекристаллизационных процессов. Научитесь выбирать температуру рекристаллизации. Уясните практическое значение этого процесса, различие между холодной и горячей пластическими деформациями.
Вопросы для самопроверки
1. Какие группы механических свойств вам известны? 2. Что такое деформации? Напряжения? 3. С помощью какой характеристики может быть определено напряженное состояние в точке? В результате чего может возникнуть напряженное состояние в теле? 4. В чем различие между упругой и пластической деформациями? 5. Как изменяется строение металла в процессе пластического деформирования? 6. Как изменяется плотность дислокаций при пластической деформации? 7. Как влияют дислокации на прочность металла? 8. Почему наблюдается огромное различие теоретической и практической прочности? 9. Как влияет изменение строения на свойства деформированного металла? 10. Какие характеристики механических свойств определяются при испытании на растяжение? 11. Что такое твердость? Какие методы определения твердости вы знаете? 12. Что такое ударная вязкость? 13. Как изменяются свойства металла при холодной пластической деформации? 14. Как изменяются свойства деформированного металла при нагреве? 15. В чем сущность процесса возврата? 16. Что такое полигонизация? 17. В чем сущность процессов первичной и вторичной рекристаллизации? 18. Как влияют состав сплава и степень пластической деформации на температуру рекристаллизации? 19. Каково назначение процесса рекристаллизации?
1.4. ДИАГРАММЫ СОСТОЯНИЯ СПЛАВОВ
Правило фаз, построение диаграмм состояния. Диаграмма состояния сплавов, образующих смеси из чистых компонентов. Диаграмма состояния сплавов с неограниченной растворимостью в твердом состоянии. Диаграмма состояния сплавов с ограниченной растворимостью в твердом состоянии, с эвтектикой. Диаграмма состояния сплавов с ограниченной растворимостью в твердом состоянии, с перитектикой. Диаграмма состояния сплавов, образующих химические соединения. Диаграмма состояния сплавов с полиморфным превращением одного из компонентов. Диаграмма состояния сплавов с полиморфными превращениями компонентов и эвтектоидным превращением.
Необходимо отчетливо представлять строение металлов и сплавов в твердом состоянии. Уясните, что такое твёрдый металл, химическое соединение, а также понятия «фаза», «структура». Наглядное представление о состоянии любого сплава в зависимости от его состава и температуры дают диаграммы состояния. Нужно усвоить общую методику построения диаграмм состояния для различных случаев взаимодействия компонентов.
При изучении диаграмм состояния нужно уметь применять правило отрезков (для определения доли каждой фазы или структурной составляющей в сплаве), правило фаз (для построения кривых охлаждения), определять химический состав фаз.
Вопросы для самопроверки
1. Что такое компонент, фаза, структура? 2. Основные группы металлических соединений и их особенности. 3. Как строятся диаграммы состояния? 4. Начертите и проанализируйте диаграмму состояния для случая образования непрерывного ряда твёрдых растворов. 5. Начертите и проанализируйте диаграмму со стояния для случая полной нерастворимости компонентов в твердом состоянии. 6. Начертите и проанализируйте диаграмму состояния для случая образования эвтектики, состоящей из ограниченных твёрдых растворов. 7. Каким образом определяются концентрация фаз и их количественное соотношение? 8. В чем различие между эвтектической и перитектической кристаллизациями? 9. В чем различие между эвтектоидным и эвтектическим превращениями? 10. Виды ликвации и методы их устранения.
1.5. ДИАГРАММА «ЖЕЛЕЗО – УГЛЕРОД (ЦЕМЕНТИТ)»
Компоненты, фазы и структурные составляющие железоуглеродистых сплавов. Изменения структуры сталей при охлаждении. Изменения структуры чугунов при охлаждении.
Научитесь вычерчивать диаграмму состояния «Железо – цементит» и определять все фазы и структурные составляющие этой системы. Изучите, как классифицируются железоуглеродистые сплавы по содержанию углерода. С помощью правила фаз постройте кривые охлаждения для доэвтектоидных, эвтектоидной, заэвтектоидных сталей, эвтектического, доэвтектических и заэвтектических чугунов, технического железа и укажите, какие протекают превращения и какая формируется структура.
Вопросы для самопроверки
1. Что такое феррит, аустенит, перлит, цементит и ледебурит?
2. Какие превращения происходят в сплавах при температурах А1, А2, А3, Аст? 3. Построить с помощью правила фаз кривую охлаждения для стали с 0,8 % С и для чугуна с 4,3 % С. Каковы структура и свойства технического железа, стали и белого чугуна? 4. В каких условиях выделяется первичный, вторичный и третичный цементиты? 5. Каково строение ледебурита при комнатной температуре, немного выше эвтектоидной температуры
727 °С и немного ниже эвтектической температуры 1147 °С? 6. Как классифицируют по структуре стали и белые чугуны?
1.6. ЖЕЛЕЗОУГЛЕРОДИСТЫЕ СПЛАВЫ
Классификация и свойства углеродистых сталей. Классификация и свойства чугунов.
Разберитесь в классификации железоуглеродистых сплавов и усвойте, что различие между тремя классами (технические железо, сталь, чугун) не является формальным (по содержанию углерода). Разные классы сплавов принципиально различны по структуре и свойствам.
Уясните принципиальное различие белых и графитизированных чугунов. Оцените влияние примесей на строение чугунов и разберитесь с их структурой. Запомните основные механические свойства и назначение чугунов, а также их маркировку. Обратите внимание на способы получения ковких и высокопрочных чугунов.
Вопросы для самопроверки
1. Расскажите как влияет углерод на свойства углеродистых сталей. 2. Какие вы знаете полезные и вредные примеси в углеродистых сталях? 3. В чем отличие серого чугуна от белого? 4. Как влияют примеси на свойства чугунов? 5. Каково строение эвтектики и эвтектоида в сером и белом чугунах? 6. Каковы классификация и маркировка серых чугунов? 7. Каковы структуры серых чугунов? 8. Как получают высокопрочный чугун? Его строение, свойства и назначение. 9. Сравните механические свойства серого, ковкого и высокопрочного чугунов. 10. Что означают цифры в марках чугунов СЧ35, КЧ30–6, ВЧ80?
1.7. ТЕОРИЯ И ПРАКТИКА ТЕРМИЧЕСКОЙ ОБРАБОТКИ
УГЛЕРОДИСТЫХ СТАЛЕЙ
Влияние нагрева и скорости охлаждения углеродистой стали на ее структуру. Отжиг углеродистых сталей. Нормализация углеродистых сталей.
Превращения в стали при нагреве. Изотермическое превращение переохлажденного аустенита. Превращение переохлажденного аустенита при непрерывном охлаждении. Мартенситное превращение и его особенности. Превращения при отпуске закаленной стали.
Теория и практика термической обработки стали – главные вопросы металловедения. Термическая обработка – один из основных способов влияния на строение, а следовательно, и на свойства сплавов.
При изучении превращений переохлажденного аустенита особое внимание обратите на диаграмму изотермического распада, устанавливающую связь между температурными условиями превращения, интенсивностью распада и строением продуктов превращения.
Разберитесь в механике и особенностях перлитного, промежуточного и мартенситного превращений. Уясните строение и свойства перлита, сорбита, троостита, бейнита, мартенсита и особенно различие и сходство одноименных структур, получаемых при распаде аустенита и отпуске закаленной стали. Запомните практическое значение термокинетических диаграмм.
Изучите основные виды термической обработки стали Различные виды отжига, нормализации для эвтектоидной, доэвтектоидных и заэвтектоидных сталей. Уясните влияние скорости охлаждения на структуру и свойства стали и физическую сущность процессов отжига, нормализации. При изучении технологических процессов термической обработки обратите внимание на разновидность режимов и их назначение. Для выяснения причин брака при термической обработке стали следует, прежде всего, разобраться в природе термических и фазовых напряжений.
Вопросы для самопроверки
1. Механизм образования аустенита при нагреве стали. 2. В чем разница между наследственно-крупнозернистой и наследственно-мелкозернистой сталью? 3. Каковы механизмы и температурные районы образования перлитного типа (перлита, сорбита, троостита) и бейнита? 4. В чем различие между перлитом, сорбитом и трооститом? 5. Что такое перегрев и пережог стали? 6. Что такое мартенсит и в чем сущность и особенности мартенситного превращения? 7. Как строится изотермические диаграммы переохлажденного аустенита? 8. Каково практическое значение термокинетических диаграмм? 9. В чем заключается сущность отжигов I и II рода? 10. Перечислите известные вам виды отжигов. 11. В чем отличие нормализации от полного отжига?
1.8. ЗАКАЛКА И ОТПУСК УГЛЕРОДИСТЫХ СТАЛЕЙ
Закалка углеродистых сталей. Отпуск закаленных углеродистых сталей. Поверхностная закалка.
Уясните влияние скорости охлаждения на структуру и свойства стали и физическую сущность процессов закалки и отпуска.
Уясните различие между закаливаемостью и прокаливаемостью стали, а также факторы, влияющие на эти характеристики. Обратите внимание, что для получения мартенситного превращения требуется быстрое переохлаждение аустенита, но не во всем интервале температур, а только в том, в котором аустенит менее устойчив. Изучите механизм действия закалочных сред. При изучении технологических процессов термической обработки (закалки) обратите внимание на разновидность режимов и их назначение.
Изучите схему превращений, происходящих в сталях при отпуске, и виды отпускной хрупкости.
Вопросы для самопроверки
1. Что такое критическая скорость закалки? 2. От чего зависит количество остаточного аустенита? 3. Какие вам известны разновидности закалки и в каких случаях они применяются? 4. В чем отличие закалки с полиморфным превращением от закалки без полиморфного превращения? 5. От чего зависит прокаливаемость стали и ее технологическое значение? 6. Каковы особенности известных вам групп охлаждающих сред? 7. В чем сущность превращений при отпуске? 8. Чем отличаются структуры троостита, сорбита отпуска от одноименных структур, образующихся при распаде переохлажденного аустенита? 9. Для какого вида отпуска характерна необратимая отпускная хрупкость? 10. Для какого вида отпуска характерна обратимая отпускная хрупкость?
1.9. ЛЕГИРОВАННЫЕ СТАЛИ
Назначение легирования. Влияние легирующих элементов на структуру и механические свойства сталей. Влияние легирования на превращения при термообработке. Маркировка и классификация легированных сталей.
Изучите влияние легирующих элементов на критические точки железа и сталей и объясните, при каком состоянии углерода и легирующего элемента могут быть получены легированные стали ферритного, перлитного, аустенитного и ледебуритного классов.
Изучите влияние легирующих элементов на кинетику и характер превращения аустенита в перлитной, промежуточной и мартенситной областях. В связи с влиянием легирующих элементов на диаграммы изотермического распада аустенита рассмотрите причины получения различных классов сталей по структуре (перлитного, мартенситного, аустенитного). Уясните влияние легирующих элементов на превращения при отпуске. Запомните, что легирующие элементы, как правило, затормаживают процессы превращений.
Вопросы для самопроверки
1. Как влияют легирующие элементы на положение критических точек А1, А2, А3, Аст? 2. Какие легирующие элементы способствуют графитизации? 3. Какие легирующие элементы являются карбидообразующими? 4. Как влияют легирующие элементы на свойства феррита и аустенита? 5. Как классифицируют легированные стали по структуре в равновесном состоянии? 6. Как классифицируются легированные стали после охлаждения на воздухе? 7. В чем заключаются особенности упрочняющей термической обработки легированных сталей по сравнению с углеродистыми? 8. Расшифруйте состав и содержание легирующих элементов в следующих марках сталей: 12Х2СМФ, 12ХГН2МФБАЮ, 12ХН3А, 18Х2Н4МА, 20ХГНР, 36Х2Н2МФА, 38ХН3МА.
1.10. УПРОЧНЕНИЕ СПЛАВОВ
Упрочнение легированием. Упрочнение пластическим деформированием. Упрочнение термическими методами. Цементация стали. Азотирование стали. Нитроцементация. Физическое упрочнение.
К основным способам упрочнения металлов и сплавов относятся: легирование с образованием твёрдых растворов; пластическое деформирование; создание дисперсных выделений; упрочнение термическими методами; упрочнение химико-термическими методами.
Разберитесь в способах упрочнения сталей легированием, механической, термической и термомеханической обработкой. Разберитесь в сущности явления наклепа и его практическом использовании. Легирование обеспечивает формирование благоприятной структуры металла, повышение его качества и измельчение зерна. Изучите явление наклепа, возникающего в результате холодной пластической деформации, т. е. изменение свойств металла: повышение прочности, электросопротивления, снижение пластичности, плотности, коррозионной стойкости.
При изучении основ химико-термической обработки следует исходить из того, что принципы различных видов этих обработок едины. Процесс химико-термической обработки состоит из выделения атомов насыщающего вещества внешней средой, захвата (абсорбции) этих атомов поверхностью металла и диффузии их внутрь металла. Поэтому рассмотрите реакции в газовой среде при цементации или азотировании и разберитесь в механизме формирования структуры поверхностного слоя. Разберитесь в технологии проведения отдельных видов химико-термической обработки. Уясните преимущества и области использования цементации, азотирования, нитроцементации и различных видов диффузионной металлизации.
Усвойте, что различные виды поверхностной закалки позволяют получать особое сочетание свойств поверхностного слоя и сердцевины изделия, что приводит к повышению его эксплуатационных характеристик. При изучении индукционной закалки уясните связь между глубиной закаленного слоя и частотой тока.
Вопросы для самопроверки
1. Что вы можете рассказать о дисперсионном твердении? 2. Как изменяются свойства изделия при дробеструйной обработке и какова природа этих изменений? 3. Как влияет поверхностное упрочнение на эксплуатационные характеристики изделий? 4. В чем различие между холодной и горячей пластическими деформациями? 5. В чем сущность и особенности термомеханической обработки? 6. Как влияет поверхностная закалка на эксплуатационные характеристики изделия? 7. Каковы преимущества поверхностной индукционной закалки? 8. В чем заключаются физические основы химико-термической обработки? 9. В чем заключается процесс цементации, азотирования? 10. Назначение и режим термической обработки после цементации.
1.11. КОНСТРУКЦИОННЫЕ СТАЛИ
Строительные стали. Цементуемые (нитроцементуемые) стали. Улучшаемые стали. Рессорно-пружинные стали. Подшипниковые стали. Автоматные стали. Износостойкие стали.
Конструкционные стали общего назначения. Необходимо усвоить принципы маркировки сталей и уметь по маркировке определять состав и особенности сталей.
Разберитесь во влиянии легирующих элементов на изменение структуры и свойств стали, особое внимание уделите технологическим особенностям термической обработки сталей различных групп.
Рассмотрите классификации сталей по структуре в нормализованном состоянии и по назначению, уясните основные принципы выбора сталей различного назначения.
В качестве примеров следует указать две-три марки сталей каждой группы, расшифровать состав, назначить термическую обработку, охарактеризовать структуру, свойства и область применения.
Вопросы для самопроверки
1. Расшифруйте химический состав стали марок: 40, 20Х, 30ХГСА, 50Г, 110Г13Л, ШХ15, 18Х22Н4ВА, 5ХНМ, АС30. 2. Какие требования предъявляются к строительным сталям? 3. Назовите группы цементуемых сталей (в зависимости от степени упрочняемости сердцевины) и приведите примеры марок сталей. 4. Какой термической обработке подвергаются цементуемые стали? 5. Какой термической обработке подвергаются улучшаемые стали? 6. Назовите состав стали Гадфильда. К какому виду конструкционных сталей она относится? 7. Основные требования к рессорно-пружинным сталям. Какой термической обработке подвергается данный вид сталей? 8. Какой термической обработке подвергаются подшипниковые стали? 9. Приведите примеры марок автоматных сталей.
1.12. КОРРОЗИОННО-СТОЙКИЕ, ЖАРОСТОЙКИЕ И ЖАРОПРОЧНЫЕ СТАЛИ И СПЛАВЫ
Коррозионная стойкость стали. Жаростойкие стали и сплавы. Коррозионно-стойкие стали и сплавы. Жаропрочные стали и сплавы.
При изучении коррозионно-стойких сталей разберитесь с явлениями химической и электрохимической коррозии.
При изучении жаропрочных сталей обратите внимание на особенности поведения в условиях нагружения при повышенных температурах. Уясните сущность ползучести и основные характеристики жаропрочности. Запомните предельные рабочие температуры и области применения сталей различного структурного класса.
Уясните отличие между жаростойкими и жаропрочными сталями и сплавами.
В качестве примеров следует указать две−три марки сталей каждой группы, расшифровать состав, назначить термическую обработку, охарактеризовать структуру, свойства и область применения.
Вопросы для самопроверки
1. Каковы требования, предъявляемые к нержавеющим сталям? 2. Какие виды коррозии вы знаете? 3. Укажите марки хромистых нержавеющих сталей. Их состав, термическая обработка, свойства и назначение. 4. Укажите марки хромоникелевых нержавеющих сталей. Их свойства, состав, термическая обработка, назначение. 5. Что такое окалиностойкость? 6. Каковы требования, предъявляемые к жаростойким сталям? 7. Какими способами можно повысить окалиностойкость? 8. Каковы требования, предъявляемые к жаропрочным сталям? 9. В чем сущность явления ползучести? 10. Приведите определения предела ползучести и предела длительной прочности. Что такое скорость ползучести? Каков физический смысл этих характеристик? 11. Какими способами можно повысить жаропрочность стали? Объясните природу упрочнения. 12. Приведите примеры жаропрочных сталей перлитного, мартенситного и аустенитного классов. Укажите их состав, обработку, свойства и области применения. 13. Каковы особенности и области применения сплавов на основе никеля и кобальта?
1.13. ИНСТРУМЕНТАЛЬНЫЕ СТАЛИ
Условия работы деформирующих и режущих инструментов, требования к инструментальным материалам. Инструментальные легированные (штамповые) стали. Классификация режущих инструментальных материалов. Режущие инструментальные и быстрорежущие стали.
Изучите классификацию инструментальных сталей в зависимости от назначения и в связи с этим рассмотрите основные эксплуатационные свойства инструмента каждой группы. Особое внимание уделите быстрорежущим сталям. Уясните причины их высокой теплостойкости и особенности термической обработки.
При изучении штамповых сталей необходимо различать условия работы штампов для деформирования в холодном состоянии и штампов для деформирования в горячем состоянии.
Студент обязан уметь выбирать марку стали для инструмента различного назначения, расшифровать ее состав, назначить режим термической обработки, объяснить сущность происходящих при термической обработке превращений и указать получаемые структуру и свойства.
Вопросы для самопроверки
1. Расшифруйте химический состав стали марок: У10, 9ХС, ХВГ, Р18, Р18Ф2, Р9КЮ, Р9М4К8, Х12, 6ХВ2С, Х12М. 2. Как классифицируются инструментальные стали? 3. Требования, предъявляемые к сталям для режущего инструмента. Приведите примеры углеродистых и легированных сталей, используемых для режущего инструмента. Укажите их состав, режим термической обработки, структуру и свойства. 4. Укажите и расшифруйте основные марки быстрорежущей стали. 5. В чем сущность явления красностойкости и каким образом можно повысить красностойкость инструмента? 6. Какова термическая обработка быстрорежущей стали?
7. Как подразделяются штамповые стали? 8. Требования, предъявляемые к щтамповым сталям для деформирования металла в холодном состоянии и к сталям для деформирования металла в горячем состоянии.
1.14. ТВЕРДЫЕ СПЛАВЫ, РЕЖУЩАЯ КЕРАМИКА, СВЕРХТВЕРДЫЕ И АБРАЗИВНЫЕ МАТЕРИАЛЫ
Классификация и свойства твёрдых сплавов. Режущая керамика. Сверхтвердые инструментальные материалы. Абразивные материалы.
Разберитесь с группами твёрдых сплавов, их структурой и назначением. Обратите внимание на рабочие температуры твёрдых сплавов и их основные механические свойства.
Изучите основные группы режущей керамики, ее особенности и эксплуатационные характеристики, область применения.
При изучении сверхтвёрдых материалов обратите внимание на их теплостойкость, ограничивающую их применение в качестве инструментального материала.
Вопросы для самопроверки
1. Что представляют собой твердые сплавы? Каковы их свойства и преимущества? 2. Укажите марки твёрдых сплавов, их состав и назначение.
3. К какому виду твёрдых сплавов относятся марки ТН20, КНТ16? 4. Что представляет собой режущая керамика? Каковы ее свойств, преимущества и недостатки? 5. Укажите основные группы режущей керамики. 6. Что такое сверхтвердые материалы и какие сверхтвердые материалы вы можете назвать? 7. Назовите разновидности сверхтвёрдых поликристаллов на основе синтетического алмаза и нитрид бора. 8. Перечислите абразивные материалы и основные области их применения.
1.15. ТИТАНОВЫЕ И МЕДНЫЕ СПЛАВЫ
Титан и его сплавы. Медь и ее сплавы.
Изучите важнейшие свойства титана и сплавов на его основе в сравнении с другими металлами. Зависимость свойств титана и его сплавов от различных примесей и термической обработки. Рассмотрите классификацию этих сплавов и способы их упрочнения. Разберитесь в основах теории термической обработки (закалка и старение), маркировке, составе, свойствах и области применения этих сплавов.
Изучите классификацию медных сплавов и уясните маркировку, состав, структуру, свойства и области применения каждой группы сплавов. Разберитесь в основах теории термической обработки медных сплавов.
Вопросы для самопроверки
1. Каковы особенности титановых сплавов и области их применения?
2. Какой термической обработке подвергают сплавы на основе титана?
3. Приведите примеры сплавов на основе титана. Укажите их состав, обработку, свойства и области применения. 4. Как влияют примеси на свойства чистой меди? 5. Как классифицируют медные сплавы? 6. Какие сплавы относят к латуням? Их маркировка и состав. 7. Приведите несколько примеров латуней с указанием их состава, структуры, свойств и назначения. 8. Какие сплавы относят к бронзам? Их маркировка и состав. 9. Укажите строение, свойства и назначение различных бронз.
1.16. АЛЮМИНИЕВЫЕ И МАГНИЕВЫЕ СПЛАВЫ
Алюминий и его сплавы. Магний и его сплавы.
Обратите внимание на основные преимущества алюминиевых сплавов, связанных с малым удельным весом и высокой удельной прочностью.
Рассмотрите классификацию этих сплавов и способы их упрочнения. Разберитесь в основах теории термической обработки этих сплавов (закалка и старение), маркировке, составе, свойствах и применении этих сплавов.
Уясните зависимость свойств сплавов магния от различных примесей. Рассмотрите классификацию этих сплавов и способы их упрочнения. Разберитесь в основах теории термической обработки этих сплавов (закалка и старение), маркировке, составе, свойствах и применении этих сплавов.
Вопросы для самопроверки
1. Свойства и применение алюминия. 2. Как классифицируются алюминиевые сплавы? 3. Какие сплавы упрочняются путем термической обработки? Укажите их марки, состав, режим термической обработки, свойства. 4. В чем сущность процесса старения? 5. Какие вы знаете литейные алюминиевые сплавы? Приведите их марки, состав, обработку, свойства. 6. Какие вы знаете жаропрочные алюминиевые сплавы? Укажите предельные рабочие температуры их использования. 7. Каковы свойства магния? 8. Как классифицируются магниевые сплавы? 9. Укажите марки, состав, обработку, свойства и назначение различных сплавов на основе магния.
1.17. НЕМЕТАЛЛИЧЕСКИЕ МАТЕРИАЛЫ
Полимеры и пластмассы. Резиновые и клеящие материалы. Стекло, ситаллы, графит. Композиционные материалы и их строение. Композиционные материалы с металлической матрицей. Композиционные материалы с неметаллической матрицей.
В основе пластмасс лежат полимеры. Обратите внимание на особенности строения полимеров, которые определяют их механические и физико-химические свойства. Классификацию пластмасс рассмотрите с учетом особенностей и состава их строения. Изучите различные группы пластических масс, их свойства и области применения.
Резина отличается от других материалов высокими эластичными свойствами, что обусловлено свойствами основы резины – каучука. Уясните состав резины, способы получения, влияние добавок на ее свойства, области применения. Обратите внимание на клеящие материалы и герметики, в основе которых лежат полимеры и каучук.
К неметаллическим материалам относятся и графит, неорганические стекла, ситаллы, керамика. Разберитесь с особенностями строения, состава, физико-химических свойств и с применением этих групп материалов.
Обратите внимание на принципиальное отличие композиционного материала от известных материалов. Оно заключается в сочетании разнообразных материалов с четкой границей раздела между ними. В связи с этим композиты обладают свойствами, которыми не может обладать ни один из компонентов в отдельности. Укажите свойства композитов в зависимости от вида матрицы, а также от формы, размеров и взаимного расположения наполнителя. Выясните возможные области использования этих материалов.
Вопросы для самопроверки
1. Что лежит в основе классификации полимеров? 2. Укажите область применения термопластов и реактопластов. 3. В чем преимущество пластмасс по сравнению с металлическими материалами? Каковы их недостатки? 4. Что представляет собой резина? 5. Виды стекол? Их отличительные свойства. 6. Укажите основные свойства ситаллов и область их применения. 7. Что такое композиты? 8. Как подразделяют композиты в зависимости от формы и размеров наполнителя? 9. Как подразделяют композиты по виду матрицы? 10. От чего зависят механические свойства композитов?
2. ДОМАШНЯЯ РАБОТА «АНАЛИЗ ДВОЙНЫХ ДИАГРАММ»
2.1. МЕТОДИЧЕСКИЕ УКАЗАНИЯ ПО ВЫПОЛНЕНИЮ ДОМАШНЕЙ РАБОТЫ «АНАЛИЗ ДВОЙНЫХ ДИАГРАММ»
К выполнению домашнего задания предъявляются следующие требования:
· домашнее задание выполняется на формате А4 в печатном виде;
· оформление титульного листа в приложении П1;
· на первой странице указываются номер задания и через тире буквенный индекс варианта, помещается текст содержания задания с указанием названия диаграммы, химического состава заданного сплава и температуры;
· на второй странице слева вычерчивается в масштабе диаграмма так, чтобы справа было место для изображения кривой охлаждения. Для построения кривой охлаждения заданного в варианте сплава необходимо на оси концентраций найти точку, соответствующую составу сплава. Из этой точки восстановить ординату заданного сплава так, чтобы она охватывала диапазон температур от оси концентраций до области жидкого состояния. Ордината сплава должна отчетливо выделяться на диаграмме. Точки пересечения ординаты с линиями диаграммы являются критическими точками заданного сплава (температурами начала или окончания фазовых превращений). Правее диаграммы необходимо вычертить оси «Температура – Время» для построения кривой охлаждения. На ось ординат следует также нанести критические точки заданного сплава в градусах Цельсия;
· на последующих страницах необходимо произвести общее описание заданной диаграммы, описание процесса кристаллизации, указанного в варианте сплава, и определить состав и количество фаз на 1 килограмм сплава.
Пример выполнения домашнего задания приведен в приложении П2.
2.2. ЦелИ и задчи изучения диаграмм состояния
Диаграмма состояния представляет собой графическое изображение зависимости температур фазовых превращений в сплавах от их состава.
Цель изучения диаграмм состояния сплавов:
· научиться по диаграмме состояния устанавливать, какие процессы происходят в сплавах при их охлаждении, какие при этом образуются фазы и структуры сплавов разного состава;
· научиться анализировать процессы фазовых превращений в зависимости от изменения температуры сплава;
· выявлять взаимосвязь механических и технологических свойств сплавов от соответствующего фазового и структурного состояния.
По диаграммам состояния можно устанавливать не только температуры фазовых превращений в сплавах любого состава, но и качество и количество фаз в разных областях диаграммы состояния. Однако этим не исчерпывается практическая значимость диаграмм состояния сплавов. В частности, разбирая процессы, происходящие при охлаждении сплава, по диаграмме состояния можно выявить, в какой форме проявляются образующиеся фазы при охлаждении сплава.
Фазой называется однородная часть системы, образованная компонентами сплава, которая во всех своих точках имеет одинаковые составы, строение и свойства. Жидкая фаза представляет собой раствор расплавленных компонентов. Твердые фазы являются зернами, имеющими определенную форму, размер, состав, структуру и свойства. Это могут быть твердые растворы, химические соединения, зерна чистых компонентов, не образующих с другими компонентами ни твёрдых растворов, ни химических соединений.
Форма проявления фаз называется структурой сплава. Возможность по диаграмме состояния прогнозировать структуру, образующуюся из сплавов разного состава, имеет очень большое практическое значение, так как в двухфазных сплавах не фазы, а именно структуры сплавов определяют их механические свойства. Так, например, стали и белые чугуны состоят из одних и тех же фаз, но свойства этих сплавов сильно различаются именно потому, что структуры этих сплавов разные.
Имеются тысячи разработанных диаграмм состояния сплавов. Все их выучить механически невозможно. Поэтому специалист должен уметь мысленно представить те процессы, которые происходят в сплавах и образуют их структуру и свойства, чтобы оптимально воздействовать на технологический процесс.
Для этого необходимо: 1) ясное понимание особенностей строения основных фаз в сплавах, которыми являются твердые растворы, химические соединения, чистые компоненты; 2) знание, как эти фазы обозначаются; 3) знание признаков этих фаз; 4) умение по диаграмме состояния определить состав и количество фаз; 5) умение логически мыслить.
Для выработки навыка разбора процессов, происходящих при охлаждении конкретного сплава, необходимо обязательно выполнение следующих действий: строить кривую охлаждения разбираемого сплава; против участков кривой охлаждения схематично изображать состояние фаз (структуру) сплава; письменно объяснять процесс, происходящий в сплаве при рассматриваемых температурных условиях.
2.3. ПРАВИЛО ФАЗ
При рассмотрении процессов превращения в диаграммах равновесного состояния сплавов широко применяется так называемое «правило фаз», дающее возможность проверить правильность построения диаграмм и теоретически обосновать направление протекания процессов превращения для установления равновесного состояния системы, которое определяется следующими переменными факторами: температурой, давлением и составом фаз системы (концентрацией).
Число переменных величин (концентрация фаз, температура, давление), которые могут изменяться независимо друг от друга, называется числом степеней свободы или вариантностью системы.
Число степеней свободы зависит от количества компонентов, числа фаз в системе и переменных внешних условий – температуры и давления. Так как давление в практических условиях изменяется в небольших пределах, не оказывая существенного влияния на процессы превращения, то основным переменным фактором является только температура и тогда уравнение «правила фаз» имеет вид
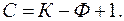 (2.1)
(2.1)
 где С ≥ 0 – число степеней свободы (вариантность системы), К – число компонентов в системе, Ф – количество фаз, находящихся в равновесии при рассматриваемых условиях.
где С ≥ 0 – число степеней свободы (вариантность системы), К – число компонентов в системе, Ф – количество фаз, находящихся в равновесии при рассматриваемых условиях.
Если число степеней свободы системы равно нулю (С = 0), то такое равновесие называют нонвариантным (безвариантным). Это означает, что сплав с данным числом фаз может существовать только при определенных условиях: при постоянной температуре и определенной концентрации всех находящихся в равновесии фаз. Если С = 1, то такая система называется моновариантной (одновариантной), т. е. чтобы не нарушилось равновесное состояние фаз, можно изменить либо концентрацию фаз, либо температуру. Когда С = 2, система бивариантна (двухвариантна). Наличие одной или двух степеней свободы позволяет изменять одну или две переменных без изменения числа фаз.
2.4. Правило отрезков
При анализе строения и свойств сплавов рассматривается состав фаз и их количественное соотношение. Для определения количества фаз и их концентрации в любой точке двухфазной области диаграммы состояния сплавов служит «правило отрезков (рычага)».
На рис. 2.1 приведена диаграмма состояния сплавов с неограниченной растворимостью в твердом состоянии. При температуре t1 сплав состоит из α -твёрдого раствора и жидкой фазы. Для определения массового или объемного соотношения фаз и их состава для сплава I при температуре t1 проводим через данный температурный уровень горизонтальную линию (коноду) до пересечения с ближайшими линиями диаграммы АВС и АDС, ограничивающими двухфазную область. Проекции точек пересечения В, D, спроектированные на ось концентрации В’, D’ показывают состав (концентрацию) фаз: жидкая содержит 20 % В, твердая – 72 % В.
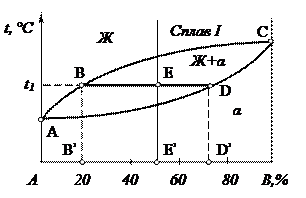
Рис. 2.1. Применение «правила отрезков» для определения концентрации фаз
в двухфазной области диаграммы
Отрезки, лежащие на температурной горизонтали (коноде) между точками концентрации фаз ( В, D ) и средней точкой, соответствующей концентрации исходного сплава (Е), обратно пропорциональны количеству этих фаз:
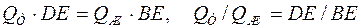 . (2.2)
. (2.2)
Иными словами, количество фазы, например жидкости, характеризуется величиной противолежащего отрезка ЕD, а количество кристаллов
α -твёрдого раствора – величиной противолежащего отрезка ВЕ.
С помощью правила отрезков можно определить не только фазовый состав сплава, но и количественное соотношение структурных составляющих, например избыточных кристаллов и эвтектики.
Для определения количественного соотношения фаз:
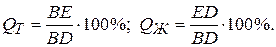 (2.3)
(2.3)
Для определения веса фаз на 1 килограмм сплава:
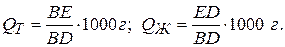 (2.4)
(2.4)
2.5. Общий Обзор диаграмм состояния
Как известно, вид диаграммы состояния зависит от характера взаимодействия компонентов в жидком и твердом состояниях, возможности образования устойчивых и неустойчивых химических соединений, протекания тех или иных нонвариантных превращений. Различные варианты простейших (или типовых) диаграмм состояний как диаграмм равновесия систем безымянных компонентов А и В приведены ниже.
1. Диаграмма состояния для сплавов, образующих смеси из чистых компонентов.
Общий вид диаграммы для случая, когда оба компонента сплава в жидком состоянии неограниченно растворимы, а в твердом – не растворяются, не образуют химических соединений и не имеют полиморфных превращений, представлен на рис. 2.2а. Фазы: жидкость – Ж, чистые компоненты – А и В. Линия АСВ– линия ликвидус; линия ДСЕ – линия солидус. На линии АС начинают выделяться кристаллы А; на линии СВ – кристаллы В; на линии ДСЕ из жидкости концентрации С одновременно выделяются кристаллы А и В. Эвтектическая смесь двух видов кристаллов, одновременно кристаллизующихся из жидкости, называется эвтектикой.
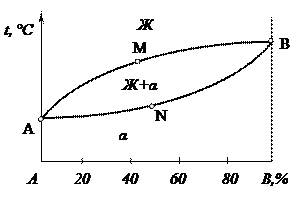
2. Диаграмма состояния для сплавов с неограниченной растворимостью в твердом состоянии.
На рис. 2.2б приведена диаграмма состояния для сплавов с неограниченной растворимостью компонентов друг в друге в жидком и твердом состоянии, имеющих одинаковые типы решеток, небольшую разницу атомных радиусов (до 10–12 %) и сходное строение наружных электронных оболочек, т. е. близость химической природы металлов.
Линия АМВ– линия ликвидус; линия АNВ – линия солидус; фаза α представляет собой неограниченный твёрдый раствор замещения компонентов А и В, зерна этой фазы имеют единую кристаллическую решетку, но у сплавов разного состава число атомов компонентов А и В в элементарных ячейках решетки различно.
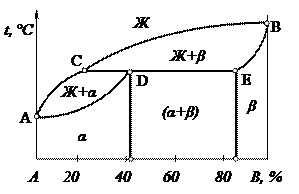
3. Диаграмма состояния для сплавов с ограниченной растворимостью в твердом состоянии, с эвтектикой.
На рис. 2.2в приведена диаграмма состояния для сплавов с ограниченной растворимостью компонентов друг в друге в твердом состоянии, с эвтектическим превращением. Ограниченные твердые растворы на основе компонентов А и В образуются, когда последние заметно отличаются строением и размером атомов, кристаллической структурой и физико-механическими свойствами. Ограниченные твердые растворы могут образовываться по типу замещения и внедрения.
Линия АСВ – линия ликвидус; линия АDCEВ – линия солидус; фаза α является твердым раствором компонента В в кристаллической решетке компонента А; фаза β представляет собой твёрдый раствор компонента А в кристаллической решетке компонента В. Кривые DM и EN – линии ограниченной растворимости в твердом состоянии (сольвус), отражающие характер изменения растворимости компонентов друг в друге в зависимости от температуры. Растворимость компонента В в компоненте А уменьшается с понижением температуры (линия DM). Растворимость компонента А в компоненте В не зависит от температуры (линия EN).
DCE – линия эвтектического превращения ЖВ → (αD+βE). Смесь получившихся в результате данной реакции ограниченных твёрдых растворов αD и βE называется эвтектической (эвтектикой). Сплавы, располо- женные между точкой максимальной растворимости М и эвтектической точкой С, называют доэвтектическими, а сплавы, расположенные между С и N, – заэвтектическими.
4. Диаграмма состояния для сплавов с ограниченной растворимостью в твердом состоянии, с перитектикой.
На рис. 2.2г показана диаграмма состояния для сплавов с ограниченной растворимостью в твердом состояния с перитектическим превращением. Диаграммы такого типа образуют металлы с небольшой разницей в строении атомов и их размеров, но заметно отличающиеся друг от друга температурами плавления.
Линия АСВ – линия ликвидус; линия АDEВ – линия солидус; линия
СDE – линия перитектического превращения, которое заключается в том, что жидкость реагирует с ранее выпавшими кристаллами (ЖВ+βЕ) и образует новый вид кристаллов (ЖВ+αD). Структура двухфазного сплава представляет собой смесь, в которой фаза, выделившаяся ранее (β -фаза), окружена фазой, выделившейся позднее (α -фаза).
Такая диаграмма получается (рис. 2.2д), когда сплавляемые компоненты образуют устойчивое химическое соединение АnВm, не диссоциирующее при нагреве вплоть до температуры плавления и образующее промежуточную фазу постоянного состава. Химическое соединение считается устойчивым, если оно плавится без разложения.
При концентрации, соответствующей химическому соединению АnВm, отмечается характерный перелом на кривой свойств. Это объясняется тем, что некоторые свойства химических соединений обычно резко отличаются от свойств образующих их компонентов. Обычно такие диаграммы состояния характерны для систем, образованных металлами и элементами, которые обладают и металлическими, и неметаллическими свойствами.
В ряде диаграмм состояния сплавов, образующих химические соединения (рис. 2.2е), могут возникать промежуточные фазы переменного состава (δ -фаза), имеющие сравнительно широкие области существования. Эти фазы представляют собой твердые растворы замещения или внедрения в кристаллической решетке химического соединения. Для этих фаз обычно характерны свои кристаллические решетки, отличные от кристаллических решеток компонентов.
Помимо устойчивых химических соединений, которые плавятся (кристаллизуются) при постоянной температуре, в диаграммах могут образовываться и неустойчивые химические соединения, распад которых происходит, не доходя до температуры плавления.
6. Диаграмма состояния для сплавов с полиморфным превращением одного из компонентов.
Полиморфизм (греч.) – многоформие, способность веществ иметь различную кристаллическую структуру в зависимости от внешних условий – температуры и давления.
 а)
а)
|  б)
б)
|
 в)
в)
|  г)
г)
|
 д)
д)
|    е) е)
|
 ж)
ж)
|  з)
з)
|
Рис. 2.2. Простейшие (типовые) диаграммы состояния сплавов
Таблица 2.1
Типы элементарной кристаллической решетки некоторых элементов
| Металл (элемент) | Поли- морфная модифи- кация | Интервал температур устойчивого состояния, °С | Тип кристаллической решетки |
| Fe | α γ α(δ) | <911 911–1392 1392–1539 | Кубическая объемно центрированная Кубическая гранецентрированная Кубическая объемно центрированная |
| Co | α β | <450 450–1480 | Гексагональная плотноупакованная Кубическая гранецентрированная |
| Sn | α β | <18 18–232 | Алмазная Тетрагональная объемноцентрированная |
| Mn | α β γ δ | <700 700–1079 1079–1243 1143–1244 | Кубическая сложная многоатомная Кубическая сложная многоатомная Тетрагональная гранецентрированная Кубическая объемно центрированная |
| Ti | α β | <882 882–1660 | Гексагональная плотноупакованная Кубическая объемно центрированная |
| Zr | α β | <867 867–1860 | Гексагональная плотноупакованная Кубическая объемно центрированная |
| U | α β γ | <668 668–720 720–1132 | Орторомбическая Тетрагональная Кубическая объемно центрированная |
| Ca | α β | <450 450–816 | Гексагональная плотноупакованная Кубическая гранецентрированная |
| Si | <1414 | Алмазная | |
| P | <44 | Кубическая | |
| W | <3380 | Кубическая объемно центрированная | |
| Cu | <1083 | Кубическая гранецентрированная | |
| La | α β γ | <310 310–844 844–920 | Кубическая обьемноцентрированнная Кубическая гранецентрированная Гексагональная плотноупакованная |
| Mg | <650 | Гексагональная плотноупакованная | |
| Pb | <327 | Кубическая гранецентрированная | |
| Al | <657 | Кубическая гранецентрированная |
При полиморфическом превращении изменяется не только форма элементарной ячейки, но и характер и свойства кристаллов.
Полиморфизмом обладают многие металлы (Fe, Ti, Mn и др.), неметаллы (С, S и др.) и промежуточные фазы (TiCr2, BaPb и др.). Разные полиморфные модификации обозначаются буквами греческого алфавита – α, β, γ и т. д. На диаграмме состояния каждая полиморфная модификация имеет свою область существования и образующиеся твердые растворы на их основе отделены друг от друга двухфазными областями.
В табл. 2.1 приведены типы элементарной кристаллической решетки и температурные инервалы их существования для некоторых металлов и неметаллов.
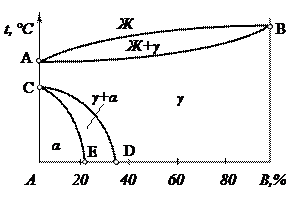
Простейшая диаграмма состояния системы с рядом γ -твёрдых растворов между высокотемпературной модификацией компонента А и компонентом В показана на рис. 2.2ж. Линии CE и CD – линии начала и конца полиморфного превращения γ → α. В сплавах участка Е – D подобное превращение до конца не доходит и при комнатной температуре они сохраняют двухфазную структуру (γ+α). Сплавы, лежащие правее точки D, полиморфного превращения не испытывают и при всех температурах ниже солидуса имеют структуру γ -раствора.
|
|
|
|
|
Дата добавления: 2014-10-15; Просмотров: 1365; Нарушение авторских прав?; Мы поможем в написании вашей работы!