
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Тепловий розрахунок І теплової підстадії
|
|
|
|
ТЕПЛОВІ РОЗРАХУНКИ
Теплові розрахунки виконуються з метою визначення кількості тепла, яке необхідно підвести або відвести для здійснення процесу, обчислення поверхні теплообміну і витрат теплоносіїв і холодоагентів.
Для періодичного процесу теплові розрахунки і тепловий баланс складаються на одну операцію за прийнятим або заданим температурним графіком роботи апарату [13]. Для першої стадії технологічного процесу одержання о-ТСА температурний графік роботи реактора матиме такий вигляд:
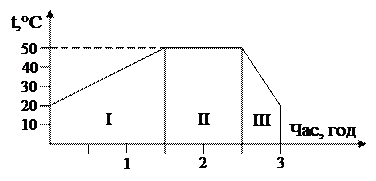
Рис. 4.1 Температурний графік роботи реактора Р1
І теплова підстадія – розігрів вихідних речовин від 20 до 50°С;
ІІ теплова підстадія – витримка при постійній температурі 50°С;
ІІІ теплова підстадія – охолодження продуктів реакції від 50 до 20°С.
Рівняння теплового балансу має вигляд:
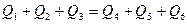 ,
,
де 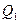 - тепло, що вноситься в апарат з вихідними речовинами, кДж;
- тепло, що вноситься в апарат з вихідними речовинами, кДж;
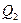 - тепло, що підводиться теплоносієм або відводиться холодоагентом, кДж;
- тепло, що підводиться теплоносієм або відводиться холодоагентом, кДж;
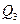 - тепловий ефект процесу, кДж;
- тепловий ефект процесу, кДж;
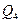 - тепло, що виноситься з апарата продуктами реакції (або тепло, що міститься в продуктах в кінці теплової стадії), кДж;
- тепло, що виноситься з апарата продуктами реакції (або тепло, що міститься в продуктах в кінці теплової стадії), кДж;
 - тепло, що витрачається на нагрівання (охолодження) окремих частин апарату, кДж;
- тепло, що витрачається на нагрівання (охолодження) окремих частин апарату, кДж;
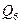 - тепло, що витрачається апаратом у навколишнє середовище, кДж.
- тепло, що витрачається апаратом у навколишнє середовище, кДж.
Основну величину 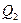 визначають з рівняння:
визначають з рівняння:
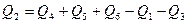 .
.
Кількість тепла, що вноситься в апарат з вихідними речовинами, або ж виноситься з апарата з продуктами реакції, може бути визначена за формулою:
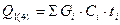 ,
,
де 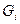 - маса і-того компоненту на одне операційне завантаження, кг;
- маса і-того компоненту на одне операційне завантаження, кг;
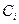 - питома теплоємність і-того компоненту, кДж/(кг·К);
- питома теплоємність і-того компоненту, кДж/(кг·К);
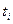 - температура і-того компоненту, °С.
- температура і-того компоненту, °С.
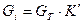 ,
,
де 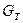 - маса і-того компоненту на 1 тонну 100-ного % готового продукту;
- маса і-того компоненту на 1 тонну 100-ного % готового продукту;
 - перерахунковий коефіцієнт від завантаження на 1 тонну готового продукту до операційного завантаження;
- перерахунковий коефіцієнт від завантаження на 1 тонну готового продукту до операційного завантаження;
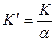 ,
,
де 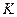 - перерахунковий коефіцієнт від завантаження на 1 тонну готового продукту до добового завантаження,
- перерахунковий коефіцієнт від завантаження на 1 тонну готового продукту до добового завантаження,  ;
;
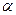 - число операцій, які проводяться на даній стадії за добу,
- число операцій, які проводяться на даній стадії за добу, 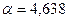 оп/добу;
оп/добу;
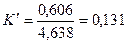 .
.
Оскільки в довіднику вказані молярні теплоємності неорганічних речовин [5], то необхідно провести їх перерахунок в питомі за формулою [13]:
 ,
,
де 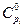 - молярна теплоємність і-того компонента, Дж/(моль·К);
- молярна теплоємність і-того компонента, Дж/(моль·К);
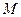 - молекулярна маса, г/моль.
- молекулярна маса, г/моль.
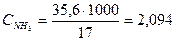 кДж/(кг·К);
кДж/(кг·К);
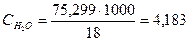 кДж/(кг·К);
кДж/(кг·К);
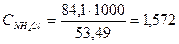 кДж/(кг·К).
кДж/(кг·К).
За відсутності дослідних даних значень питомої теплоємності 25%-ного водного розчину аміаку розрахуємо її за формулою [13]:
 ,
,
де 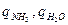 - масовий вміст аміаку і води у розчині, %;
- масовий вміст аміаку і води у розчині, %;
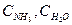 - питомі теплоємності аміаку і води, кДж/(кг·К).
- питомі теплоємності аміаку і води, кДж/(кг·К).
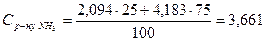 кДж/(кг·К).
кДж/(кг·К).
За відсутності даних теплоємності органічних речовин, визначаємо її за правилом Коппа [13]:
 ,
,
де 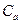 - атомна теплоємність елементів, що входять у склад молекули, кДж/(кг·К);
- атомна теплоємність елементів, що входять у склад молекули, кДж/(кг·К);
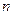 - число однойменних атомів у молекулі;
- число однойменних атомів у молекулі;
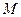 - молекулярна маса сполуки.
- молекулярна маса сполуки.
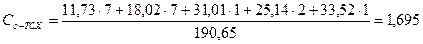 кДж/(кг·К);
кДж/(кг·К);
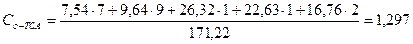 кДж/(кг·К);
кДж/(кг·К);
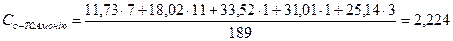 кДж/(кг·К).
кДж/(кг·К).
Теплоємність, розраховану за формулою Коппа, рекомендується збільшити на 5-10%:
 кДж/(кг·К);
кДж/(кг·К);
 кДж/(кг·К);
кДж/(кг·К);
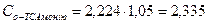 кДж/(кг·К).
кДж/(кг·К).
Таблиця 4.1
Значення питомих теплоємностей речовин
| № п/п | Назва речовини | Питома теплоємність, кДж/(кг·К) |
| 1. | о -Толуенсульфохлорид | 1,780 |
| 2. | п -Толуенсульфохлорид | 1,780 |
| 3. | о -Толуенсульфамід | 1,362 |
| 4. | п -Толуенсульфамід | 1,362 |
| 5. | о -Толуенсульфонат амонію | 2,335 |
| 6. | Аміак | 2,094 |
| 7. | Вода | 4,183 |
| 8. | Амонію хлорид | 1,572 |
Маси і-тих компонентів на одне операційне завантаження взяті із таблиці 2.1. Обчислимо кількість тепла, що вноситься в реактор з вихідними речовинами:
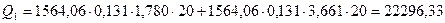 кДж.
кДж.
При розрахунку  прийнятий ступінь перетворення вихідних речовин у продукти реакції на даній стадії спричиняє необхідність проведення додаткових матеріальних розрахунків. Припустимо, що на першій тепловій підстадії ступінь перетворення складає 80%. Очевидно, що продукти реакції на цій стадії будуть представляти собою суміш, у якій міститься по 80% (від загальної кількості речовин, що утворюються з урахуванням коефіцієнту виходу на стадії) кінцевих продуктів реакції і по 20% вихідних продуктів, які вступають у хімічну взаємодію, плюс надлишок вихідних компонентів.
прийнятий ступінь перетворення вихідних речовин у продукти реакції на даній стадії спричиняє необхідність проведення додаткових матеріальних розрахунків. Припустимо, що на першій тепловій підстадії ступінь перетворення складає 80%. Очевидно, що продукти реакції на цій стадії будуть представляти собою суміш, у якій міститься по 80% (від загальної кількості речовин, що утворюються з урахуванням коефіцієнту виходу на стадії) кінцевих продуктів реакції і по 20% вихідних продуктів, які вступають у хімічну взаємодію, плюс надлишок вихідних компонентів.
Склад продуктів реакції на І тепловій підстадії на одне операційне завантаження (див. табл. 2.2):
1. о -Толуенсульфамід……..……….………..…….......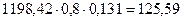 кг
кг
2. п -Толуенсульфамід………..……....….…...………….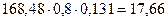 кг
кг
3. о -Толуенсульфонат амонію…...……..........…...............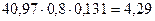 кг
кг
4. Амонію хлорид............................................................. кг
кг
5. о -Толуенсульфохлорид...............................................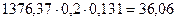 кг
кг
6. п -Толуенсульфохлорид.................................................. кг
кг
7. Аміак..........................................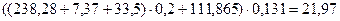 кг
кг
8. Вода................................................................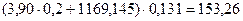 кг
кг
Обчислимо кількість тепла, що міститься в продуктах реакції в кінці першої теплової підстадії:
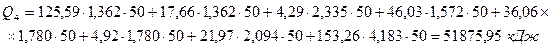
Тепловий ефект процесу 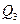 - це сумарна кількість тепла, яке виділяється або поглинається при перебігу хімічних реакцій і фізико-хімічних процесів, що їх супроводжують:
- це сумарна кількість тепла, яке виділяється або поглинається при перебігу хімічних реакцій і фізико-хімічних процесів, що їх супроводжують:
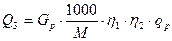 ,
,
де  - маса 100%-ної реагуючої сполуки на одне завантаження, кг;
- маса 100%-ної реагуючої сполуки на одне завантаження, кг;
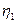 - коефіцієнт виходу хімічної реакції, соті долі відсотка;
- коефіцієнт виходу хімічної реакції, соті долі відсотка;
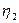 - коефіцієнт виходу хімічної реакції на тепловій підстадії, соті долі відсотка;
- коефіцієнт виходу хімічної реакції на тепловій підстадії, соті долі відсотка;
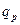 - молярний тепловий ефект хімічної реакції, кДж/моль.
- молярний тепловий ефект хімічної реакції, кДж/моль.
Відповідно до закону Гесса для розрахунку молярного теплового ефекту хімічної реакції необхідно від суми теплот утворення продуктів реакції відняти суму теплот утворення вихідних речовин:
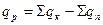 ,
,
де 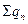 і
і 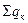 - сума теплот утворення сполук, що вступають в реакцію і утворюються в результаті реакції відповідно, кДж/моль.
- сума теплот утворення сполук, що вступають в реакцію і утворюються в результаті реакції відповідно, кДж/моль.
При відсутності теплот утворення сполук їх можна розрахувати за теплотами згоряння, як різницю між теплотою згоряння елементів, що входять до складу сполуки і теплотою згоряння самої сполуки [13]:
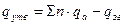 ,
,
де 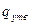 - теплота утворення сполуки, кДж/моль;
- теплота утворення сполуки, кДж/моль;
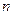 - число однойменних атомів у молекулі;
- число однойменних атомів у молекулі;
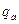 - теплота згоряння 1 грам-атома елемента, кДж;
- теплота згоряння 1 грам-атома елемента, кДж;
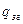 - теплота згоряння сполуки, кДж/моль.
- теплота згоряння сполуки, кДж/моль.
Для визначення теплот утворення сполук, що знаходяться в іншому агрегатному стані, вноситься поправка на теплоти фізичних процесів [13]:
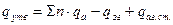 .
.
Оскільки вихідні речовини – рідини, а в результаті реакції утворюється тверді речовини – о -ТСА і п -ТСА, то теплова поправка на агрегатний стан для о -ТСА і п -ТСА буде рівною теплоті топлення відповідно о -ТСА і п -ТСА, яка розраховується за формулою [13]:
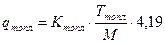 кДж/моль,
кДж/моль,
де 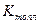 - постійна величина, яка для органічних сполук рівна 9-15; приймаємо, що
- постійна величина, яка для органічних сполук рівна 9-15; приймаємо, що  ;
;
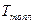 - температура топлення, °К; для о -ТСА
- температура топлення, °К; для о -ТСА  °С, а для п -ТСА
°С, а для п -ТСА  °С.
°С.
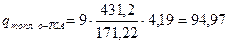 кДж/кг;
кДж/кг;
 кДж/кг.
кДж/кг.
Теплота згоряння рідких органічних сполук визначається за формулою:
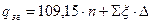 кДж/моль,
кДж/моль,
де 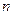 - число електронів, що переміщуються при згорянні органічної сполуки;
- число електронів, що переміщуються при згорянні органічної сполуки;
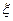 - число однойменних замісників;
- число однойменних замісників;
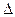 - теплова поправка на зв'язок із замісником, кДж/моль.
- теплова поправка на зв'язок із замісником, кДж/моль.
Розрахунок теплоти згоряння о -ТСХ:
- число електронів, що переміщуються при згорянні:
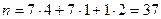 ;
;
- число теплових поправок:  ;
;
- чисельні значення теплових поправок [41, 46]:
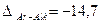 кДж/моль;
кДж/моль;
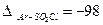 кДж/моль;
кДж/моль;
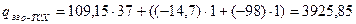 кДж/моль.
кДж/моль.
Розрахунок теплоти згоряння о -ТСА і п -ТСА:
- число електронів, що переміщуються при згорянні:
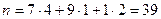 ;
;
- число теплових поправок:  ;
;
- чисельні значення теплових поправок:
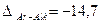 кДж/моль;
кДж/моль;
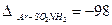 кДж/моль;
кДж/моль;
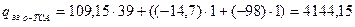 кДж/моль;
кДж/моль;
 кДж/моль.
кДж/моль.
Розрахуємо теплоти утворення о -ТСХ, о -ТСА і п -ТСА:
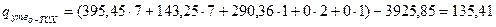 кДж/моль;
кДж/моль;
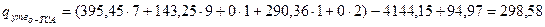 ;
;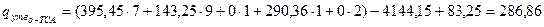 .
.
Теплота утворення о -толуенсульфонату амонію (сіль органічної кислоти) розраховується за формулою:
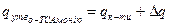 кДж/моль,
кДж/моль,
де 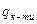 - теплота утворення о-толуєнсульфокислоти (о -ТСК), кДж/моль;
- теплота утворення о-толуєнсульфокислоти (о -ТСК), кДж/моль;
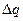 - теплота заміщення –SO2OH на –SO2ONH4, кДж/моль.
- теплота заміщення –SO2OH на –SO2ONH4, кДж/моль.
 кДж/моль,
кДж/моль,
де 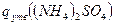 - теплота утворення амонію сульфату, кДж/моль;
- теплота утворення амонію сульфату, кДж/моль;
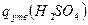 - теплота утворення сульфатної кислоти, кДж/моль;
- теплота утворення сульфатної кислоти, кДж/моль;
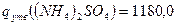 кДж/моль;
кДж/моль; 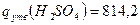 кДж/моль [26];
кДж/моль [26];
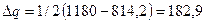 кДж/моль.
кДж/моль.
Розрахунок теплоти згоряння о -ТСК:
- число електронів, що переміщуються при згорянні:
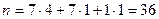 ;
;
- число теплових поправок:  ;
;
- чисельні значення теплових поправок:
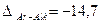 кДж/моль;
кДж/моль;
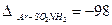 кДж/моль;
кДж/моль;
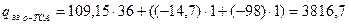 кДж/моль.
кДж/моль.
Теплота утворення о -ТСК:
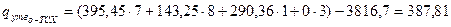 кДж/моль.
кДж/моль.
Теплота утворення о -толуенсульфонату амонію рівна:
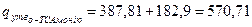 кДж/моль.
кДж/моль.
Таблиця 4.2
Значення теплот утворення речовин [5]
| № п/п | Назва речовини | Теплота утворення, кДж/моль |
| 1. | о -Толуенсульфохлорид | 135,41 |
| 2. | п -Толуенсульфохлорид | 135,41 |
| 3. | о -Толуенсульфамід | 298,58 |
| 4. | п -Толуенсульфамід | 286,86 |
| 5. | о -Толуенсульфонат амонію | 570,71 |
| 6. | Аміак | 46,19 |
| 7. | Вода | 285,83 |
| 8. | Амонію хлорид | 314,20 |
Розрахуємо тепловий ефект основної реакції:
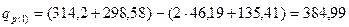 кДж/моль.
кДж/моль.
Розрахуємо тепловий ефект побічних реакцій:
 кДж/моль;
кДж/моль;
 кДж/моль.
кДж/моль.
Тепловий ефект процесу дорівнює:
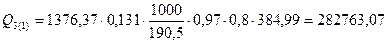 кДж;
кДж;
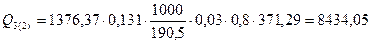 кДж;
кДж;
 кДж;
кДж;
 кДж.
кДж.
Витрата тепла на охолодження окремих частин апарату визначається за формулою:
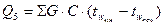 ,
,
де 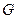 - маса окремих частин апарату, кг;
- маса окремих частин апарату, кг;
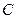 - теплоємність окремих частин апарату, кДж/(кг·К);
- теплоємність окремих частин апарату, кДж/(кг·К);
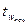 - середня початкова температура окремих частин апарату, °С,
- середня початкова температура окремих частин апарату, °С, 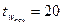 °С;
°С;
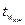 - середня кінцева температура окремих частин апарату, °С.
- середня кінцева температура окремих частин апарату, °С.
Середня кінцева температура 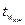 дорівнює середньому арифметичному між температурами стінок з боку холодоагента і реакційної маси:
дорівнює середньому арифметичному між температурами стінок з боку холодоагента і реакційної маси:
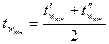 ,
,
де 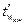 - температура стінки апарату з боку холодоагента, °С;
- температура стінки апарату з боку холодоагента, °С;
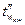 - температура стінки апарату з боку реакційної маси, °С;
- температура стінки апарату з боку реакційної маси, °С;
 ;
;
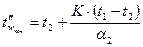 ;
;
 ,
,
де 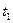 - температура холодоагента, °С;
- температура холодоагента, °С;
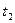 - температура реакційної маси, °С;
- температура реакційної маси, °С;
 - коефіцієнт тепловіддачі від стінки апарату до холодоагенту, Вт/(м2·К);
- коефіцієнт тепловіддачі від стінки апарату до холодоагенту, Вт/(м2·К);
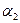 - коефіцієнт тепловіддачі від реакційної маси до стінки апарату, Вт/(м2·К);
- коефіцієнт тепловіддачі від реакційної маси до стінки апарату, Вт/(м2·К);
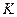 - коефіцієнт теплопередачі від реакційної маси до холодоагенту, Вт/(м2·К);
- коефіцієнт теплопередачі від реакційної маси до холодоагенту, Вт/(м2·К);
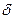 - товщина стінки апарату (одного шару стінки), м;
- товщина стінки апарату (одного шару стінки), м;
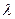 - теплопровідність стінки (одного шару стінки), Вт/(м2·К).
- теплопровідність стінки (одного шару стінки), Вт/(м2·К).
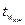 розраховується для кожної частини апарату.
розраховується для кожної частини апарату.

Рис. 4.2 До розрахунку Q5 i Q6: 1-емалеве покриття; 2 – стінка апарата;
3 – стінка сорочки; 4 - теплоізоляції
Для розрахунку витрати тепла на охолодження окремих частин апарату випишемо із довідникової літератури необхідні дані.
Процес протікає в реакторі об'ємом 0,5 м3. Діаметр апарату 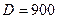 мм, діаметр апарату з сорочкою
мм, діаметр апарату з сорочкою  мм. Висота апарату становить
мм. Висота апарату становить 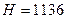 мм. Маса окремих частин апарату становить [13]:
мм. Маса окремих частин апарату становить [13]:
- маса царги 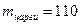 кг;
кг;
- маса накривки 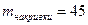 кг;
кг;
- маса днища 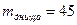 кг;
кг;
- маса лопатевої мішалки 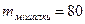 кг;
кг;
- маса сорочки  кг;
кг;
- маса ізоляції 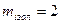 кг.
кг.
Товщина стінок апарату і сорочки: 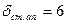 мм;
мм;  мм.
мм.
Товщина ізоляції з пінополістиролу (ППС): 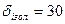 мм.
мм.
Товщина емалевого покриття  мк.
мк.
Температура холодоагенту (розсолу) становить 1 °С, температура реакційної маси рівна 50 °С.
Теплоємність матеріалів становить [18]: 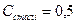 кДж/(кг·К);
кДж/(кг·К);  кДж/(кг·К).
кДж/(кг·К).
Теплопровідність матеріалів складає [18]: 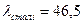 Вт/(м·К);
Вт/(м·К); 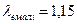 Вт/(м·К);
Вт/(м·К); 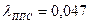 Вт/(м·К).
Вт/(м·К).
Коефіцієнт тепловіддачі при нагріванні і охолодженні розсолу 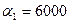 Вт/(м2·К) [13].
Вт/(м2·К) [13].
Коефіцієнт тепловіддачі при нагріванні і охолодженні органічних речовин 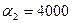 Вт/(м2·К) [13].
Вт/(м2·К) [13].
Розрахуємо коефіцієнт теплопередачі від реакційної маси до холодоагенту:
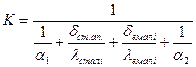 Вт/(м2·К);
Вт/(м2·К);
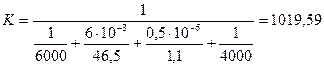 Вт/(м2·К).
Вт/(м2·К).
Температура стінки з боку холодоагента:
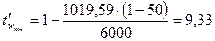 °С.
°С.
Температура стінки з боку реакційної маси:
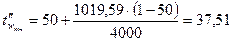 °С.
°С.
Середня кінцева температура стінки апарату:
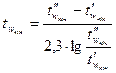 , °С;
, °С;
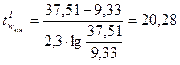 °С.
°С.
Для розрахунку кількості тепла, що віддає накривка апарата, визначимо коефіцієнт теплопередачі від верхньої частини апарату до повітря:
 Вт/(м2·К).
Вт/(м2·К).
Приймаємо, що середня кінцева температура накривки апарату становить 25 °С.
Розрахуємо коефіцієнт теплопередачі від навколишнього середовища до холодоагенту через теплоізоляцію і стінку сорочки:
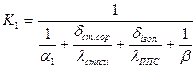 ,
,
де 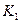 - коефіцієнт теплопередачі від навколишнього середовища до холодоагенту через теплоізоляцію і стінку сорочки, Вт/(м2·К).
- коефіцієнт теплопередачі від навколишнього середовища до холодоагенту через теплоізоляцію і стінку сорочки, Вт/(м2·К).
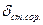 - товщина стінки сорочки, м;
- товщина стінки сорочки, м;
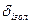 - товщина теплоізоляції, м;
- товщина теплоізоляції, м;
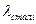 - теплопровідність стінки сорочки, Вт/(м2·К);
- теплопровідність стінки сорочки, Вт/(м2·К);
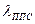 - теплопровідність ізоляції, Вт/(м2·К);
- теплопровідність ізоляції, Вт/(м2·К);
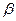 - коефіцієнт тепловіддачі від навколишнього середовища до стінки апарату, Вт/(м2·К);
- коефіцієнт тепловіддачі від навколишнього середовища до стінки апарату, Вт/(м2·К);
Коефіцієнт 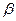 є алгебраїчною сумою тепловіддачі конвекцією
є алгебраїчною сумою тепловіддачі конвекцією 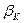 і випромінюванням
і випромінюванням 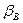 . Якщо температура стінок не перевищує 200 °С, то величиною
. Якщо температура стінок не перевищує 200 °С, то величиною 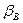 можна знехтувати. Величина
можна знехтувати. Величина 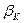 визначається за формулою:
визначається за формулою:
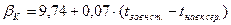 ,
,
де 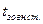 - температура зовнішньої поверхні стінки апарату, °С;
- температура зовнішньої поверхні стінки апарату, °С;
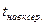 - температура навколишнього середовища (приміщення цеху), °С;
- температура навколишнього середовища (приміщення цеху), °С;
Приймаємо, що  °С;
°С; 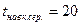 °С, тоді
°С, тоді
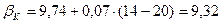 Вт/(м2·К).
Вт/(м2·К).
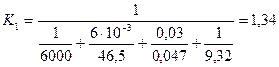 Вт/(м2·К).
Вт/(м2·К).
Розрахуємо середню температуру стінки сорочки:
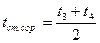 ,
,
де 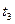 - температура стінки сорочки зі сторони холодоагенту, °С;
- температура стінки сорочки зі сторони холодоагенту, °С;
 - температура стінки сорочки зі сторони теплоізоляції, °С;
- температура стінки сорочки зі сторони теплоізоляції, °С;
 ;
;
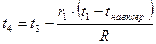 ;
;
де 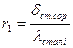 , а
, а 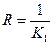 ;
;
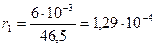 ;
; 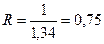 ;
;
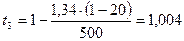 °С;
°С;
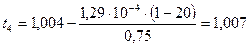 °С;
°С;
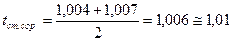 °С.
°С.
Аналогічно розраховуємо середню температуру шару теплоізоляції:
температура шару ізоляції зі сторони сорочки:
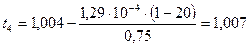 °С;
°С;
температура шару ізоляції зі сторони навколишнього середовища дорівнює температурі зовнішньої стінки ізольованої поверхні апарату  °С;
°С;
оскільки співвідношення  , то середню температуру шару ізоляції обчислюємо за такою формулою:
, то середню температуру шару ізоляції обчислюємо за такою формулою:
 , °С;
, °С;
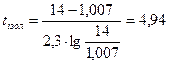 °С.
°С.
Розрахуємо  :
:

Тепло, що витрачається в навколишнє середовище:
 ,
,
де  - поверхня частини апарату, що втрачає тепло (холод), м2;
- поверхня частини апарату, що втрачає тепло (холод), м2;
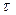 - тривалість процесу, год;
- тривалість процесу, год; 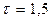 год (табл. 3.1);
год (табл. 3.1);
Площа поверхні ізольованої частини апарату:
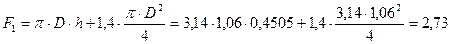 м2.
м2.
Площа поверхні неізольованої частини апарату:
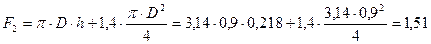 м2.
м2.
Коефіцієнт тепловіддачі від неізольованої стінки апарату в навколишнє середовище:
 Вт/(м2·К);
Вт/(м2·К);
Коефіцієнт тепловіддачі від навколишнього середовища до ізольованої стінки апарату:
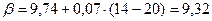 Вт/(м2·К);
Вт/(м2·К);
Визначаємо 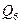 :
:
 кДж.
кДж.
Визначаємо тепло, що необхідно відвести за допомогою холодоагенту:
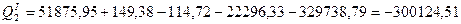 кДж.
кДж.
|
|
|
|
|
Дата добавления: 2014-10-23; Просмотров: 892; Нарушение авторских прав?; Мы поможем в написании вашей работы!