
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
VI. Важнейшие методы очистки газов
|
|
|
|
Перегонка при атмосферном давлении (простая перегонка)
Простую перегонку используют для очистки жидкостей либо от нелетучих примесей (соли, щёлочи, красители), либо от примесей, у которых температуры кипения на 100–150 оС выше температуры кипения очищаемого вещества.
 |
Прибор для простой перегонки (рис.25) состоит из перегонной колбы (колбы Вюрца), термометра, холодильника Либиха, аллонжа и колбы-приёмника. Перед началом перегонки в перегонную колбу помещают центры кипения (кусочки битого фарфора), которые способствуют равномерному кипению жидкости и препятствуют её перебрасыванию в холодильник. Перегонную колбу заполняют очищаемой жидкостью не более, чем на ⅔ её объёма. Термометр закрепляют так, чтобы шарик со ртутью оказался чуть ниже отводной трубки перегонной колбы и полностью омывался парами. Холодную воду пускают в холодильник в направлении «снизу вверх» и начинают нагревание перегонной колбы. Если в ней находится водный раствор, то разрешается нагревание открытым пламенем. Если
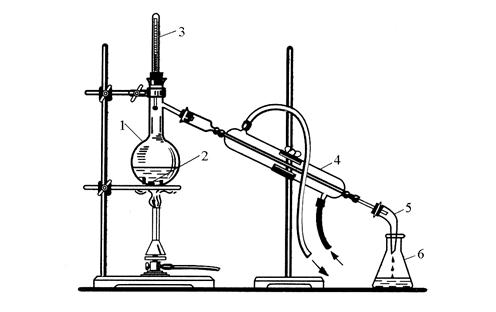 |
же в колбе содержится горючее вещество, то её нагревают на водяной бане. По показаниям термометра идентифицируют перегоняемое вещество и собирают его в колбу-приёмник.
Известны смеси жидких веществ, которые нельзя разделить перегонкой. Они называются азеотрóпными смесями. К ним относится, например, азеотропная смесь этанола с водой с массовой долей спирта, равной 95,6 %. При нормальном давлении температура её кипения составляет 78,17 оС, хотя температуры кипения чистого (100-%-го) спирта и воды выше и равны соответственно 78,3 оС и 100 оС. Поэтому при нагревании растворов спирта с массовой его долей, большей 95,6 %, из них вначале отгоняется азеотропная смесь, а затем чистый спирт. При нагревании растворов спирта с массовой его долей, меньшей 95,6 %, из них так же вначале отгоняется азеотропная смесь, а затем – оставшаяся вода.
Азеотропные смеси разделяют химическими методами.
Простую перегонку широко используют в лабораториях для получения дистиллированной воды (воды, очищенной методом дистилляции) от растворённых в ней солей.
2. Перегонка при пониженном давлении (вакуум-перегонка)
Её применяют, если невозможна простая перегонка, т.е. если очищаемая жидкость при нагревании под атмосферным давлением разлагается. При понижении давления в системе температура кипения очищаемой жидкости уменьшается и она кипит без разложения. Пары её конденсируются и собираются в приёмнике.
Если целью перегонки является разделение жидкой смеси на несколько разных фракций, то такая перегонка называется фракционной или дробной перегонкой.
Газы, полученные в результате соответствующих химических реакций, практически всегда загрязнены парами воды и примесями сопутствующих газов, которые образуются вследствие протекания побочных реакций.
Выбор способа очистки газов зависит как от химических и физических свойств самих газов, так и от свойств содержащихся в них примесей.
В лабораторной практике для высушивания газов наиболее часто применяют концентрированные растворы серной или фосфорной кислот, безводные хлорид кальция или перхлорат магния («ангидрон»), безводный сульфат меди(II), оксид фосфора(V) («фосфорный ангидрид»), гидрид кальция, твёрдый гидроксид натрия («едкий натр»), оксид кальция («негашёная известь»), смесь твёрдых гидроксида натрия и оксида кальция («натронная известь»), частично обезвоженный гель кремниевой кислоты («силикагéль») и др. В каждом конкретном случае выбирают такой осушитель, который поглощал бы пары воды, но не реагировал бы с осушаемым газом. Например, для осушки аммиака нельзя использовать первых шесть из числа указанных осушителей, поскольку аммиак реагирует с ними.
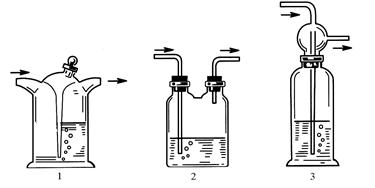 |
Осушающие вещества могут быть жидкими (серная кислота), твёрдыми в виде гранул (хлорид кальция), в виде зёрен (силикагель), в виде порошков (фосфорный ангидрид).
Жидкие осушители используются в промывных склянках (рис.26).
 | |||
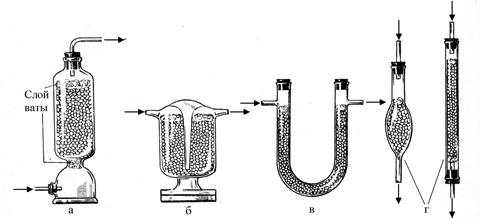 | |||
Твёрдые осушители наиболее часто используются в специальных осушительных колонках (рис.27-а), склянках Тищенко (рис. 27-б), U-образных трубках (рис. 27-в) или в хлоркальциевых трубках (рис.27-г).
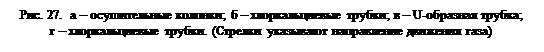 |
|
|
|
|
|
Дата добавления: 2014-11-25; Просмотров: 1954; Нарушение авторских прав?; Мы поможем в написании вашей работы!