
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Рахитоподобные заболевания
|
|
|
|
Это группа наследственных тубулопатий, клиническая картина которых в ранние сроки заболевания имитирует рахит, но не связана с дефицитом поступающего в организм витамина D. Встречаются у 1 из 20 000 родившихся.
Витамин‑0‑зависимый рахит (псевдовитамин‑D‑дефицитный рахит, псевдорахит)
Этиология. К этой группе относятся два заболевания с аутосомно‑рецессивным наследованием. Тип I – генетический дефект синтеза в почках 1,25‑дигидроксивитамина D – l,25(OH)2D3 Тип II – генетическая резистентность рецепторов органов‑мишеней к l,25(OH)2D3.
Клиника. Клинические признаки при I типе болезни появляются в первом полугодии и характеризуются симптомами «цветущего» классического рахита в сочетании с явлениями гипокальциемии: возбудимость, плаксивость, раздражительность, мышечная гипотония, тонические судороги.
Постоянные лабораторные признаки – выраженная гипокальциемия, гипофосфатемия, высокие уровни паратгормонав крови. У большинства больных имеются повышенная активность щелочной фосфатазы в крови, аминоацидурия, глюкозурия, почечный канальцевый ацидоз.
Несмотря на терапию обычными дозами витамина D, заболевание клинически и рентгенологически прогрессирует. В постоянных зубах обнаруживают гипоплазию зубной эмали. Уровни в плазме крови 2 5(OH)D3 нормальные, но l,25(OH)2D3– снижен.
II тип заболевания клинически ничем не отличается от I типа, но у многих больных имеется тотальная алопеция и резко замедлен рост тела.
Уровень 1,25(OH)2D3 в крови нормален и при лечении большими дозами витамина D2 (1–3 мг в сутки), несмотря на повышение уровня 1,25(OH)2D3 в крови до величины, в 2–3 раза превышающей нормальную, гипокальциемия и гипофосфатемия сохраняются. Рентгенологически наиболее типичен остеопороз костей.
Диагноз. Основными критериями служат клинические проявления, семейный характер заболевания с аутосомно‑рецессивным типом наследования, отмеченные особенности метаболических сдвигов и отсутствие эффекта от проводимого антирахитического лечения витаминов D. Наибольшие дифференциально‑диагностические затруднения возникают при разграничении витамин‑Б‑зависимого и витамин‑Б‑дефицитного рахита. В пользу первого свидетельствуют прогрессирующий характер костных деформаций и отсутствие признаков нормализации клинико‑биохимических показателей при контрольном лечении витамином D в дозе 4000 ЕД в сутки в течение 6–8 недель.
Лечение. Заместительная терапия оксидевитом – аналогом биологически активного метаболита витамина D 1,25‑диоксихолекальциферола. Суточные дозы 0,5–4 мкг в зависимости от индивидуальной переносимости препарата и тяжести течения заболевания. Используют также витамин D в дозах от 10 000‑15 000 ЕД до 40 000‑60 000 ЕД в сутки. Обязательны препараты кальция и фосфора, витамина А, С, Е, цитратные смеси курсами по 3–5 мес. Положительная динамика показателей фосфорно‑кальциевого гомеостаза наблюдается через 4–6 недель после начала комплексной терапии. При отмене препаратов витамина D через 3–6 мес. может развиться рецидив заболевания, поэтому лечение проводят непрерывно в течение нескольких лет.
Витамин‑D – резистентный рахит (семейный гипофосфатемический рахит, фосфат‑диабет)
Этиология. Характеризуется доминантным типом наследования, сцепленным с полом, возможен также аутосомно‑доминантный тип. У родителей больных детей возможны небольшой рост, умеренно выраженные деформации костей, иногда – лишь гипофосфатемия натощак. Развитие болезни связывают с первичным нарушением процессов всасывания кальция и фосфора в кишечнике; с первичным дефектом транспорта неорганических фосфатов в почках и повышением чувствительности эпителия канальцев почек к действию паратгормона; с генетически детерминированным сочетанием этих нарушений; с синтезом в организме фосфатурических метаболитов витамина D и недостаточным образованием 25‑оксихолекальциферола в печени.
Клиника. Заболевание проявляется обычно на 2‑м, реже на 1‑м году жизни. Основные симптомы болезни – задержка роста и выраженные прогрессирующие деформации скелета, особенно нижних конечностей (по варусному типу, О‑образные искривления), что сопровождается нарушением походки («утиная походка»); значительная болезненность костей и мышц. В дальнейшем дети низкорослы, приземисты. У девочек костные деформации менее грубые. Нередко отмечается патология зубов. Интеллект сохранен.
Витамин‑Б‑резистентный рахит отличается выраженным клиническим полиморфизмом. Первый вариант характеризуется ранней (на 1‑м году) манифестацией, незначительной степенью костных деформаций, гипофосфатемией, гиперфосфатурией, повышением уровня паратгормона в крови, хорошей переносимостью витамина D. Второй вариант характеризуется более поздней (на 2‑м году) манифестацией, выраженными костными изменениями, гипофосфатемией, значительной гиперфосфатурией, резистентностью к высоким дозам витамина D. Третьему варианту присущи поздние сроки проявления заболевания (в 5–6 лет), тяжесть поражений скелета, выраженная гипофосфатемия, значительное снижение абсорбции фосфора в кишечнике при нормальной или незначительной гиперфосфатурии; отмечается нечувствительность к витамину D. Четвертый вариант характеризуется манифестацией на 2‑м году жизни, умеренной степенью костных деформаций, повышенной чувствительностью к витамину D и склонностью к развитию клинико‑биохимической картины гипервитаминоза D (рвота, тошнота, жажда, гиперкальциемия, гиперкальциурия и др.) в ответ на небольшие дозы витамина D.
Диагноз. Основными критериями диагностики служат: клинические проявления; наследственный анамнез; биохимические отклонения в обмене электролитов. Гипофосфатемия и гиперфосфатурия при нормальном содержании кальция в крови – дифференциально‑диагностический признак. Никогда не выявляют глюкозурию, калиурию, аминоацидурию. Рентгенологически – рахитоподобные изменения костей, преимущественно нижних конечностей.
Лечение витамин‑Б‑резистентного рахита должно быть комплексным. Основные препараты – витамин D и его метаболиты. Начальные дозы витамина D – 10 000‑15 000 ЕД в сутки. Их увеличивают под контролем показателей кальция и фосфора в сыворотке крови и моче, активности щелочной фосфатазы крови, уровень которых определяют каждые 10–14 дней. Максимальные суточные дозы витамина D при первом варианте 85 000–100 000 ЕД, при втором 150 000–200 000 ЕД, при третьем 200 000–300 000 ЕД. При четвертом варианте болезни назначение витамина D противопоказано. Из метаболитов витамина D используют оксидевит в суточной дозе 0,25‑3 мкг, при применении которого необходим строгий контроль (1 раз в 7‑10 дней) за уровнем кальция в крови. В амбулаторных условиях проводят реакцию Сулковича. Противопоказания для консервативной терапии – индивидуальная непереносимость препаратов, выраженная гиперкальциурия (более 4 ммоль/ сут), отсутствие активного процесса в костной ткани по данным лабораторных и рентгенологических исследований. В комплекс лечения включают препараты кальция (глюконат кальция или хлорид кальция по 1,5–2 г в сутки) и фосфора (фитин 1–1,5 г в сутки, глицерофосфат кальция 0,5–1 г в сутки). Для улучшения всасывания кальция и фосфора в кишечнике – длительное (5–6 мес.) применение концентрированных цитратных смесей (лимонная кислота 24 г, цитрат натрия 48 г и дистиллированная вода 500 мл) по 20–50 мл в сутки. В активной фазе болезни при наличии болей в костях и суставах показан постельный режим продолжительностью до 2 недель. В период клинико‑лабораторной ремиссии ограничивают физические нагрузки, ЛФК и лечебный массаж по специальной программе, назначают соляно‑хвойные ванны, показано санаторно‑курортное лечение.
Болезнь де Тони‑Дебре‑Фанкони (глюкоаминофосфат‑диабет)
Этиология. Наследуется по аутосомно‑рецессивному типу, встречаются спорадические случаи, обусловленные свежей мутацией.
В основе болезни лежит врожденное нарушение функции проксимальных отделов канальцев: неспособность к реабсорбции глюкозы, фосфатов и аминокислот (комбинированная тубулопатия). Развивающийся метаболический ацидоз и недостаток фосфорных соединений способствуют нарушению формирования костной ткани по типу остеомаляции и рахитоподобных изменений скелета.
Клиника. Развернутый симптомокомплекс формируется ко второму году жизни; реже наблюдается поздняя манифестация болезни – в 6–7 лет. Начальные клинические проявления – повышенная жажда, полиурия, иногда длительный субфебрилитет, рвота. На втором году жизни выявляют выраженный дефицит массы тела и роста ребенка, задержку становления статико‑моторных функций, рахитоподобные деформации нижних конечностей (вальгусные или варусные), грудной клетки, предплечий и плечевых костей.
Диагноз. Основными критериями диагностики служат: клинические проявления; наследственный анамнез. Характерны биохимические нарушения – снижение уровня кальция и фосфора в крови, повышение активности щелочной фосфатазы, метаболический ацидоз. Экскреция кальция с мочой остается нормальной при повышенном клиренсе фосфатов мочи. Отмечают глюкозурию (20–30 г/л и выше), генерализованную гипераминоацидурию, повышение pH мочи > 6,0. При полиурии до 2 л и более в сутки удельная плотность мочи, как правило, высокая (1025–1035), что обычно связано с глюкозурией.
Рентгенологически определяют системный остеопороз различной степени выраженности, истончение коркового слоя трубчатых костей, разрыхление зон роста, отставание темпов роста костной ткани от биологического возраста ребенка.
Лечение заключается в коррекции электролитных нарушений, сдвигов в кислотно‑щелочном равновесии, устранении дефицита калия и бикарбонатов. Повторные курсы витамина D и его метаболитов для ликвидации нарушений фосфорно‑кальциевого гомеостаза (начальная суточная доза витамина D 25 000‑30 ООО ЕД, максимальная – 75 000–150 ООО ЕД, доза оксидевита 0,5–1,5 мкг в сутки). В комплекс лечения включают препараты кальция, фосфора, витамины А, С, Е, группы В в возрастных дозах. Показано ограничение поваренной соли и включение в рацион продуктов, оказывающих ощелачивающее действие, а также богатых калием. В фазе ремиссии назначают массаж, соляно‑хвойные ванны.
Почечный тубулярный ацидоз (синдром Лайтвуда‑Олбрайта)
Этиология. Наследуется по аутосомно‑рецессивному типу, но не исключаются аутосомно‑доминантное наследование и спорадические случаи, обусловленные первичными мутациями. Первый («классический») тип болезни обусловлен дефектом функции дистальных почечных канальцев; второй тип – дефектом проксимальных канальцев.
Клиника. Первые признаки болезни появляются на первом году жизни: снижение аппетита, полиурия, полидипсия, быстрая утомляемость. Дети отстают в физическом развитии. На втором году жизни развиваются деформации скелета (вальгусные деформации нижних конечностей, «четки», «браслеты», лобные и теменные бугры), выраженная мышечная гипотония. К 2 годам формируется полный симптомокомплекс почечного тубулярного ацидоза. Рентгенологические изменения костной ткани не имеют специфических особенностей и напоминают таковые при болезни де Тони‑Дебре‑Фанкони.
При первом («классическом») типе болезни наблюдаются значительная задержка физического развития, тяжелое течение заболевания с выраженными костными деформациями, гипокальциемия, гипокалиемия, значительный вторичный гиперпаратиреоидизм, сниженное усвоение кальция в кишечнике. Второй тип характеризуется умеренной задержкой физического развития, относительно легким течением заболевания с незначительными костными деформациями, нормокальциемией и нормокалиемией, а также нормальным усвоением кальция в кишечнике.
Диагноз. Основные критерии диагностики – клинические проявления; выраженный метаболический ацидоз, высокий pH мочи, гиперкальциурия, нефрокальциноз, гипофосфатемия, гипокальциемия, повышение активности щелочной фосфатазы, значительное снижение концентрационной функции почек (относительная плотность мочи 1001–1008). При рентгенологическом и ультразвуковом исследовании мочевой системы примерно у половины больных выявляют множественные конкременты (нефролитиаз и нефрокальциноз).
Лечение направлено на коррекцию метаболического ацидоза, гипокалиемии с помощью бикарбоната натрия, препаратов калия, цитратных смесей, димефосфона. При явлениях остеопороза и остеомаляции показано назначение препаратов витамина D или его метаболитов (начальные суточные дозы витамина D 10 000‑20 000 ЕД, максимальные – 30 000‑60 000 ЕД; суточные дозы оксидевита 0,5–2 мкг), препаратов кальция до нормализации его уровня в крови. При оксалатно‑кальциевом нефролитиазе окись магния по 0,2–0,25 г в сутки курсами по 3–4 недели в течение длительного времени, 15 % раствор димефосфона в суточной дозе 1 мл на 5 кг массы тела, а также исключение из рациона продуктов, богатых оксалатами (щавель, шпинат, томатный сок, шоколад и др.). Лекарственную терапию проводят на фоне общеукрепляющего лечения с включением щелочных минеральных вод, фруктовых соков, ограничением белков животного происхождения, использованием комплекса витаминов (А, Е, группы В).
Спазмофилия (тетания)
Этиология. Заболевание, характеризующееся наклонностью ребенка первых 6‑18 мес. к судорогам и спастическим состояниям, патогенетически связанное с рахитом и снижением функции паращитовидных желез.
Болеют чаще дети от 6 мес. до 2,5 лет, страдающие рахитом. Спазмофилия возникает в связи с остро развившейся гипокальциемией на фоне электролитного дисбаланса и алкалоза, причиной которых является быстрое, почти внезапное увеличение количества активного метаболита витамина D в крови, что может наблюдаться при одномоментном приеме большой дозы витамина D2 или D3 («ударный» метод лечения), а также при длительном пребывании ребенка на весеннем солнце, особенно богатом ультрафиолетовыми лучами. Имеют значение также нарушение функций паращитовидных желез, снижение всасывания кальция в кишечнике или повышенное выделение его с мочой. Дополнительные причины развития судорожной готовности – снижение в крови уровня магния, натрия, хлоридов, витаминов В1 и В6. Наблюдается сезонность – в марте‑апреле у детей в первом или втором клиническом периоде рахита.
Снижение уровня ионизированного кальция в крови ведет к повышению нервно‑мышечной возбудимости.
Клиника. Различают явную и скрытую (латентную) формы спазмофилии.
Явная спазмофилия может проявляться в виде ларингоспазма, карпопедального спазма и эклампсии, иногда сочетающихся между собой.
Таблица 2
Дифференциальный диагноз рахитоподобных заболеваний
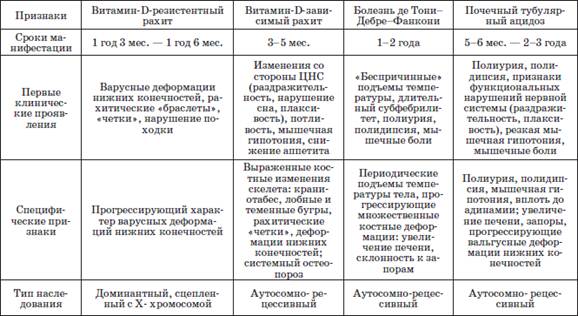
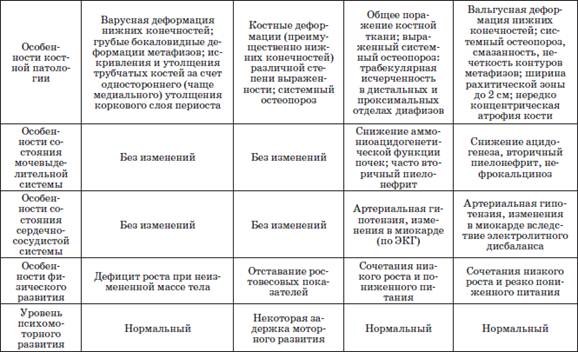
Ларингоспазм («родимчик») – спазм голосовой щели. Возникает внезапно при плаче или испуге. Он проявляется звучным или хриплым вдохом («петушиный крик») и остановкой дыхания на несколько секунд, при этом отмечаются испуганное выражение лица, цианоз, холодный пот, потеря сознания. Обычно приступ продолжается от нескольких секунд до 1–2 мин, заканчивается глубоким звучным вдохом, после которого ребенок почти всегда плачет, но уже через несколько минут приходит в нормальное состояние и часто засыпает.
Карпопедальный спазм наблюдается чаще у детей после года, проявляется в виде тонических судорог кистей, стоп, лица. Кисти принимают положение «руки акушера», стопы – положение резкого подошвенного сгибания. Спазм может продолжаться несколько минут, часов, дней. Нередко возникает спазм круговых мышц рта («рыбий рот»).
Редкой, но наиболее опасной формой спазмофилии является эклампсия, проявляющаяся клоническими судорогами, протекающими с потерей сознания. Во время приступа может произойти остановка дыхания и сердца. Чаще наблюдается у детей 1‑го года жизни.
При скрытой форме дети внешне практически здоровы, психомоторное развитие в пределах возрастных особенностей; почти всегда у них имеются симптомы рахита, чаще всего в периоде выздоровления. Скрытую форму спазмофилии можно диагностировать с помощью ряда симптомов: симптом Хвостека – при легком поколачивании щеки между скуловой дугой и углом рта на соответствующей стороне происходит сокращение мимической мускулатуры лица; симптом Труссо – при сдавливании на плече сосудисто‑нервного пучка кисть судорожно сокращается, принимая положение «рука акушера»; симптом Люста – поколачивание перкуссионным молоточком ниже головки малоберцовой кости вызывает быстрое отведение и подошвенное сгибание стопы.
Скрытая спазмофилия встречается часто и под влиянием провоцирующих факторов (плач, рвота, высокая температура, инфекционное заболевание, испуг) может переходить в явную.
Диагноз подтверждается наличием гипокальциемии в сочетании с гипофосфатемией, алкалозом в крови.
Лечение. При появлении явной тетании основными задачами являются немедленное прекращение судорог и лечение основного заболевания. При клонических судорогах вводят седуксен (0,5 % раствор – 0,1 мл/кг в/м), ГОМК (20 % раствор – 0,5 мл/кг), сульфат магния (25 % раствор – 0,2 мл/кг в/м); одновременно вводят 10 % раствор глюконата или хлорида кальция в/в. Ребенка госпитализируют после исчезновения судорог. Назначают 10 % раствор хлорида кальция по 1 чайной ложке или десертной ложке или глюконат кальция по 2–3 г 3–4 раза в день, а также 10 % раствор аммония хлорида (для создания ацидоза) по 1 чайной ложке 3 раза в день. Спустя 2–3 дня после судорог проводят противорахитическое лечение.
|
|
|
|
|
Дата добавления: 2014-11-25; Просмотров: 3606; Нарушение авторских прав?; Мы поможем в написании вашей работы!