
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Обучающие упражнения. Задание 1. Один из стереоизомеров 2-амино-3-гидроксибутановой кислоты (треонин) входит в состав белков
|
|
|
|
Задание 1. Один из стереоизомеров 2-амино-3-гидроксибутановой кислоты (треонин) входит в состав белков. Какие стереоизомеры возможны для треонина?
Ответ: в молекуле треонина два центра хиральности

Изобразим возможные стереоизомеры в виде проекционной формулы Фишера

| I | II | III | IV |
| L-алло-треонин | D-алло-треонин | D-треонин | L-треонин |
Для отнесения амино- и гидроксикислот к стереохимическим рядам, используется так называемый “гидроксильный ключ”, когда рассматривается конфигурация хирального центра с наименьшим номером.
По этому правилу стереоизомеры I и IV относятся к L ряду, а II и III к D-ряду. В состав белков входит L-треонин IV. Соединения I и II имеют эритроконфигурацию, т.е. заместители находятся в проекции Фишера по одну сторону углеродной цепи, в этом случае еще используется приставка алло-.
Заключение: I и II, III и IV - энантиомеры; I и III; I и IV; II и III; II и IV; диастереомеры.
Задание 2. На примере a-аланина и триптофана опишите схему образования биполярной структуры. Получите дипептиды образованные этими аминокислотами. Каковы особенности строения пептидной связи?
Ответ:

| катионная форма | биполярный ион | анионная форма |
В кислой среде a-аминокислоты существуют в виде катионной формы, в щелочной в виде анионной и в изоэлектрической точке в виде биполярного иона, т.е. одинаковое количество катионной и анионной форм.
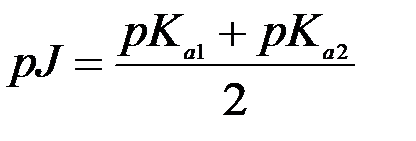 ,это формула для определения изоэлектрической точки
,это формула для определения изоэлектрической точки
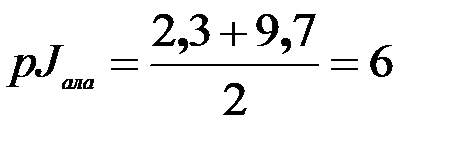

| катионная форма рКа1=2,4 | биполярный ион pJтри=5,9 | анионная форма рКа2=9,4 |
При взаимодействии триптофана и a-аланина могут образовываться четыре дипептида: Три-Ала, Ала-Три, Ала-Ала, Три-Три.

аланилтриптофан Ала-Три

аланилаланин Ала-Ала

триптофанилтриптофан Три-Три
|
|
|
|
|
Дата добавления: 2014-11-16; Просмотров: 700; Нарушение авторских прав?; Мы поможем в написании вашей работы!