
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Атом водорода в квантовой механике
|
|
|
|
ЭЛЕМЕНТЫ СОВРЕМЕННОЙ ФИ3ИКИ АТОМОВ И МОЛЕКУЛ
Решение задачи об энергетических уравнениях электрона для атома водорода (а также водородоподобных систем: иона гелия Не +, двукратно ионизированного лития Li++ и др.) сводится к задаче о движении электрона в кулоновском поле ядра.
Потенциальная энергия взаимодействия электрона с ядром, обладающим зарядом Ze (для атома водорода Z = 1),
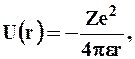
где r - расстояние между электроном и ядром. Графически функция U (r) изображена жирной кривой на рис. 38, неограниченно убывающей (возрастающей) по модулю при уменьшении r, т.е. при приближении электрона к ядру.
Состояние электрона в атоме водорода описывается волновой функцией 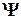 , удовлетворяющей стационарному уравнению Шредингера
, удовлетворяющей стационарному уравнению Шредингера
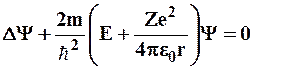 (9.1)
(9.1)
где m - масса электрона, Е - полная энергия электрона в атоме. Так как поле, в котором движется электрон, является центрально-симметричным; то для решения уравнения (9.1) обычно используют сферическую систему координат: 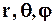 . Не вдаваясь в математическое решение этой задачи; ограничимся рассмотрением важнейших результатов; которые из него следуют; пояснив их физический смысл.
. Не вдаваясь в математическое решение этой задачи; ограничимся рассмотрением важнейших результатов; которые из него следуют; пояснив их физический смысл.
1. Энергия. В теории дифференциальных уравнений доказывается, что уравнения типа (9.1) имеют решения; удовлетворяющие требованиям однозначности; конечности и непрерывности волновой функции 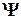 только при собственных значениях энергии
только при собственных значениях энергии
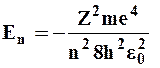 (n=1,2,3,…) (9.2)
(n=1,2,3,…) (9.2)
т.е. для дискретного набора отрицательных значений энергии.
Таким образом; решение уравнения Шредингера для атома водорода приводит к появлению дискретных энергетических уровней. Возможные значения Е1,Е2,Е3 показаны на рис. 38 в виде горизонтальных прямых.
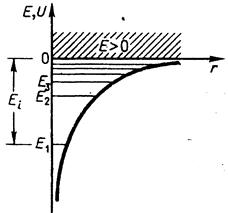
| Самый нижний уровень E1, отвечающий минимально возможной энергии, - основной. Все остальные 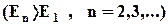 -возбужденные. При Е<0движение электрона является связанным - он находится внутри гиперболической "потенциальной ямы". По мере роста главного квантового числа n энергетические уровни располагаются теснее и при -возбужденные. При Е<0движение электрона является связанным - он находится внутри гиперболической "потенциальной ямы". По мере роста главного квантового числа n энергетические уровни располагаются теснее и при 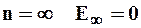 . .
|
Рис. 38
При Е>О движение электрона является свободным; область непрерывного спектра Е>О (на рис. 37 заштрихована) соответствует ионизированному атому. Энергия ионизации атома водорода равна
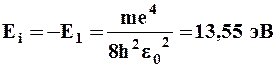 (9.3)
(9.3)
Выражение (9.3) совпадает с формулой (7.7), полученной Бором для энергии атома водорода. Однако если Бору пришлось вводить дополнительные гипотезы, то в квантовой механике дискретные значения энергии, являясь следствием самой теории, вытекают непосредственно из решения уравнения Шредингера.
2. Квантовые числа. В квантовой механике доказывается, что уравнению Шредингера (9.1) удовлетворяют собственные функции, 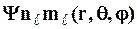 , определяемые тремя квантовыми числами: главным n, орбитальным
, определяемые тремя квантовыми числами: главным n, орбитальным 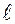 и магнитным
и магнитным 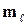 .
.
Главное квантовое число n, согласно (9.2), определяет энерге-тические уровни электрона в атоме и может принимать любые цело-численные значения начиная с единицы: n=1, 2, 3,
Из решения уравнения Шредингера вытекает, что момент импульса (механический орбитальный момент) электрона квантуется, т.е. не может быть произвольным, а принимает дискретные значения, опреде-ляемые формулой
 , (9.4)
, (9.4)
где 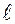 – орбитальное квантовое число, которое при заданном n принимает значения
– орбитальное квантовое число, которое при заданном n принимает значения
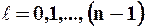 (9.5)
(9.5)
т.е. всего n значений, и определяет момент импульса электрона в атоме.
Из решения уравнений Шредингера следует также, что вектор 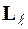 момента импульса электрона может иметь лишь такие ориентации в пространстве, при которых его проекция
момента импульса электрона может иметь лишь такие ориентации в пространстве, при которых его проекция 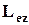 на направление z внешнего магнитного поля принимает квантовые значения кратные
на направление z внешнего магнитного поля принимает квантовые значения кратные 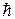
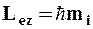 (9.6)
(9.6)
где  - магнитное квантовое число, которое может принимать значения =0,±1,±2,…,±
- магнитное квантовое число, которое может принимать значения =0,±1,±2,…,± 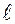 ,
,  - определяет проекцию момента импульса электрона на заданное направление, причем вектор момента импульса электрона в атоме может иметь в пространстве 2
- определяет проекцию момента импульса электрона на заданное направление, причем вектор момента импульса электрона в атоме может иметь в пространстве 2 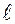 +
+ 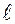 ориентаций. Наличие квантового числа
ориентаций. Наличие квантового числа  должно привести в магнитном поле к расщеплению уровня с главным квантовым числом n на 2
должно привести в магнитном поле к расщеплению уровня с главным квантовым числом n на 2 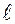 + 1 подуровней. Соответственно в спектре атома должно наблюдаться расщепление спектральных линий. Действительно, расщепление энергетических уровней в магнитном поле было обнаружено в 1896 г. голландским физиком П. Зееманом и получило название эффекта Зеемана. Расщепление уровней энергии во внешнем электрическом поле, тоже доказанное экспериментально, называется эффектом Штарка.
+ 1 подуровней. Соответственно в спектре атома должно наблюдаться расщепление спектральных линий. Действительно, расщепление энергетических уровней в магнитном поле было обнаружено в 1896 г. голландским физиком П. Зееманом и получило название эффекта Зеемана. Расщепление уровней энергии во внешнем электрическом поле, тоже доказанное экспериментально, называется эффектом Штарка.
Хотя энергия электрона (9.2) и зависит только от главного квантового числа n, но каждому собственному значению En (кроме Е1) соответствует несколько собственных функций  , отличающихся значениями
, отличающихся значениями  . Следовательно, атом водорода может иметь одно и то же значение энергии, находясь в нескольких различных состояниях. Так как при данном n орбитальное квантовое число
. Следовательно, атом водорода может иметь одно и то же значение энергии, находясь в нескольких различных состояниях. Так как при данном n орбитальное квантовое число 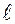 может изменяться от 0 до n- 1, а каждому значению
может изменяться от 0 до n- 1, а каждому значению 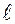 соответствует 2
соответствует 2 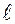 +
+ 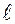 различных значений, то число различных состояний, соответствующих данному n, равно
различных значений, то число различных состояний, соответствующих данному n, равно 
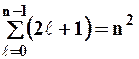 . (9.7)
. (9.7)
Квантовые числа и их значения являются следствием решений уравнений Шредингера и условий однозначности, непрерывности и конечности, налагаемых на волновую функцию 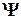 . Кроме того, поскольку при движении электрона в атоме существенны волновые свойства электрона, квантовая механика вообще отказывается от классического представления об электронных орбитах. Согласно учению, каждому энергетическому состоянию соответствует волновая функция, квадрат модуля которой определяет вероятность обнаружения электрона в единице объема, различную в разных частях атома. Электрон при своем движении как бы "размазан" по всему объему и образует электронное облако, плотность (густота) которого характеризует вероятность нахождения электрона в различных точках объема атома. Квантовые числа n и
. Кроме того, поскольку при движении электрона в атоме существенны волновые свойства электрона, квантовая механика вообще отказывается от классического представления об электронных орбитах. Согласно учению, каждому энергетическому состоянию соответствует волновая функция, квадрат модуля которой определяет вероятность обнаружения электрона в единице объема, различную в разных частях атома. Электрон при своем движении как бы "размазан" по всему объему и образует электронное облако, плотность (густота) которого характеризует вероятность нахождения электрона в различных точках объема атома. Квантовые числа n и 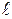 характеризуют размер и форму электронного облака, квантовое число
характеризуют размер и форму электронного облака, квантовое число  - ориентацию электронного облака в пространстве.
- ориентацию электронного облака в пространстве.
В атомной физике по аналогии со спектроскопией состояние электрона, характеризующееся квантовым числом 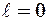 , называют s - состоянием (электрон в этом состоянии называют s - электроном),
, называют s - состоянием (электрон в этом состоянии называют s - электроном), 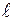 =1 - р – состоянием,
=1 - р – состоянием, 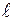 =2 - d - состоянием,
=2 - d - состоянием, 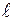 = 3 - f - состоянием и т. д. Значение главного квантового числа указывается перед условным обозначением орбитального квантового числа. Например, электроны в состояниях с n = 2 и
= 3 - f - состоянием и т. д. Значение главного квантового числа указывается перед условным обозначением орбитального квантового числа. Например, электроны в состояниях с n = 2 и 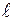 = 0 и
= 0 и 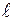 обозначаются соответственно символами 2s и 2р.
обозначаются соответственно символами 2s и 2р.

Рис. 39
На рис. 39 для примера приведено распределение электрон-ной плотности (в форме электронного облака) для состояний атома во-дорода при n = 1 и n = 2, определяемое 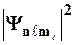 как видно из рисунка, оно зависит от n,
как видно из рисунка, оно зависит от n, 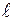 и
и  . Так при
. Так при 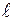 = 0 электронная плотность в центре отлична от нуля и не зависит от направления (сферически симметрична), а для остальных состояний в центре она равна нулю зависит от направления.
= 0 электронная плотность в центре отлична от нуля и не зависит от направления (сферически симметрична), а для остальных состояний в центре она равна нулю зависит от направления.
3. Спектр. Квантовые числа n, 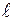 и
и  позволяют более полно описать спектр испускания (поглощения) атома водорода, полученный в теории Бора. В квантовой механике вводятся правила отбора, ограничивающее число возможных переходов электронов в атоме, связанных с испусканием и поглощением света.
позволяют более полно описать спектр испускания (поглощения) атома водорода, полученный в теории Бора. В квантовой механике вводятся правила отбора, ограничивающее число возможных переходов электронов в атоме, связанных с испусканием и поглощением света.
Теоретически доказано и экспериментально подтверждено, что для дипольного излучения электрона, движущегося в центрально - симметричном поле ядра, могут осуществляться только такие переходы, для ко-
торых: 1) изменение орбитального квантового числа 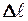 удовлетворяет условию
удовлетворяет условию
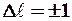 ; (9.7) 2) изменение магнитного квантового числа
; (9.7) 2) изменение магнитного квантового числа 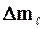 удовлетворяет условию
удовлетворяет условию
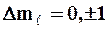 .
.

В оптических спектрах указанные правила отбора в основном выполняются. Однако в принципе могут наблюдаться и слабые, "запрещенные" линии, например возникающие при переходах с 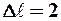 . Появление этих линий объясняется тем, что строгая теория, запрещая дипольные переходы, разрешает переходы, соответствующие излучению более сложных систем зарядов. Например, квадруполей. Вероятность же квадрупольных переходов (переходы с
. Появление этих линий объясняется тем, что строгая теория, запрещая дипольные переходы, разрешает переходы, соответствующие излучению более сложных систем зарядов. Например, квадруполей. Вероятность же квадрупольных переходов (переходы с 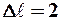 ) во много раз меньше вероятности дипольных переходов, поэтому "запрещенные" линии и являются слабыми. Учитывая число возможных состояний, соответствующих данному n, и правило отбора (9.8), рассмотрим спектральные линии атома водорода: серии Лаймана соответствуют переходы
) во много раз меньше вероятности дипольных переходов, поэтому "запрещенные" линии и являются слабыми. Учитывая число возможных состояний, соответствующих данному n, и правило отбора (9.8), рассмотрим спектральные линии атома водорода: серии Лаймана соответствуют переходы
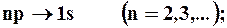
серии Бальмера -
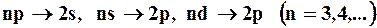 .
.
Переход электрона из основного состояния в возбужденное обусловлен увеличением энергии атома и может происходить только при сообщении атому энергии извне. Например, на счет поглощения атомом фотона. Так как поглощающий атом находится обычно в основном состоянии, то спектр атома водорода должен состоять из линий, соответствующих переходам 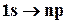 (n=2,3,...), что находится в полном согласии с опытом.
(n=2,3,...), что находится в полном согласии с опытом.
|
|
|
|
|
Дата добавления: 2014-11-16; Просмотров: 1364; Нарушение авторских прав?; Мы поможем в написании вашей работы!