
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Основные химические понятия. Химический элемент – вид атомов, характеризующихся одинаковым зарядом ядра
|
|
|
|
ОСНОВНЫЕ ПОНЯТИЯ И ЗАКОНЫ В ХИМИИ
Химический элемент – вид атомов, характеризующихся одинаковым зарядом ядра.
Атом – наименьшая частица элемента, обладающая его химическими свойствами и неделимая при химических реакциях.
Молекула – наименьшая частица вещества, обладающая его химическими свойствами.
Простое вещество – вещество, в состав которого входят атомы одного и того же элемента.
Сложное вещество – вещество, в состав которого входят атомы разных элементов.
Атомная единица массы (а. е. м.) – 1/12 массы атома углерода – 12(12с), т.е. 1,6666∙10-27 кг.
Относительная атомная масса элемента (Аr) – безразмерная величина, равная отношению средней массы атома естественного изотопического состава элемента и 1/12 массы углерода-12:
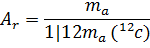
(подстрочная буква r – от лат. relativus относительный).
Относительная молекулярная масса (Mr) простого или сложного вещества – безразмерная величина, равная отношению средней массы естественного изотопического состава вещества к 1/12 массы атома углерода – 12.
Условная частица (УЧ) – любой вид реальных частиц (атомы, молекулы, ионы, электроны, атомные группы и т. д.) и условно существующие доли таких частиц (1/2 Ba2+, 1/3 H3PO4 и т. п.).
Моль – единица количества вещества или системы, содержащая столько определенных УЧ, сколько атомов содержится в углероде – 12 массой 0,012 кг, т. е. 6,02∙1023.
Постоянная Авогадро Na равна отношению числа частиц любой системы (N) к количеству вещества системы n: N/n=NAмоль-1=6,02∙1023 моль-1.
Молярная масса M(X) вещества, состоящего из частиц X, равна отношению m порции вещества к количеству вещества n(X) в этой порции:
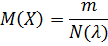
Единица молярной массы – кг∙моль-1 или г∙моль-1
Числовое значение молярной массы {M}; выраженной в г/моль, равно относительной молекулярной массе. Например, Ar(Na)= 23 и Mr(H2SO4)=98, следовательно, M(Na)=23 г/моль, а M(H2SO4)=98 г/моль.
Молярный объем Vm – отношение объема вещества к количеству вещества в этом объеме:
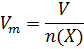
Единица измерения – м3/моль или л/моль.
При n(X)= 1 моль Vm = 22.4л или 22,4∙10-3 м3.
Масса атома (кг, г) – отношение молярной массы элемента к постоянной Авогадро. Так,
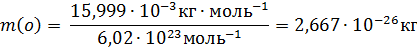
Масса атома равна также произведению относительной атомной массы на атомную единицу массы. Тогда m(0)=15,999∙1,6605∙10-27кг = 2,667∙10-26кг.
Масса молекулы (кг, г) – отношение молярной массы данного вещества к постоянной Авогадро. Так,
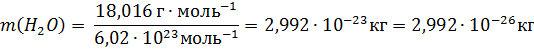
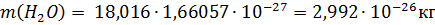
|
|
|
|
|
Дата добавления: 2014-11-16; Просмотров: 614; Нарушение авторских прав?; Мы поможем в написании вашей работы!