
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Инфаркт миокарда. Инфаркт миокарда (ИМ) — острое заболевание, обусловленное возникновением одного или нескольких очагов ишемического некроза в сердечной мышце в связи с
|
|
|
|
Инфаркт миокарда (ИМ) — острое заболевание, обусловленное возникновением одного или нескольких очагов ишемического некроза в сердечной мышце в связи с абсолютной или относительной недостаточностью коронарного кровотока.
У мужчин ИМ встречается чаще, чем у женщин, особенно в молодых возрастных группах. В группе больных в возрасте от 21 года до 50 лет это соотношение равняется 5:1, от 51 года до 60 лет — 2:1. В более поздние возрастные периоды эта разница исчезает за счет увеличения числа инфарктов у женщин. В последнее время значительно увеличилась заболеваемость ИМ лиц молодого возраста (мужчин до 40 лет).
Классификация. ИМ подразделяется с учетом величины и локализации некроза, характера течения заболевания.
• В зависимости от величины некроза различают крупноочаговый и мелкоочаговый инфаркт миокарда.
С учетом распространенности некроза в глубь мышцы сердца в настоящее время выделяют следующие формы ИМ:
♦ трансмуральный (включает как QS-, так и Q-инфаркт миокарда,
ранее называемый «крупноочаговым»);
♦ ИМ без зубца Q (изменения касаются лишь сегмента ST и зубца Г;
ранее называемый «мелкоочаговым») нетрансмуральный; как
правило, бывает субэндокардиальным.
• По локализации выделяют передний, верхушечный, боковой, сеп-
тальный, нижний (диафрагмальный), задний и нижнебазальный.
Возможны сочетанные поражения.
Указанные локализации относятся к левому желудочку как наиболее часто страдающему при ИМ. Инфаркт правого желудочка развивается крайне редко.
• В зависимости от характера течения выделяют ИМ с затяжным те
чением, рецидивирующий ИМ, повторный ИМ.
Затяжное течение характеризуется длительным (от нескольких дней до недели и более) периодом следующих один за другим болевых приступов, замедленными процессами репарации (затянувшимся обратным развитием изменений на ЭКГ и резорбционно-некротического синдрома).
Рецидивирующий ИМ — вариант болезни, при котором новые участки некроза возникают в сроки от 72 ч до 4 нед после развития ИМ, т.е. до окончания основных процессов рубцевания (появление новых очагов некроза в течение первых 72 ч — расширение зоны ИМ, а не рецидив его).
Развитие повторного ИМ не связано с первичным некрозом миокарда. Обычно повторный ИМ возникает в бассейнах других коронарных артерий в сроки, как правило, превышающие 28 дней от начала предыдущего инфаркта. Эти сроки установлены Международной классификацией болезней X пересмотра (ранее этот срок был указан как 8 нед).
Этиология. Основной причиной ИМ является атеросклероз коронарных артерий, осложненный тромбозом или кровоизлиянием в атероскле-ротическую бляшку (у умерших от ИМ атеросклероз коронарных артерий обнаруживается в 90 — 95 % случаев).
В последнее время существенное значение в возникновении ИМ придается функциональным нарушениям, приводящим к спазму коронарных артерий (не всегда патологически измененных) и острому несоответствию объема коронарного кровотока потребностям миокарда в кислороде и питательных веществах.
Редко причинами ИМ бывают эмболии коронарных артерий, тромбоз их при воспалительных поражениях (тромбангиит, ревматический корона-рит и т.д.), сдавление устья коронарных артерий расслаивающей аневризмой аорты и пр. Они приводят к развитию ИМ в 1 % случаев и не относятся к проявлениям ИБС.
Факторами, способствующими возникновению ИМ, являются:
1) недостаточность коллатеральных связей между коронарными сосу
дами и нарушение их функции;
2) усиление тромбообразующих свойств крови;
3) повышение потребности миокарда в кислороде;
4) нарушение микроциркуляции в миокарде.
Чаще всего ИМ локализуется в передней стенке левого желудочка, т.е. в бассейне кровоснабжения наиболее часто поражаемой атеросклеро-
|
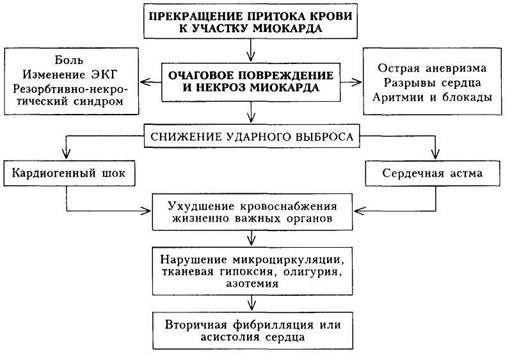
| Схема 13. Патогенез инфаркта миокарда и его осложнений |
зом передней нисходящей ветви левой коронарной артерии. Второе место по частоте занимает ИМ задней стенки левого желудочка; ИМ межжелудочковой перегородки составляет 25 % всех поражений.
Патогенез. В патогенезе ИМ ведущая роль принадлежит прекращению притока крови к участку сердечной мышцы, что приводит к повреждению миокарда, его некрозу, ухудшению жизнедеятельности периин-фарктной зоны (схема 13).
Некроз миокарда проявляется резорбционно-некротическим синдромом (данные лабораторных исследований, повышение температуры тела) подтверждается данными ЭКГ. Он вызывает длительный болевой синдром, может проявляться развитием аритмий и блокад сердца, а трансму-ральный некроз — разрывами сердца или острой аневризмой.
Некроз миокарда, нарушение состояния периинфарктной зоны способствуют снижению ударного и минутного объемов сердца. Клинически это проявляется развитием острой левожелудочковой недостаточности — отеком легких и(или) кардиогенным шоком. Последний сопровождается резким снижением кровоснабжения жизненно важных органов, что приводит к нарушению микроциркуляции, тканевой гипоксии и накоплению продуктов обмена.
Метаболические нарушения в миокарде служат причиной тяжелых нарушений ритма сердца, нередко заканчивающихся фибрилляцией желудочков.
Возникающее при кардиогенном шоке снижение коронарного кровотока еще больше способствует снижению насосной функции сердца и усу-
губляет течение кардиогенного шока, отека легких — главных причин смерти при ИМ.
Клиническая картина. Проявления ИМ определяются вариантом начала болезни, периодом течения и развитием тех или иных осложнений.
В течении ИМ выделяют ряд периодов.
Острейший период (I) — время между возникновением ишемии участка миокарда (так называемая ишемическая стадия) и появлением признаков его некроза (от 30 мин до 2 ч).
Острый период (II) — образуется участок некроза и миомаляции (продолжительность 10 дней; при затяжном и рецидивирующем течении дольше).
Подострый период (III) — завершаются начальные процессы организации рубца (с 10-го дня до конца 4 — 8-й недели от начала заболевания).
Постинфарктный (послеинфарктный) период (IV) характеризуется увеличением плотности рубца и максимально возможной адаптацией миокарда к новым условиям функционирования сердечно-сосудистой системы (продолжается 2 — 6 мес с момента образования рубца).
Выделяют продромальный период («предынфарктное состояние»), который характеризуется: а) стенокардией, впервые возникшей в течение ближайших 4 нед; б) увеличением частоты и усугублением тяжести приступов у больного со стабильной до того стенокардией; в) появлением стенокардии покоя у больного со стенокардией напряжения; г) так называемой вариантной стенокардией (см. «Хроническая ишемическая болезнь сердца»). Этот период может продолжаться от нескольких часов до месяца.
Типичная, или ангинозная, форма начала ИМ отличается интенсивным болевым синдромом с локализацией боли за грудиной, в области сердца, часто иррадиирующей в левую руку, плечо, лопатку, челюсть и т.д. Боль длительная, не купируется нитроглицерином, сопровождается холодным потом, страхом смерти.
Помимо типичной формы начала болезни, выделяют ряд других вариантов (форм):
1) астматический — начало болезни проявляется одышкой или уду
шьем;
2) гастралгический — боли в животе, чаще в подложечной области,
диспепсические расстройства;
3) аритмический — манифестация заболевания нарушениями ритма,
чаще желудочковой тахикардией;
4) церебральный — основными проявлениями служат неврологичес
кие расстройства, напоминает клиническую картину инсульта;
5) с атипичной локализацией боли (боль появляется в позвоночнике,
руке, плече, челюсти и т.д.; локализуется не только слева, но и справа);
6) «бессимптомный» — симптомы общего недомогания, немотивиро
ванной слабости, адинамия, особенно у пожилых, в подобных случаях не
находят правильного истолкования, если не снимают ЭКГ.
Астматический и гастралгический варианты встречаются наиболее часто.
Осложнения. В острейший период ИМ часто успевают развиться тяжелые нарушения сердечного ритма и острая недостаточность кровообращения, которые могут привести к летальному исходу (в этот период больному еще не оказывается интенсивная врачебная помощь).
В острый период возникают осложнения, большинство которых также может служить причиной смерти больных:
1) нарушения ритма и проводимости (пароксизмальная тахикардия,
атриовентрикулярная блокада, мерцание и трепетание предсердий, фиб
рилляция желудочков и другие менее грозные нарушения);
2) шок (рефлекторный, кардиогенный и аритмический);
3) сердечная астма, отек легких (проявление острой левожелудочко-
вой недостаточности);
4) острая аневризма сердца;
5) разрывы сердца (в том числе перфорация межжелудочковой пере
городки и разрыв сосочковых мышц);
6) тромбоэмболические осложнения (в большом и малом круге крово
обращения);
7) парез желудка и кишечника, эрозивный гастрит с желудочным
кровотечением, панкреатит.
Подострый период протекает более благоприятно, но и в его течении возможны осложнения:
1) тромбоэндокардит с тромбоэмболическим синдромом (чаще эмбо
лия мелких сосудов большого круга кровообращения);
2) пневмония;
3) постинфарктный синдром — синдром Дресслера, синдром перед
ней грудной стенки, синдром плеча. Постинфарктный синдром развивает
ся обычно на 2 —6-й неделе после ИМ, характеризуется перикардитом,
плевритом, пневмонитом; иногда в воспалительный процесс вовлекаются
синовиальные оболочки суставов. Одновременно все симптомы встречают
ся редко, чаще наблюдается сочетание перикардита с плевритом или пнев
монитом. Иногда каждый из этих симптомов может встречаться изолиро
ванно, затрудняя диагностику постинфарктного синдрома;
4) психические изменения (чаще неврозоподобные симптомы);
5) хроническая левожелудочковая сердечная недостаточность;
6) начало формирования хронической аневризмы сердца;
7) правожелудочковая недостаточность развивается редко. При ее на
личии следует думать о тромбоэмболии ветвей легочной артерии, разрыве
межжелудочковой перегородки и крайне редко об инфаркте правого
желудочка.
В постинфарктном периоде заканчивается формирование хронической аневризмы, могут оставаться проявления синдрома Дресслера и симптомы хронической сердечной недостаточности. Вновь могут возникнуть нарушения ритма сердца. В целом для этого периода развитие осложнений нехарактерно.
На I этапе диагностического поиска на основании клинической картины, характера ее развития, с учетом предшествующего анамнеза, возраста и пола больного можно: а) заподозрить развитие ИМ; 6) высказать предположения о клиническом варианте болезни; в) получить сведения о тех или иных осложнениях.
При наличии длительного приступа нестерпимых болей за грудиной и в области сердца с характерной иррадиацией, не купирующихся нитроглицерином, следует прежде всего предположить ИМ, особенно у мужчин старше 40 лет. Надо помнить, что такая симптоматика иногда мо-
жет быть обусловлена и другими причинами (неврит, плеврит, миозит и др.).
Остро возникший приступ удушья, особенно у лиц пожилого возраста, прежде всего наводит на мысль об астматическом варианте ИМ. Однако острая левожелудочковая недостаточность может быть проявлением иной болезни (аортальный или митральный порок сердца, гипертоническая болезнь). Сердечная астма и отек легких при соответствующей клинической картине ИМ могут быть не вариантом его начала, а осложнением.
Наличие резких болей в эпигастральной области, особенно у больных с хронической ИБС, позволяет заподозрить гастралгический вариант ИМ. Подобная клиническая картина может быть проявлением других заболеваний (обострение язвенной болезни, гастрита, холецистита, острого панкреатита; пищевое отравление, особенно при наличии симптомов желудочной диспепсии).
Жалобы больного на приступы сердцебиений или резкого урежения ритма, появление аритмий, обмороков могут указывать на начало ИМ или его осложнений. Кроме этого, нарушения ритма могут появиться и вне связи с ИМ и быть проявлением НЦД, миокардитического кардиосклероза, хронической ИБС и др.
Интенсивный болевой синдром с атипичной локализацией реже напоминает ИМ, но не исключает его, в связи с чем дальнейшее обследование больного обязательно.
Внезапное немотивированное развитие кардиогенного шока, когда больной заторможен, вял, сознание его спутано, также должно вызвать у врача подозрение на ИМ.
Все сведения, полученные на I этапе, должны оцениваться с учетом данных физикального и лабораторно-инструментального обследования. Иногда на этом этапе диагностического поиска можно не получить никакой информации, позволяющей поставить диагноз ИМ. Диагностический поиск ИМ, особенно у лиц пожилого и старческого возраста, нельзя прекращать.
На II этапе диагностического поиска можно получить сведения: а) косвенно указывающие на развитие ИМ (прямых признаков не существует); б) позволяющие выявить осложнения.
При соответствующем анамнезе такие симптомы, как повышение температуры тела, тахикардия, артериальная гипотензия, особенно развившаяся на фоне предшествующей гипертензии, глухость тонов сердца и кратковременно выслушиваемый шум трения перикарда, позволяют высказаться в пользу диагноза ИМ. Однако сами по себе эти симптомы непа-тогномоничны для ИМ и могут встречаться при ряде заболеваний (ревматизм, миокардит, перикардит и т.д.).
Физикальное исследование помогает выявить симптомы возможных осложнений.
Для кардиогенного шока характерны: холодная кожа серо-бледного цвета, покрытая липким потом (нарушение периферической циркуляции); олигоанурия (уменьшение мочеобразования); нитевидный пульс; уменьшение пульсового давления (менее 20 — 30 мм рт.ст.); снижение систолического давления (ниже 80 мм рт.ст.; непостоянный симптом).
Могут наблюдаться симптомы острой левожелудочковой недостаточности: одышка, ортопноэ, влажные хрипы в легких.
Тромбоэмболия легочной артерии проявляется одышкой, болями в груди, кровохарканьем, появлением цианоза.
Увеличенная печень, периферические отеки — симптомы недостаточности кровообращения в большом круге.
При физикальном обследовании представляется возможность обнаружить брадитахикардию, экстрасистолию, мерцательную аритмию, паро-ксизмальную тахикардию.
Диагностическое значение всех указанных осложнений невелико, так как они встречаются и при других заболеваниях. Лишь в сочетании с анамнезом и данными III этапа они значимы при постановке диагноза ИМ.
Большое диагностическое значение приобретает выявление острой аневризмы (патологическая пульсация в прекардиальной области), разрыва межжелудочковой перегородки (интенсивный систолический шум в нижней трети грудины с симптомами быстро нарастающей недостаточности кровообращения в малом и большом круге), разрыва или отрыва сосо-чковой мышцы (дующий систолический шум на верхушке сердца, иногда определяемый пальпаторно, в сочетании с нарастающим застоем в малом круге кровообращения).
III этап диагностического поиска позволяет: а) поставить окончательный диагноз ИМ; б) уточнить его локализацию и распространенность (степень поражения миокарда); в) подтвердить или выявить нарушения ритма и проводимости; г) выявить новые осложнения (аневризма сердца, очаговое поражение почек при тромбоэмболии).
Поставить окончательный диагноз ИМ можно на основании сочетания признаков резорбционно-некротического синдрома и данных ЭКГ.
Резорбционно-некротический синдром выявляется по результатам общеклинического и биохимического исследований крови: лейкоцитоз со сдвигом лейкоцитарной формулы влево и анэозинофилия (не всегда) с первых часов заболевания; увеличение СОЭ с 3 —5-го дня; повышение в крови активности ферментов — креатинфосфокиназы (КФК) и ее МВ-фракции (с первых часов, сохраняющееся 2 — 3 дня), аминотрансфераз (особенно аспарагиновой и в меньшей степени аланиновой с конца первых суток, нормализующееся к 3 —5-му дню), ЛДГ — лактатдегидрогеназы (общей) и ее первого и второго изоферментов, которое может держаться 10—14 дней.
В настоящее время при острой коронарной патологии наряду с прочно вошедшими в клиническую практику лабораторными методами, такими как исследование уровня КФК, ЛДГ-1, КФК-МБ, широко используют новые маркеры — тропонин Т, тропонин И и миоглобин.
Тропонин является белковым комплексом, регулирующим мышечное сокращение, и состоит из трех субъединиц — тропонин Т (ТнТ), тропонин Ц (ТнЦ) и тропонин И (ТнИ). В начале 90-х годов были разработаны иммунологические методы, позволяющие с помощью моноклональных антител различать тропонины Т и И кардиомиоцитов и других поперечнополосатых мышечных волокон. Считается, что ТнИ и ТнТ являются наиболее чувствительными и специфичными маркерами некроза сердечной мышцы. Их уровень повышается в крови уже через 2 — 3 ч после инфаркта миокарда, увеличивается в 300 — 400 раз по сравнению с нормой и сохраняется повышенным в течение 10—14 дней.
В последнее время появились данные о том, что уровень ТнТ может повышаться при ХПН и некоторых других патологических состояниях, в связи с чем большее предпочтение отдается ТнИ.
Миоглобин — хромопротеид, сходный по строению с гемоглобином, — пигментный белок мышечной ткани, обеспечивающий депонирование в ней кислорода, что особенно важно для сердечной мышцы. У здоровых людей уровень миоглобина в крови, определяемый радиоиммунным методом, не превышает 80 мкг/л, а с мочой за сутки выделяется 0,4 — 4 мкг. При травмировании и ишемии мышц миоглобин, обладая малой молекулярной массой, быстро выделяется в кровь, а затем поступает в мочу.
При ИМ содержание миоглобина в крови у большинства больных превышает 200 мкг/л через 4 ч после ангинозного приступа, а через б ч его уровень повышается у 100 % больных с впервые возникшим ИМ.
Определение гипермиоглобинемии — наиболее достоверный тест для исключения острого ИМ в ранние сроки.
Электрокардиография является методом, который позволяет уточнить диагноз ИМ, его локализацию, глубину и обширность поражения, фазу течения; подтвердить или выявить нарушения ритма и проводимости; высказать предположение о развитии аневризмы сердца.
В ишемическую стадию отмечаются подъем сегмента ST в так называемых «прямых» отведениях (в этих отведениях в последующем будет формироваться патологический зубец Q) и реципрокное снижение ST в отведениях, в которых изменений комплекса QRS не будет. В острую фазу в «прямых» отведениях при трансмуральном ИМ резко снижается (или полностью исчезает) зубец R и формируется комплекс QS. При меньшей глубине поражения некрозом стенки миокарда в «прямых» отведениях появляется патологический зубец Q (равный по амплитуде '/3 зубца R или более, длительностью 0,04 с и более). Последующая эволюция ЭКГ сводится к возвращению сегмента ST к изоэлектрической линии и формированию в «прямых» отведениях отрицательного («коронарного») зубца Т.
При нетрансмуральном инфаркте изменения ограничиваются небольшим смещением сегмента ST вверх или вниз и инверсией зубца Т.
Для инфаркта миокарда передней стенки (включая область верхушки) характерны изменения ЭКГ в отведениях I, II, aVL и Уз,4; для инфаркта нижней стенки — в отведениях II, III и aVF; для инфаркта боковой стенки — в отведениях I, aVL и У$,6, при поражениях области перегородки выявляют изменения в отведениях Vi^co-
ЭКГ не является информативной в случае предшествовавшей блокады левой ножки пучка Гиса и при инфаркте правого желудочка. На ЭКГ выявляются самые разнообразные нарушения ритма, встречающиеся при ИМ. По ЭКГ впервые узнают о нарушениях атриовентрикулярной проводимости и проводимости по ножкам пучка Гиса, определяют характер блокады и ее степень.
Признаком, позволяющим предположить аневризму, является так называемая застывшая ЭКГ — сохранение подъема сегмента ST в сочетании с комплексом QS в «прямых» отведениях, при этом может отмечаться «коронарный» зубец Т.
Ультразвуковой метод исследования позволяет выявить участок гипокинезии или акинезии, соответствующий зоне поражения, а также состояние сосочковых мышц и межжелудочковой перегородки, которые также могут поражаться при инфаркте миокарда.
При рентгеноскопии органов грудной клетки можно выявить анев-ризматическое выпячивание и участок парадоксальной пульсации.
Данные инструментальных исследований, проводимых в общепринятом порядке, позволяют выявить атеросклеротическое поражение аорты (при рентгенологическом исследовании органов грудной клетки) и сосудов нижних конечностей (по данным реографии). Эти симптомы являются косвенным доводом наличия атеросклеротического поражения коронарных артерий при ИМ.
На III этапе диагностического поиска могут быть впервые получены данные, свидетельствующие о тромбоэмболии мелких сосудов почки (гематурия, невысокая протеинурия).
В подавляющем большинстве случаев диагностический поиск на этом заканчивается и формулируется развернутый клинический диагноз. Иногда прибегают к специальным методам диагностики.
1. Визуализация ИМ с помощью радиоактивных изотопов. Этот
метод применяют, если затруднена диагностика ИМ при помощи ЭКГ, а
исследование активности ферментов сыворотки крови невозможно или
малоинформативно.
Пирофосфат, меченный технецием, начинает накапливаться в зоне некроза спустя 12 ч от начала заболевания, и очаг «свечения» определяется до 2 нед, а при обширных поражениях — 2 — 3 мес.
Реже используют 201Т1, который накапливается в хорошо кровоснаб-жаемых участках миокарда и не поступает в зону некроза.
2. Селективная коронарография применяется для решения вопроса о
возможности хирургического лечения (аортокоронарное шунтирование) в
остром периоде ИМ и для уточнения локализации тромба при попытке его
растворения местным введением фибринолитических средств.
Диагностика. Диагноз ИМ с достоверностью может быть поставлен с учетом трех основных синдромов.
• Характерный болевой синдром или его эквиваленты в сочетании с
такими физикальными данными, как шум трения перикарда, пуль
сация в прекардиальной области, снижение АД, появление наруше
ний ритма и острой сердечной недостаточности.
• Изменения на ЭКГ: признаки ИМ с характерной последующей ди
намикой.
• Признаки резорбционно-некротического синдрома: повышение тем
пературы тела; динамика общего анализа крови (лейкоцитоз и анэо-
зинофилия с последующим нарастанием СОЭ); гиперферментемия
(повышение активности КФК и МВ-фракции КФК, ЛДГ, ЛДГ-1 и
ГАсТ).
Формулировка развернутого клинического диагноза ИМ должна отражать: характер течения (рецидивирующий, с затяжным течением, повторный); глубину некроза; локализацию ИМ; дату возникновения ИМ; осложнения; фоновые заболевания — атеросклероз коронарных артерий и других сосудов (отсутствие атеросклероза коронарных артерий отмечается при соответствующих данных коронарографии); стадию гипертонической болезни (при ее наличии); стадию недостаточности кровообращения (при ее наличии).
Лечение. Лечебные мероприятия при ИМ складываются из системы организационных и терапевтических мероприятий.
Организационные мероприятия включают: 1) оказание врачами специализированной бригады скорой помощи «на месте» высококвалифици-
8 - 540 "J
рованного лечения; 2) возможно раннюю госпитализацию больного; 3) наблюдение за больным в острый период в палате интенсивной терапии; 4) систему восстановительного лечения (реабилитация).
Терапевтические мероприятия проводятся с учетом стадии ИМ, выраженности и характера осложнений.
Лекарственная терапия (режим, диета, ЛФК) назначается индивидуально в зависимости от состояния и тяжести течения ИМ.
Основными направлениями лекарственной терапии острого периода ИМ являются:
• купирование боли;
• ранний тромболизис;
• антикоагулянты и ацетилсалициловая кислота;
• разгрузка миокарда;
• предупреждение опасных аритмий сердца;
• лечение осложнений.
♦ Купирование болевого синдрома наиболее эффективно осущест
вляют с помощью нейролептаналгезии: сочетание нейролептичес
ких средств (1 —2 мл 0,25 % раствора дроперидола) с обезболива
ющими (1—2 мл 0,005 % раствора фентанила) внутривенно или
внутримышечно. Кроме того, используется наркоз закисью азота
с кислородом, при необходимости наркотические анальгетики
(морфин, омнопон, промедол).
Обезболивающий эффект оказывают гепарин и тромболитические средства, вводимые в это же время.
♦ Тромболитическую терапию, направленную на реперфузию зоны
некроза миокарда, следует начинать как можно раньше и не позд
нее 12 ч с момента его развития, так как спустя 12 ч после появле
ния первых признаков острого ИМ нет оснований рассчитывать
на успешную реперфузию миокарда. Ее проводят только при от
сутствии абсолютных противопоказаний: инсульт, желудочно-ки
шечные кровотечения, склонность к кровотечениям, расслаиваю
щая аневризма аорты или хирургическая операция в течение
предшествующих 3 нед.
В качестве тромболитических средств в настоящее время применяют стрептокиназу, урокиназу или тканевый активатор плазминогена.
Внутривенную инфузию стрептокиназы осуществляют в дозе 1 500 000 ME в течение 30 — 40 мин. Препарат разводят в изотоническом растворе хлорида натрия до объема 100 мл; инфузию осуществляют в два этапа: сначала первые 250 000 ME (50 мл) вводят внутривенно капельно в течение 10 мин, а затем после 15-минутного перерыва вводят остальные 1 250 000 ME (50 мл) также в течение 10 мин.
Непосредственно перед началом инфузии стрептокиназы и сразу же после ее окончания следует ввести внутривенно струйно по 100 мг гидрокортизона или 60 — 90 мг преднизолона.
При лечении стрептокиназой гепарин или не назначают, или вводят подкожно по 12 500 ЕД 2 раза в сутки.
При наличии противопоказаний к применению тромболитической терапии в первые часы острого ИМ иногда для ликвидации окклюзии коронарной артерии в специализированных условиях (в лаборатории по коро-
нарной катетеризации) проводят чрескожную транслюминальную коронарную ангиопластику (ЧТКА). К этой процедуре прибегают и при отсутствии эффекта от тромболитической терапии.
♦ Ацетилсалициловую кислоту в качестве антиагреганта назначают
больному с первого дня заболевания. Первую дозу (160 — 325 мг)
дают в таблетках для разжевывания; затем в дозе 80—125 мг боль
ной принимает внутрь один раз в сутки очень длительно.
При невозможности проведения тромболитической терапии больному проводят антитромботическую (антикоагулянтную) терапию гепарином. Гепарин вводят внутривенно в течение 24 —48 ч в средней дозе 1000 ЕД/ч под контролем АЧТВ. Далее гепарин вводят в течение 3 — 4 сут (при затяжном течении, тромбоэмболиях — до 7 сут) каждые 6 ч под контролем свертываемости крови.
Антикоагулянтная терапия осуществляется для предупреждения: а) прогрессирования тромбоза в коронарных артериях; 6) внутрисердеч-ного тромбоза; в) системной эмболии; г) развития венозного тромбоза.
Проведение антикоагулянтной и тромболитической терапии рассчитано и на улучшение микроциркуляции («ограничение» очага поражения) в периинфарктной зоне, от состояния которой во многом зависит течение инфаркта в первые сутки.
♦ При ИМ с Q-зубцом больным показано раннее (в первые сутки) на
значение 1 % раствора нитроглицерина внутривенно капельно из
расчета 5 — 7 мкг/кг массы тела в час под контролем АД.
Для разгрузки миокарда, помимо нитроглицерина, назначают р-адре-ноблокаторы и ингибиторы АПФ.
(З-Адреноблокаторы назначают внутрь в первые сутки ИМ в случае развития тахикардии (в отсутствие сердечной недостаточности), при относительно повышенном АД или для купирования болевого синдрома, когда неэффективны наркотические (опиоидные) анальгетики.
На 2 —4-й день заболевания добавляют ингибиторы АПФ (капто-прил, эналаприл, рамиприл, периндоприл). Установлено, что они оказываются особенно эффективными, если у больных с острым ИМ имелось снижение фракции выброса или были признаки сердечной недостаточности в ранней фазе заболевания. Назначение ингибиторов АПФ показано всем больным, перенесшим ранее ИМ.
В лечении больных острым ИМ без зубца Q применяется, как правило, терапия гепарином, нитратами и (З-адреноблокаторами.
♦ Комплексная ранняя лекарственная терапия острого ИМ способст
вует предупреждению развития опасных аритмий сердца. Профи
лактическое назначение лидокаина больным острым ИМ в настоя
щее время не осуществляется.
♦ Лечение осложнений определяется их характером и выраженнос
тью.
Лечение кардиогенного шока проводят с учетом формы шока и гемодинамических параметров.
А. Рефлекторная форма шока. При данной форме кардиогенного шока применяют: а) обезболивание; б) прессорные препараты; в) плазмо-замещающие растворы.
При сохранении артериальной гипотензии и купировании болевого синдрома внутривенно вводят 0,5—1,0 мл 1 % раствора мезатона; при недостаточном эффекте производят внутривенную инфузию раствора допа-мина.
С целью увеличения венозного притока к сердцу иногда внутривенно вводят плазмозамещающие растворы, чаще реополиглюкин (низкомолекулярный декстран).
Б. Истинный кардиогенный шок. Данное осложнение ИМ в 50 % случаев заканчивается летально. Относительно оптимистические перспективы открываются при своевременном восстановлении коронарного кровотока с помощью тромболитиков или так называемых механических методов лечения (транслюминальная ангиопластика или аортокоронарное шунтирование). Развитие его зависит в конечном итоге от размеров зоны поражения. Среди методов лечения наиболее эффективны следующие:
1) применение периферических вазодилататоров в сочетании с допа-
мином;
2) нормализация кислотно-основного состояния;
3) использование низкомолекулярного декстрана (реополиглюкин).
Периферические вазодилататоры обеспечивают гемодинамическую разгрузку миокарда (уменьшают работу сердца, снижают потребность миокарда в кислороде), способствуют улучшению коронарной циркуляции. Применение допамина призвано улучшить насосную функцию сердца за счет влияния на контрактильный статус уцелевшего миокарда. Допамин вводят внутривенно капельно со скоростью 0,1 — 1,5 мкг/мин. Препарат не вызывает снижения общего периферического сопротивления (ОПС), но может уменьшать тонус коронарных, мозговых и печеночных артерий, повышая его в то же время в сосудах скелетных мышц.
Методы, применяемые с целью коррекции кислотно-основного состояния (внутривенное введение гидрокарбоната натрия), так же как и направленные на улучшение реологических свойств крови и микроциркуляции (тромболитическая, антикоагулянтная, антиагрегантная терапия, ок-сигенотерапия), занимают видное место в терапии шока. Однако они влияют на вторичные механизмы патогенеза и не могут ликвидировать шок до тех пор, пока не решена основная задача — восстановление насосной функции сердца.
Таким патогенетически обоснованным методом лечения истинного кардиогенного шока является контрпульсация. Контрпульсация — один из методов вспомогательного кровообращения, суть которого заключается в том, что в период систолы уменьшается давление в аорте и снижается сопротивление выбросу крови из желудочка (одновременно снижается и потребность миокарда в кислороде). В период диастолы, когда коронарный кровоток максимален, давление в аорте резко увеличивается за счет работы аппарата, который синхронизирован с работой сердца. С помощью такого метода удается значительно улучшить гемодинамику у многих больных шоком.
Лечение при кардиогенном шоке проводят с учетом гемодинамичес-ких параметров. Несмотря на то что истинное представление о них можно получить, лишь определяя сердечный индекс (СИ), конечное диастоли-ческое давление (КДД) и давление заклинивания в легочной артерии (эти исследования проводятся только в специализированных стационарах), су-
ществуют клинические симптомы, косвенно отражающие состояние гемодинамики.
а) Гиповолемический вариант кардиогенного шока (встречается
редко): резкое снижение АД, серый цианоз, тахикардия, СИ менее
2,2 л/минм2, диастолическое давление в легочной артерии снижено
(менее 10 мм рт.ст.).
Основные лечебные мероприятия: внутривенное капельное введение реополиглюкина со скоростью не менее 20 мл/мин в сочетании с допамином (50 мг в 400 мл 0,5 % раствора глюкозы с частотой 15 капель в минуту). Введение глюкозы и реополиглюкина способствует увеличению давления наполнения левого желудочка и росту сердечного выброса, что приводит к нормализации АД и исчезновению периферических симптомов шока.
б) Гиподинамический вариант кардиогенного шока: клинически про
является сочетанием кардиогенного шока с отеком легких, сопровождаю
щимся выраженной одышкой и влажными хрипами; диастолическое дав
ление в легочной артерии более 25 мм рт.ст., СИ снижен.
Основные лечебные мероприятия: внутривенное капельное введение 1 % раствора нитроглицерина или другого периферического вазодилатато-ра нитропруссида натрия — 50 мг в 500 мл 5 % раствора глюкозы [0,5 — 1 мкг/(кгмин)] и 90 мг фуросемида; при отсутствии эффекта показано дополнительное внутривенное капельное введение допамина — 50 мг в 400 мл 5 % раствора глюкозы с частотой 15 капель в минуту.
в) Застойный вариант кардиогенного шока: конечное диастолическое
давление и давление заклинивания в легочной артерии существенно по
вышены, но СИ не изменен; в этой ситуации показано введение фуросеми
да и внутривенное капельное введение 1 % раствора нитроглицерина (пе
риферический венозный дилататор, способствующий уменьшению притока
крови к сердцу и снижению повышенного давления в малом круге крово
обращения).
В. Аритмический шок. При данном шоке показаны: а) антиаритмические препараты; б) электроимпульсная терапия; в) электростимуляция сердца.
Лечение нарушений ритма и проводимости определяется видом нарушений и их влиянием на гемодинамику.
При желудочковой экстрасистолии вводят лидокаин: 100—150 мг внутривенно струйно. Если после первых суток эффекта от введения ли-докаина нет, то переходят на использование амиодарона (кордарона): вначале внутривенно вводят 600 — 800 мг и сразу же назначают внутрь 600 мг ежедневно.
При наджелудочковой пароксизмальной тахикардии внутривенно вводят 10 мг верапамила (изоптина) в течение 5—10 мин во избежание падения АД.
При мерцательной аритмии у больных инфарктом миокарда, за исключением тех случаев, когда мерцание предсердий создает угрозу жизни (в таких случаях сразу проводится электроимпульсная терапия), лечение рекомендуется начинать с введения сердечных гликозидов.
Если лекарственные средства неэффективны, то при наджелудочковой и желудочковой тахикардии, а также при трепетании и мерцании предсердий проводят электроимпульсную терапию (дефибрилляция). Электрическая дефибрилляция (кардиоверсия) является единственным эффективным методом лечения фибрилляции желудочков сердца.
Лечение отека легких заключается в уменьшении притока крови к сердцу, что способствует быстрому снижению давления в сосудах малого круга; с этой целью применяют периферические вазодилататоры (нитропруссид натрия) и мочегонные средства (фуросемид). Используют также нейролептаналгезию (фентанил и дроперидол).
Лечение тромбоэмболии крупных периферических сосудов осуществляют как с помощью лекарственных препаратов, так и хирургическим путем.
При неосложненном течении ИМ проводится активизация больного, включая ЛФК с первых дней, когда полностью купируется ангинозный статус. К концу 1-й недели больной под контролем методиста ЛФК садится на кровати, на 10— 11-й день ему разрешают сидеть и ходить до туалета, к концу 2-й недели больной совершает прогулки по коридору на 100 — 200 м в 2 —3 приема, а к концу 3-й недели — длительные прогулки, осваивает пролет лестницы. Активизация больного с осложненным ИМ проводится в индивидуально устанавливаемые сроки.
В подостром периоде ИМ продолжают терапию ацетилсалициловой кислотой, назначают коронароактивные препараты, подобранные индивидуально и включающие пролонгированные нитраты, блокато-ры кальциевых каналов, р-блокаторы и др.
При развитии иных осложнений (пневмония, сердечная недостаточность) проводят соответствующую их клинической картине терапию (антибиотики, сердечные гликозиды, мочегонные средства).
В терапии постинфарктного синдрома Дресслера используют неспецифические противовоспалительные средства (бутадион, реопирин и др.), небольшие дозы кортикостероидов, начиная с 15 — 20 мг преднизолона и затем постепенно снижая дозу.
Симптоматическое лечение седативными, снотворными, слабительными средствами проводится по показаниям; дозы препаратов подбирают индивидуально. В комплексном лечении больных ИМ, особенно в подостром и постинфарктном периодах, важно проведение восстановительной терапии — реабилитации больных (ЛФК, гимнастика) как физической, так и психологической. Реабилитационные мероприятия в дальнейшем проводятся в санаторно-курортных условиях или в специализированных реабилитационных отделениях.
Прогноз. Прогноз заболевания серьезный, ухудшается с развитием осложнений.
Профилактика. Устраняют так называемые факторы риска ИБС, особенно у лиц, в семьях которых есть случаи раннего атеросклероза.
Рекомендуют диету с низким содержанием насыщенных жиров, но обогащенную фруктами и овощами; необходимым условием является отказ от курения.
|
|
|
|
|
Дата добавления: 2014-11-20; Просмотров: 2804; Нарушение авторских прав?; Мы поможем в написании вашей работы!