
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Всероссийская олимпиада школьников по химии
|
|
|
|
Класс (Ответы)
Уч. год
Школьный этап
Всероссийская олимпиада школьников по химии
Класс
Уч. год
Школьный этап
1. Смесь сульфата бария и сульфита бария общей массой 70,0 г обработали избытком соляной кислоты. Выделился газ, при пропускании которого через избыток известковой воды образовалось 24,0 г осадка. Рассчитайте массовые доли веществ в исходной смеси. (10 баллов)
2. Расставить коэффициенты в уравнении реакции, назвать окислитель и восстановитель:
K2Cr2O7 + … + … 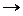 I2 + Cr2(SO4)3 + … + H2O
I2 + Cr2(SO4)3 + … + H2O
(5 баллов)
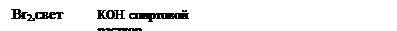 | |||||
|
| ||||

|



 3. бутадиен -1,3 Х1 2- метлпропан Х2 Х3 ацетон
3. бутадиен -1,3 Х1 2- метлпропан Х2 Х3 ацетон
(5 баллов)
Департамент образования администрации г. Арзамаса
1. Ответ:
2 NН3 + 6 КМnО4 + 6 КОН = N2 + 6 Н2О + 6 К2МnО4
восстановитель 2N -3 -6е = N2 1
окислитель Мn+7 +1е = Мn+6 6
2. Ответ: АlН4 - =17 протонов,18 электронов
NF3 =34 протона,34 электрона
3. К раствору гидрокарбоната натрия объемом 220,6 мл, плотность 1,12 г/мл с массовой долей 8,5% добавили избыток раствора соляной кислоты, определите объем углекислого газа, который выделился в результате реакции
(10 баллов)
NaHCO3 + HCl = NaCl + CO2 + H2O
1. m р-а = V*r =220,6* 1,12 =247,072 г
2. mр.в .=. m р-а*ω =247,072 * 0,085 =21 г
3. n (NaHCO3 ) = m /M =21 /84 =0,25 моль
4. 1:1 n(CO2) = 0,25 моль
5. V = n·Vm = 0,25 * 22,4 =5,6 л
Департамент образования администрации г. Арзамаса
|
|
|
|
|
Дата добавления: 2014-12-10; Просмотров: 638; Нарушение авторских прав?; Мы поможем в написании вашей работы!