
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Для чего нужна сульфатная( серная) кислота?
|
|
|
|
Не очень часто нам приходится иметь дело непосредственно с серной кислотой. Может показаться, что не так уж она нам и нужна. А между тем трудно найти другой продукт, который был бы так важен, как серная кислота.
Посмотрим повнимательнее вокруг. Предмет первой необходимости для нас – растительная пища: хлеб, овощи, крупа и т.п. Удовлетворить эту насущную потребность можно при хорошем урожае. Получить же такой урожай возможно при помощи минеральных удобрений. На их изготовление тратится около половины всей серной кислоты, получаемой на химических заводах. Без нее мы не могли бы получать питательные вещества в достаточной мере.
Наша одежда, белье сделаны из хлопчатобумажной, шерстяной или льняной ткани. Хлопок, лен, идущие на изготовление соответствующей ткани, тоже нуждаются в удобрениях, получаемых при помощи серной кислоты.
Кроме того, ткань требует после выхода с ткацкой машины последующей обработки – аппретуры, только тогда она получает свой настоящий вид. Аппретурная обработка производится особой массой, состоящей из сульфатов алюминия и бария, получаемых при помощи серной кислоты.
Чтобы окрасить шерстяную или хлопчатобумажную ткань, требуется протравливание, т.е. пропитка ткани такими солями, главным образом сульфатами, которые прочно соединяются как с самой тканью, так и с красителями, благодаря чему окрашенная ткань не линяет при стирке. Эти соли без серной кислоты изготовить, конечно, невозможно. Сами красители тоже не могут быть изготовлены без серной кислоты.
Мы носим кожаную обувь. Для получения ее из сырых шкур требуется освобождение их от волоса, смягчение, дубление, окраска. Все эти операции не могут обойтись без серной кислоты и ряда ее солей, например квасцов, изготовляемых при ее помощи.
|
|
|
Современное человеческое общество никоим образом без серной кислоты обойтись не может. Оказывается, помыться, быть чистым тоже нельзя без косвенного участия серной кислоты. Мы моемся мылом, стирка белья без мыла или стирального порошка невозможна. Мыло и порошки готовят из соды и жирных кислот. Чтобы получить жирные кислоты из жиров и очистить их, нужна серная кислота.
Вы читаете книгу, напечатанную на проклеенной бумаге, пишете на такой бумаге. Проклейка бумаги производится при помощи сульфата алюминия, т.е. опять при участии серной кислоты. Чернила готовили при помощи железного купороса, получаемого обработкой серной кислоты железом. Значит, и распространение культуры немыслимо без применения серной кислоты.
Ни один двигатель, ни одна машина, ни один станок не может работать без смазочных масел, керосина и других продуктов, получаемых из нефти, очистка которой производится при помощи серной кислоты. Значит, работа наших фабрик, заводов, движение поездов, пароходов, полет самолетов находятся в зависимости от нее.
Лужение, никелирование, серебрение, меднение проводятся при помощи сульфатов. Очистка некоторых металлов (серебра, меди и др.) проходит также при участии серной кислоты.
Для производства кислот, например уксусной, солей, неорганических и органических красок требуется серная кислота. Фармацевтическая отрасль промышленности, производство искусственного волокна не могут обойтись без серной кислоты. Взрывчатые вещества готовятся при участии концентрированной серной кислоты.
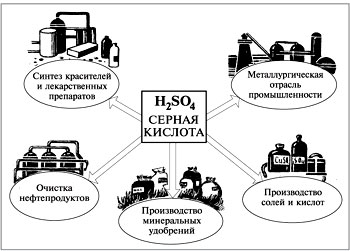
|
| Некоторые области применения сульфатной кислоты |
Получение: основным методом производства серной кислоты из SO3 является контактный метод. Вначале получают диоксид серы SO2 (сжигание серы и др.). Самый распространенный способ получения – обжиг серного колчедана FeS2, затем диоксид серы SO2 окисляют в триоксид серы SO3 контактным методом. Полученный три-оксид серы SO3 направляют на стадию поглощения, которую проводят концентрированной серной кислотой. Раствор SO3 в H2SO4 называется олеум. Контактным методом получают 92,5 %-ную серную кислоту. При нитрозном методе H2SO4 получают, окисляя SO2 в сернокислотном растворе, для этого в качестве катализатора используют смесь оксидов азота NO и NO2. Нитрозным методом получают 75 %-ную серную кислоту.
|
|
|
Чтобы приготовить раствор серной кислоты, ее необходимо выливать в воду тонкой струйкой, сильно перемешивая, при этом в воде образуются гидраты и происходит выделение теплоты.
Физические свойства: Серная кислота – бесцветная вязкая жидкость, имеющая температуру плавления 10 °C, температура кипения 296 °C (с разложением на H2O и SO3). Серная кислота – сильная кислота. Концентрированная серная кислота в большом количестве поглощает пары воды, поэтому ее используют для осушения газов.
Химические свойства.
1. Концентрированная серная кислота является сильным окислителем. Окислительно-восстановительные реакции требуют нагревания, а продуктом реакции в основном является SO2.
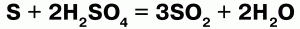
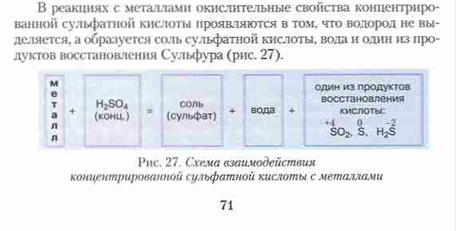
2. С металлами вступает в реакцию по-разному в зависимости от концентрации. Разбавленная серная кислота взаимодействует со всеми металлами, стоящими в ряду напряжений до водорода. Концентрированная серная кислота окисляет все металлы, стоящие в ряду напряжений, и серебро в том числе.
3. Разбавленная серная кислота взаимодействует с основаниями, основными и амфотерными оксидами, солями.
Серная кислота образует два вида солей: средние (сульфаты) и кислые (гидросульфаты).

Для выявления сульфатов и гидросульфатов (солей сульфатной кислоты) используют раствор барий хлорида BaCL2 или барий нитрата Ba(NO3)2, которые с сульфатной кислотой и ее солями образуют белый осадок нерастворимый в кислотах—барий сульфат BaSO4.
Сокращенное ионное уравнение такой реакции:
Ba2+ + SO4 2- = BaSO4.



Для более подробного изучения темы изучите параграф 9 учебника, после чего в рабочей тетради выполните упр.81, 82, 84.
Литература:
П.П.Попель, Л.С.Крикля. Химия 10класс. Киев, «Академия».2010
Выполненную работу присылайте по адресу [email protected]
|
|
|
Или приходите по возможности на консультацию в любой день недели с 9до 12час.
Видеоуроки по предметам http://interneturok.ru/ua помогут вам лучше усвоить материал.
Учиться самостоятельно кажется вам тяжелой необходимостью? Люди, ориентированные на успех своих жизненных начинаний, называют подобные обстоятельства возможностью. Умный человек не боится никакой работы, он делает ее, получает опыт и стремится к чему-то большему.
|
|
|
|
Дата добавления: 2014-12-16; Просмотров: 2313; Нарушение авторских прав?; Мы поможем в написании вашей работы!