
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Математические модели процесса получения хлорноватистой кислоты
|
|
|
|
Проведенные исследования математической модели на устойчивость поливинилхлорида данной марки показали, что положение равновесия системы асимптотически устойчиво.
Полученные результаты кроме теоретического значения имеют и практический характер, так как с их помощью можно более качественно вести технологический процесс полимеризации винилхлорида.
Используя методологию амбивалентных систем, как систем с противоположностями, были получены различные математические модели процесса получения хлорноватистой кислоты. В качестве примера приведем математическую модель процесса получения хлорноватистой кислоты в кислой среде.
Уравнение скорости реакции имеет вид:
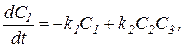
где 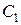 - концентрация хлора,
- концентрация хлора, 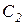 - концентрация хлорноватистой кислоты,
- концентрация хлорноватистой кислоты, 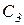 - концентрация соляной кислоты,
- концентрация соляной кислоты, 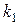 - константа скорости прямой реакции,
- константа скорости прямой реакции, 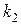 - константа скорости обратной реакции.
- константа скорости обратной реакции.
Так как в любой момент времени хлорноватистая и соляная кислоты образуются в равных концентрациях, то уравнение можно записать в виде:
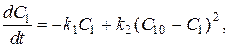
где 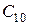 - начальная концентрация хлора.
- начальная концентрация хлора.
В положении равновесия, когда производная равна нулю, выполняется соотношение:
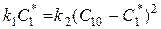 .
.
Сдвинуть равновесие вправо в направлении образования HOCl можно, выводя из реакции любое из веществ в правой части уравнения. Большинство действующих в промышленности производств получают хлорноватистую кислоту нужной концентрации, связывая соляную кислоту. Добиться этого проще всего прибавлением к реакционной смеси какой-нибудь щелочи. Применяя, например, NaOH, имеем:
HCl + NaOH = NaCl + H2O.
Процесс получения хлорноватистой кислоты описывается системой четырех нелинейных дифференциальных уравнений первого порядка:
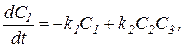
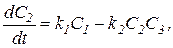

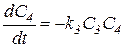 .
.
В этих обозначениях 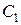 - концентрация хлора,
- концентрация хлора, 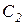 - концентрация хлорноватистой кислоты,
- концентрация хлорноватистой кислоты, 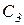 - концентрация соляной кислоты,
- концентрация соляной кислоты, 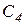 - концентрация щелочи,
- концентрация щелочи, 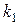 и
и 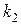 - константы скоростей прямой и обратной реакций в формуле (1),
- константы скоростей прямой и обратной реакций в формуле (1), 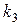 - константа скорости реакции.
- константа скорости реакции.
Константы скоростей отличаются друг от друга на несколько порядков:
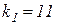 ,
,  ,
, 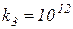 .
.
Как видно из значений констант скоростей система имеет несколько масштабов времени. Для изучения таких разномасштабных систем широко применяется метод квазистационарных концентраций, который предполагает разделение переменных на два класса: быстрые и медленные и позволяет понизить порядок системы.
Используя принцип выявления противоречия, можно считать, что быстрые и медленные реакции – это и есть противоположности, которые умещаются в одной системе.
Разделим третье и четвертое уравнения системы на больший параметр 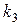 и введем обозначения:
и введем обозначения: 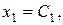
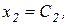

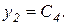
В результате получим систему уравнений с малым параметром при производных:
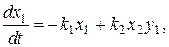
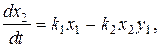
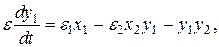
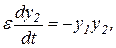
где 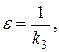
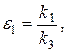
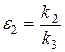 .
.
Таким образом, система разбилась на две подсистемы. Первые два уравнения системы описывают изменение медленных переменных 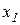 и
и 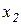 , а вторые два уравнения описывают изменение быстрых переменных
, а вторые два уравнения описывают изменение быстрых переменных 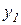 и
и 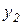 .
.
|
|
|
|
|
Дата добавления: 2014-12-16; Просмотров: 479; Нарушение авторских прав?; Мы поможем в написании вашей работы!