
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Белки молока
|
|
|
|
Общее содержание белков в молоке колеблется от 2,9 до 4,0 %, они разнообразны по строению, физико-химическим свойствам и биологическим функциям. Среди белков молока выделяют две главные группы: казеин (78-85%) и сывороточные белки.
Таблица 3
Классификация белков молока
| Белок | Содержание в % от общего количества белков обезжиренного молока | Молекулярная масса | Изоэлектрическая точка, рН. |
| Казеины | 78-85 | ||
| Альфа – казеины | 45-55 | 22000-24000 | 4,1 |
| Каппа - казеины | 8-15 | 4,1 | |
| Бета – казеины | 25-35 | 4,5 | |
| Гамма – казеины Сывороточные белки | 3-7 15-22 | 12000-21000 | 5,8-6,0 |
| Бета - лактоглобулин | 7-12 | 5,3 | |
| Альфа – лактальбумин Альбумин сыворотки крови | 2-5 0,7-1,3 | 4,2-4,5 4,7 | |
| Иммуноглобулины | 1,9-3,33 |
Казеин.
В практике под казеином понимают смесь белков (казеинов), осаждаемых из обезжиренного молока при подкислении до рН=4,6. Очищенный казеин, выделенный из молока, представляет собой аморфный белый порошок без запаха и вкуса, практически нерастворимый в воде. Он может быть разделен на фракции, различающиеся по составу и свойствам. При помощи электрофореза на крахмальном или полиакриламидном геле его можно разделить на компоненты – фракции казеина. Эти компоненты имеют несколько генетических вариантов, молекулярную массу 19000-24000 и отличаются друг от друга электрофоретической подвижностью, аминокислотным составом, а также содержанием остатков фосфорной кислоты.
В молоке молекулы казеина образуют мицеллы глобулярной формы, каждая мицелла содержит в себе все виды казеина и состоит из 7000-8000 полипептидных цепей, соединенных между собой катионами Са 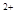 . На периферии мицелл расположен каппа – казеин, выполняющий роль защитного коллоида. От каппа - казеина при этом отщепляется гликомакропептид, после чего нарушается структура мицелл и происходит створаживание молока. Причиной створаживания является то, что каппа - казеин, потеряв под действием фермента гидрофильный гликомакропептид, образует нерастворимые соли с ионами кальция даже в нейтральной среде, чего не происходит при нативном состоянии белка в молоке.
. На периферии мицелл расположен каппа – казеин, выполняющий роль защитного коллоида. От каппа - казеина при этом отщепляется гликомакропептид, после чего нарушается структура мицелл и происходит створаживание молока. Причиной створаживания является то, что каппа - казеин, потеряв под действием фермента гидрофильный гликомакропептид, образует нерастворимые соли с ионами кальция даже в нейтральной среде, чего не происходит при нативном состоянии белка в молоке.
При рН. свежего молока (рН=6,6) казеин имеет отрицательный заряд. Носителями отрицательных зарядов и кислых свойств казеина являются карбоксильные группы аспарагиновой и глютаминовой кислот, носителями положительных зарядов и основных свойств - аминогруппы лизина, гуанидиновые группы аргинина и имидазольные группы гистидина. Равенство положительных и отрицательных зарядов (ИЭТ - изоэлектрическая точка) наступает при рН 4,6-4,7. Следовательно, в составе казеина преобладают дикарбоновые кислоты. Кроме того, отрицательный заряд и кислые свойства казеина усиливают гидроксильные группы фосфорной кислоты.
Синтез казеина осуществляется в молочной железе из доставляемых в нее кровью аминокислот и фосфатов.
Казеин - это фосфопротеид, в его состав входят фосфорная кислота, присоединенная моноэфирной связью к остаткам серина.

Полярные группы, находящиеся на поверхности и внутри казеиновых мицелл (СООН, ОН и др.), связывают значительное количество воды – около 3,7 г на 1 г белка. Способность казеина связывать воду характеризует его гидрофильные свойства. Гидрофильные свойства казеина зависят от структуры, величины заряда белковой молекулы, рН среды, концентрации солей и других факторов. Они имеют большое практическое значение.
От гидрофильных свойств казеина зависит устойчивость казеиновых мицелл в молоке (связанная вода образует вокруг казеиновых мицелл защитную гидратную оболочку). Сильными гидрофильными свойствами обладают макропептиды и гликомакропептиды каппа – казеина казеиновых мицелл. Поэтому при отщеплении под действием сычужного фермента (или высоких температур) нарушается гидратная оболочка и уменьшается стабильность казеиновых частиц.
В процессе высокотемпературной обработки молока происходит взаимодействие денатурированного бета – лактоглобулина с казеиновыми мицеллами. Сывороточные белки молока обладают большей гидрофильностью по сравнению с казеином, в результате чего повышается его водоудерживающая способность. В свою очередь, гидрофильные свойства казеина влияют на способность кислотного и кислотно-сычужного сгустка удерживать и выделять влагу. Изменение гидрофильных свойств казеина необходимо учитывать при выборе режима пастеризации в процессе производства кисломолочных продуктов и молочных консервов. От гидрофильных свойств казеина и продуктов его распада зависят водосвязывающая и влагоудерживающая способность сырной массы при созревании сыров, консистенция готового продукта. Следовательно, гидрофильные свойства казеина не только определяют устойчивость белковых частиц в молоке при его обработке, но и влияют на ход некоторых технологических процессов.
Таким образом, казеин, содержащий различные реакционноспособные группы, может образовывать целый ряд соединений со многими химическими веществами: кислотами, основаниями, альдегидами, металлами, галогенами и др.
При реакции казеина с формальдегидом происходит блокирование основных аминогрупп, что приводит к увеличению кислых свойств казеина. Эту реакцию применяют при определении содержания белков в молоке методом формольного титрования.
Свободные аминогруппы могут взаимодействовать с альдегидными группами лактозы и других сахаров с образованием аминосахарного комплекса (реакция меланоидообразования или побурение молока при повышении температуры). Эта реакция происходит во время первой стадии реакции Майара.
Карбоксильные и другие кислые группы казеина вступают в реакцию с ионами металлов, образуя казеинаты. При йодировании тирозина, входящего в состав белка, образуется йодказеин, который сейчас широко применяют в молочной промышленности для ликвидации йодной недостаточности населения.
Казеинаткальцийфосфатный комплекс.
В молоке казеин содержится в виде казеината кальция, соединенного с коллоидным фосфатом кальция в форме так называемого казеинаткальцийфосфатного комплекса (ККФК), образующего мицеллы почти сферической формы, состоящие из субмицелл и имеющего размеры от 40 до 300 нм.
Казеинат кальция образуется при взаимодействии ионов кальция с карбоксильными и серинфосфатными группами казеина. При этом кальций может реагировать с одной или двумя СООН и ОН - группами, например


Фосфат кальция соединяет между собой молекулы казеината кальция наподобие кальциевых мостиков между расположенными друг против друга серинфосфатными группами двух молекул
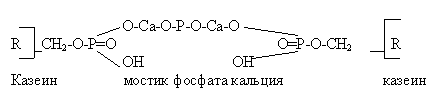
ККФК стабилен в свежем молоке. Он сохраняет свою устойчивость при тепловой и механической обработке молока. Однако в процессе высокотемпературной обработки может происходить необратимая минерализация ККФК, а при выработке кисломолочных продуктов и сыра - наоборот, его деминерализация. При этом наблюдается нарушение мицеллярной и субмицеллярной структуры казеинаткальцийфосфатного комплекса.
Сывороточные белки.
После осаждения казеина в сыворотке молока остается 15-22% всех белков, которые называют сывороточными. Главными из них являются: альфа - лактоглобулин, бета - лактоглобулин, иммуноглобулины и компоненты протеозопептонной фракции. Кроме них, в сыворотке содержатся лактоферрин, ферменты и другие минорные компоненты. Сывороточные белки по содержанию дефицитных незаменимых аминокислот (лизина, триптофана, метионина, треонина) и цистеина являются наиболее биологически ценной частью белков молока, поэтому их использование для пищевых целей имеет большое практическое значение.
Бета- лактоглобулин
На его долю приходится около половины всех сывороточных белков (или 7-12% общего количества белков). В молоке находится в виде димера, состоящего из двух полипептидных цепей с молекулярной массой около 18000 каждая. При нагревании молока до температуры выше 30  С бета- лактоглобулин распадается на мономеры, которые при дальнейшем нагревании агрегируют за счет образования дисульфидных связей.
С бета- лактоглобулин распадается на мономеры, которые при дальнейшем нагревании агрегируют за счет образования дисульфидных связей.
Денатурированный в процессе пастеризации бета - лактоглобулин образует комплексы с каппа - казеином и осаждается вместе с ним при сычужной и кислотной коагуляции казеина. В денатурированном состоянии он также препятствует створаживанию молока, поэтому молоко, предназначенное для получения творога, нельзя перегревать.
Бета - лактоглобулин в нативном состоянии обладает способностью связывать катионы, анионы, липидные соединения и т.п. В кислой среде желудка лактоглобулин устойчив к действию пепсина и химозина. Одной из его биологических функций может быть транспортирование в кишечник важных для растущего организма кислотно-неустойчивых веществ.
альфа - лактальбумин занимает второе место по количественному содержанию (2-5% от общего количества белков в молоке). Он является субъединицей лактозосинтетазы секретирующих клеток молочной железы. В молоке альфа - лактальбумин находится в тонко диспергированном состоянии (размер частиц 15-20 нм). Он не коагулирует в изоэлектрической точке (при рН 4,2-4,5) в силу своей большой гидратированности, не свертывается под действием сычужного фермента. Он термостабилен, так как в молекуле много дисульфидных связей. Биологическая роль заключается в том, что 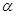 - лактоглобулин является специфическим белком, необходимым для синтеза лактозы из галактозы и глюкозы.
- лактоглобулин является специфическим белком, необходимым для синтеза лактозы из галактозы и глюкозы.
Иммуноглобулины.
В обычном молоке иммуноглобулинов содержится очень мало (1,9-3,3% общего количества белка). В молозиве они составляют основную массу до 90%) сывороточных белков. Это гликопротеиды, выполняющие функцию антител. Иммуноглобулины молока обладают резко выраженными свойствами агглютинации - склеивания микробов, чужеродных клеток, а также шариков жира. Из молозива и молока выделены три основные группы иммуноглобулинов А, М и G.
Протеозопептонная фракция - наиболее термостабильная часть сывороточных белков. Протеозопептоны не осаждаются из обезжиренного молока при рН=4,6 после нагревания до 95-100  C в течение 20 минут. Они составляют около 24% сывороточных белков и 2-6% всех белков молока. Протеозопептонная фракция неоднородна по составу.
C в течение 20 минут. Они составляют около 24% сывороточных белков и 2-6% всех белков молока. Протеозопептонная фракция неоднородна по составу.
Лактоферрин. Это красный железосвязывающий белок, по своим свойствам похожий на трансферрин крови, но отличающийся аминокислотной последовательностью цепи. Лактоферрин представляет собой гликопротеин с молекулярной массой около 77000, обладает бактериостатическим действием по отношению к  группе бактерий кишечной палочки
группе бактерий кишечной палочки
Небелковые азотистые соединения представляют собой промежуточные и конечные продукты азотистого обмена в организме животных и попадают в молоко непосредственно из крови. Важнейшими компонентами фракции небелкового азота молока являются: мочевина, пептиды, аминокислоты, креатин и креатинин, аммиак, оротовая, мочевая и гиппуровая кислоты. Их общее количество составляет около 5% всего содержания азота в молоке.
Мочевина является главным конечным продуктом азотистого обмена у животных. Нормальное содержание мочевины в крови и молоке составляет 15-30 мг %. Увеличение количества мочевины наблюдается в весенне-летний период при избыточном потреблении животными белков с зеленым кормом.
Пептиды и аминокислоты относятся к промежуточным продуктам азотистого обмена. Эти соединения молока являются одним из основных источников азотистого питания микроорганизмов заквасок. Поэтому наблюдаемое весной ослабление развития молочнокислых бактерий может быть обусловлено низким содержанием в молоке свободных аминокислот. В молоке весеннего периода понижено содержание таких важных для молочнокислых бактерий аминокислот, как аргинин, валин, метионин, фенилаланин и тирозин.
Креатин, креатинин и аммиак. Их общее количество в молоке не превышает 2,5 - 4,5 мг %. В свежевыдоенном молоке содержание аммиака невысокое (азот аммиака составляет 0,3-1 мг %), но оно может повышаться при хранении, вследствие развития посторонней микрофлоры.
Оротовая, мочевая и гиппуровая кислоты. Оротовая кислота образуется в процессе синтеза пиримидиновых азотистых оснований (урацила, цитозина, тимина). Ее содержание в молоке составляет 2-8 мг %
Мочевая и гиппуровая кислоты являются конечными продуктами азотистого обмена и в сумме их содержание не превышает 0,7-1,5 мг %.
2.3. Ферменты молока
Из молока, полученного при нормальных условиях от здорового животного, выделено более 20 ферментов. Некоторые из них специально секретируются клетками молочной железы для оказания помощи новорожденному в усвоении питательных веществ молока.
Кроме ферментов, которые синтезируются непосредственно в секреторных клетках молочной железы, или поступают в молоко изкрови животного, в молоке также присутствуют многочисленные ферменты, продуцируемые микрофлорой молока и бактериальных заквасок.
Оксидоредуктазы.
К ним относятся, например, дегидрогеназы (лактатдегидрогеназа, малатдегидрогеназа, глюкозо-6-фосфат, ДГ, цитохром-С-редуктазы). Многочисленные дегидрогеназы (редуктазы) накапливаются в сыром молоке при размножении в нем бактерий. Поэтому бактериальную обсемененность молока можно проверить так называемой редуктазной пробой (по продолжительности восстановления — обесцвечивания добавленного к молоку метиленового голубого). Дегидрогеназы, вырабатываемые молочнокислыми бактериями бактериальных заквасок принимают активное участие в молочнокислом и спиртовом брожениях. Так, образование молочной кислоты из ПВК происходит при участии ЛДГ, образование спирта из уксусного альдегида - с участием алкогольдегидрогеназы.
Оксидазы.
К оксидазам молока относятся ксантионоксидаза, являющаяся ФАД - содержащим ферментом, катализирующим окисление молекулярным кислородом пуриновых оснований - гипоксантина и ксантина до мочевой кислоты, а также различных альдегидов до соответствующих карбоновых кислот.
Пероксидаза синтезируется клетками молочной железы. Часть пероксидазы может освобождаться из лейкоцитов. Содержится в молоке в больших количествах (30-100 мг/л), обладает антибактериальными свойствами. Лактопероксидаза довольно термостабильна, инактивируется при температуре около 80  С, обладает способностью к реактивации. Фермент катализирует окисление различных органических соединений перекисью водорода, но может окислять и некоторые неорганические соединения, например, иодид калия:
С, обладает способностью к реактивации. Фермент катализирует окисление различных органических соединений перекисью водорода, но может окислять и некоторые неорганические соединения, например, иодид калия:
Данную реакцию используют в молочной промышленности для контроля эффективности пастеризации молока (проба на пероксидазу молока).
Каталаза вырабатывается клетками молочной железы. В свежем молоке каталазы мало. В молоке, полученном от больных животных (мастит, и другие заболевания вымени), ее количество резко увеличивается. Поэтому определение активности каталазы используют как метод обнаружения молока, полученного от больных животных.
Липаза катализирует гидролиз триглицеридов молочного жира. Этот фермент связан главным образом с казеином и иммуноглобулинами (плазменная липаза) и лишь небольшая его часть (1-10%) адсорбирована оболочками шариков жира (мембранная липаза).
В молоке, склонном к прогорканию, происходит перераспределение липазы с белков на оболочку шариков жира. При этом наступает гидролиз жира, выделяются жирные кислоты (масляная, капроновая, каприловая и др.) и молоко прогоркает. Спонтанное прогоркание молока характерно для стародойного и маститного молока.
Липазы выделяются также микрофлорой молока. В некоторых сырах (рокфор, камамбер) липазы микроскопических грибов обеспечивают образование специфического вкуса и аромата, который формируется в результате выделения летучих жирных кислот при разложении сыра.
Фосфатазы. Щелочная фосфатаза концентрируется на оболочках шариков жира. Фермент катализирует гидролиз большого числа различных эфиров фосфорной кислоты с образованием неорганического фосфора.
Щелочная фосфатаза молока чувствительна к повышенной температуре и полностью инактивируется при 72-74  С, что положено в основу метода контроля эффективности пастеризации молока (фосфатазная проба).
С, что положено в основу метода контроля эффективности пастеризации молока (фосфатазная проба).
Лактаза катализирует реакцию гидролитического расщепления лактозы на моносахариды (галактозу и глюкозу). Клетки молочной железы лактазу практически не синтезируют, ее вырабатывают молочнокислые бактерии.
Фермент применяют при выработке гидролизованной молочной сыворотки, используемой в пищевой промышленности (хлебобулочной, кондитерской).
Амилаза катализирует расщепление полисахаридных цепей крахмала с образованием декстринов и мальтозы. Фермент инактивируется при пастеризации.
Лизоцим (мурамидаза ) катализирует гидролиз ацетилмурамовой кислоты и ацетилглюкозамина в полисахаридах клеточных стенок некоторых видов бактерий. Лизоцим обусловливает бактерицидные свойства молока. Его содержится около 13 мкг в 100 мл. Больше всего лизоцима содержится в коровьем молоке.
Протеиназы. В молоке содержатся разнообразные нативные и бактериальные протеиназы. Они катализируют гидролиз пептидных связей белков молока, в основном бета - казеина с образованием гамма - казеинов и некоторых компонентов протеозопептонной фракции.
Микрофлора молока выделяет активные протеиназы, которые могут вызывать различные пороки молока и молочных продуктов.
При производстве творога и сыров для свертывания молока применяют сычужный фермент, содержащий кислые протеиназы: химозин или реннин. Обе протеиназы содержат в активном центре карбоксильные группы аспарагиновой кислоты, обладают молокосвертывающей, протеолитической и пептидазной активностью.
2.4 Липиды молока
Липидная фракция молока является источником биологически ценных полиненасыщенных жирных кислот и жирорастворимых витаминов.
Молочный жир.
Содержание жира в молоке колеблется от 2,8 до 5%. Главный компонент жира молока - триглицериды.
Триглицериды составляют основную массу жира молока (99%). Фосфолипиды, гликолипиды, стерины входят в состав липопротеидных оболочек шариков жира и частично связаны с белками молочной плазмы.
Молекула жира состоит из нескольких тысяч триглицеридов. Триглицериды главным образом разнокислотные. Кислотный состав в триглицеридах регулируется в процессе синтеза молочного жира специальными ферментными системами.
В триглицеридах молочного жира обнаружено 140 жирных кислот с числом атомов углерода от 4 до 26. Однако главных (около 5%) всего 10-12, остальные - минорные.
В составе триглицеридов жира преобладают насыщенные жирные кислоты: масляная, капроновая, каприловая, каприновая, лауриновая, миристиновая, пальмитиновая, стеариновая; их общее содержание колеблется от 58 до 77%. Летом их количество меньше, зимой больше; ненасыщенных - наоборот. Это связано с различиями в кормовых рационах и физиологическими особенностями организма. Среди ненасыщенных - пальмитоолеиновая, олеиновая, линолевая, линоленовая, арахидоновая.
Фосфолипиды. Содержание фосфолипидов в молоке составляет 0,03-0,05%, их них на долю лецитина приходится 28-40%, кефалина — 29-43%, сфингомиелина - 19-24%, фосфатидинсерина - 10%, цереброзидов - 6%.
Фосфолипиды обладают эмульгирующей способностью, так как их молекулы построены из двух частей – полярной (гидрофильной) и неполярной (гидрофобной). Фосфолипиды формируют оболочку шариков жира. На поверхности раздела жир - плазма они ориентируются неполярной частью к жиру, полярной - к плазме.
Стерины принадлежат к веществам, сопутствующим жиру молока и представлены в основном холестерином. Их общее содержание в жире молока 0,2-0,4%. Холестерин находится главным образом в свободном состоянии и около 5-10% их общего количества - в виде эфиров жирных кислот.
Жирорастворимые пигменты. Желтая окраска молочного жира обусловлена наличием в нем каротиноидов и каротинов. Содержание каротинов в молоке колеблется от 0,05 до 0,09 мг/кг, летом их значительно больше.
Физико-химические свойства молочного жира.
Физико-химические свойства жиров определяются свойствами входящих в их состав жирных кислот. Для их характеристики служат так называемые константы, или физические и химические числа жиров. К важнейшим физическим числам относят температуру плавления и отвердевания, число рефракции, к химическим – число омыления, йодное число, число Рейхерта-Мейссля и число Поленске.
Температурой плавления жира считают температуру, при которой он переходит в жидкое состояние (и становится совершенно прозрачным). Молочный жир является смесью триглицеридов с различными температурами плавления, поэтому его переход в жидкое состояние происходит постепенно.
Температура отвердевания – температура, при которой жир приобретает твердую консистенцию.
Число рефракции характеризует способность жира преломлять луч света, проходящий через него. Чем больше в жире ненасыщенных и высокомолекулярных жирных кислот, тем выше коэффициент преломления, или число рефракции.
Число омыления определяется количеством миллиграммов гидроксида калия, которое необходимо для омыления 1 г жира. Оно характеризует молекулярный состав жирных кислот жира – чем больше в нем содержится низкомолекулярных кислот, тем оно выше.
Йодное число показывает содержание в жире ненасыщенных жирных кислот. Оно выражается в граммах йода, которые связываются 100 г жира. Йодное число молочного жира зависит от стадии лактации, сезона года, кормов. Оно повышается летом и понижается зимой.
Число Рейхерта-Мейссля характеризует содержание в жире летучих, растворимых в воде жирных кислот (масляной и капроновой). Молочный жир, в отличие от других жиров, имеет высокое число Рейхерта-Мейссля. Поэтому по его величине судят о натуральности молочного жира (а также при количественном определении состава продуктов с комбинированной жировой фазой). Для точного контроля фальсификации молочного жира необходимо проведение газохроматографического анализа жирнокислотного состава жира.
Число Поленске показывает количество в жире летучих, нерастворимых в воде жирных кислот
(каприловой, каприновой и частично лауриновой).
2.5. Углеводы молока
В молоке содержатся моносахариды (глюкоза, галактоза), их производные и дисахарид - лактоза (молочный сахар).
Часть моносахаридов связана с белками молока. Производные моносахаридов - фосфорные эфиры и аминопроизводные - содержатся в молоке в свободном и связанном состояниях. Аминопроизводные сахаров входят в состав углеводной части гликопротеидов молока - казеинов, иммуноглобулинов, лактоферрина и других.
Сладковатый вкус молоку придает содержащаяся в нем лактоза. На ее долю приходится 30% энергетической ценности молока. Один из его компонентов (глюкоза) является источником синтеза гликогена для новорожденного, а галактоза необходима для синтеза ганглиозидов мозга
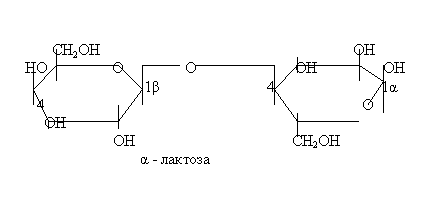
Лактоза нормализует кишечную флору новорожденных. Содержание лактозы в молоке довольно постоянно и составляет 4,5-5,2%. Оно зависит от индивидуальных особенностей животных. В виде готового продукта ее используют в пищевой промышленности и при производстве антибиотиков. Резкое снижение количества лактозы наблюдается при заболевании коров маститом.
Гидролиз лактозы осуществляется с помощью фермента лактазы (бета-галактозидазы), получаемой из дрожжей. Образующаяся при сбраживании лактозы бактериями желудочно-кишечного тракта молочная кислота способствует усвоению кальция и фосфора.
2.6. Минеральные вещества
Минеральные вещества в молоке представлены главным образом фосфатами и хлоридами щелочных и щелочноземельных металлов. Значительно меньше в молоке гидрокарбонатов, сульфатов и цитратов, они поступают в организм животных и переходят в молоко из кормов и минеральных добавок. Поэтому их количество находится в прямой зависимости от рациона кормления, окружающей среды (состава воды и почвы), времени года.
Макроэлементы.
Наиболее важными являются кальций и фосфор, они содержатся в молоке в легкоусвояемой форме. Около 22% всего кальция молока прочно связано с казеином (Са структурообразующий), остальное количество (78%) - это соли (фосфаты, цитраты и др.). Фосфаты кальция могут находиться в молоке в виде Са 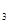 (Р0
(Р0 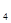 )
) 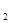 , СаНР0
, СаНР0 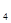 , Са (Н
, Са (Н 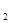 Р0
Р0 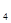 )
) 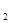 , Са
, Са 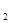 (С
(С 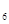 Н
Н 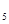 0
0 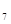 ). Большая часть этих солей содержится в коллоидном состоянии и лишь треть - в виде истинного раствора. Соотношение их форм играет важную роль в поддержании гидратации белковых частиц, их стабилизации при тепловой обработке и прохождении сычужного свертывания.
). Большая часть этих солей содержится в коллоидном состоянии и лишь треть - в виде истинного раствора. Соотношение их форм играет важную роль в поддержании гидратации белковых частиц, их стабилизации при тепловой обработке и прохождении сычужного свертывания.
Общее содержание фосфора колеблется в пределах 74-130 мг %. Может содержаться в виде неорганических (фосфаты кальция) и органических (фосфолипиды, нуклеиновые кислоты, коферменты) соединений.
Количество магния в молоке составляет 12-14 мг %.
Содержание калия, натрия и хлора - 135-160, 30-60, и 90-120 мг % соответственно. Соли калия и натрия содержатся в молоке в ионно-молекулярном состоянии в виде хорошо диссоциирующих хлоридов, фосфатов и цитратов. Они имеют большое физиологическое значение. Хлориды натрия и калия обеспечивают определенную величину осмотического давления крови и молока. Их фосфаты и карбонаты входят в состав буферных систем организма.
Количество цитратов в молоке — важный показатель его биологической активности. Они необходимы для развития ароматобразующих бактерий.
Микроэлементы.
Их концентрация измеряется в микрограммах на 1 кг продукта. Микроэлементы имеют огромное биологическое значение, они обеспечивают активность жизненно важных ферментов, витаминов и гормонов. К содержанию в молоке таких микроэлементов как марганец, железо, цинк, кобальт чувствительны многие молочнокислые бактерии, входящие в состав бактериальных заквасок.
В сравнительно больших количествах в молоке содержатся цинк, медь, кремний, алюминий. Внесение микроэлементов с кормом может повысить их содержание в молоке в несколько раз.
2.7. Витамины молока
Молоко содержит практически все витамины, необходимые для нормального развития новорожденного в первые недели его жизни. Большинство их поступает с кормом и синтезируется микрофлорой рубца. Зависимость содержания витаминов от состава кормов характерна особенно для жирорастворимых витаминов: A, Д, Е и К. Их содержание в молоке в летний период увеличивается в 4-8 раз, когда животные поедают в большом количестве зеленый корм.
К водорастворимым витаминам относятся витамины группы В, аскорбиновая кислота и другие:
В 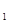 (тиамин) - 0,2-0,8 мг/кг. Синтезируется микрофлорой кишечника и поступает с кормом.
(тиамин) - 0,2-0,8 мг/кг. Синтезируется микрофлорой кишечника и поступает с кормом.
В 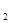 (рибофлавин) - 1,2,8 мг/кг. Желто-зеленый пигмент, обусловливает окраску молочной сыворотки.
(рибофлавин) - 1,2,8 мг/кг. Желто-зеленый пигмент, обусловливает окраску молочной сыворотки.
РР (никотиновая кислота) - 0,7-1,5 мг/кг. Является коферментом дегидрогеназ.
В 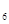 (перидоксин) в молоке животных находится в нескольких формах. Фосфопроизводное этого витамина является коферментом очень важных ферментов класса трансфераз, катализирующих переаминирование аминокислот в клетках молочной железы.
(перидоксин) в молоке животных находится в нескольких формах. Фосфопроизводное этого витамина является коферментом очень важных ферментов класса трансфераз, катализирующих переаминирование аминокислот в клетках молочной железы.
Пантотеновая кислота является фактором роста для молочнокислых бактерий. Молоко содержит 2-3,8 мг/кг этого витамина.
Биотин (витамин Н) также необходим для развития молочнокислых бактерий. Недостаток пантотеновой кислоты и биотина весной - причина замедленного развития молочнокислых бактерий заквасок.
Витамин С синтезируется в организме животных из глюкозы и микрофлорой рубца, ее содержание составляет 3-20 мг %.
2.8. Гормоны молока
В молоко из крови переходят как эндогенные, так и экзогенные гормоны (препараты, применяемые для стимулирования молочной продуктивности и других целей). По химическому строению они относятся к различным классам.
Гормоны пептидной природы представлены пролактином, окситоцином, тиролиберидином. Последние два (рилизинг-факторы, или факторы высвобождения) вырабатываются гипоталамусом и поступают в гипофиз, где стимулируют образование гонадотропных и тиреотропных гормонов.
Стероидные гормоны: кортикостероиды (кортизол, кортикостерон) - способствуют развитию молочной железы; андрогены (андростендион, тестестерон) 0,5-0,15 х 10 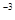 мкг/мл., эстрогены (эстрадиол, эстрон), прогестерон - применяют в ветеринарной практике для стимуляции родов и лактации (1-2) х 10
мкг/мл., эстрогены (эстрадиол, эстрон), прогестерон - применяют в ветеринарной практике для стимуляции родов и лактации (1-2) х 10 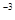 мкг/мл.
мкг/мл.
|
|
|
|
|
Дата добавления: 2014-12-17; Просмотров: 11633; Нарушение авторских прав?; Мы поможем в написании вашей работы!