
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Матеріальний і тепловий баланс процесу горіння
|
|
|
|
В результаті вивчення теми слухачі повинні
Знати:
· види горіння, основні параметри, що характеризують процес горіння;
· будову полум’я та процеси, що відбуваються в зонах полум’я;
· умови, що необхідні для виникнення горіння, та види виникнення горіння: самоспалахування, самозаймання, вимушене займання (спалахування);
Вміти:
· складати рівняння реакції горіння індивідуальних горючих речовин;
· розраховувати інтенсивність світіння полум’я при горінні різних горючих речовин, матеріалів, сумішей.
Література:
4 С. 7 – 29.
5 Частина 1. С. 14 -28.
Виконуючи розрахунки процесу горіння, потрібно враховувати, що методика розрахунку залежить від складу і агрегатного стану речовини. Розрахунок об’ємів повітря і продуктів горіння для складних речовин визначається за допомогою спеціальних таблиць.
Визначаючи об’єм повітря, враховується, що горіння може проходити з надлишком повітря α. При розрахунку об’єму продуктів горіння враховується і об’єм повітря, який не приймає участь в горінні (α – 1), а також теплове розширення продуктів горіння. Перерахунок ведеться за універсальним газовим законом.
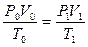 |
Продукти горіння - це різні за агрегатним станом продукти, які утворюються при гонінні за рахунок окислення киснем повітря або іншими окисниками горючих речовин.
Знаючи кількість і склад продуктів горіння можна провести розрахунки:
- для отримання процесу горіння методом герметизації;
- для розрахунку температури горіння;
- для розрахунку температури вибуху у вибухонебезпечних апаратах і тиску під час вибуху;
- для розрахунку міцності апаратів, трубопроводів, конструкцій вибухонебезпечних установок та приміщень.
Горючість речовини або матеріалу залежить від кількості тепла, яке виділяється під час його горіння. Цю кількість тепла називають тепловим ефектом реакції горіння. Потрібно знати, що усі реакції горіння проходять з виділенням тепла і тому називаються екзотермічними. Кількість тепла, яке виділяється при згоранні одиниці кількості речовини з утворенням продуктів повного горіння, називається теплотою згорання (кДж/моль, кДж/кг, кДж/м3). Теплота згорання позначається знаком Q і записується в правій частині рівняння зі знаком "мінус". Наприклад:
С + О2 = СО2 - Q
В практиці мають місце реакції, які проходять з виділенням тепла, називаються екзотермічними.
При вивчені теплових ефектів хімічних реакцій необхідно навчитися розрізняти екзотермічні і ендотермічні реакції, і теплові ефекти, які супроводжують ці реакції. Дати визначення теплоті згорання як тепловому ефекту реакцій, який супроводжує цей процес. Вивчити математичний вираз та визначення закону Г.І. Гесса, пояснити даний закон на прикладі реакцій горіння (наприклад, коксу). Показати із досвіду вашої роботи порівняльну пожежну небезпеку речовин, які здатні до екзотермічних і ендотермічних реакцій в умовах пожежі.
Розглядаючи питання визначення питомої теплоти згорання, слід уяснити значення питомої теплоти згорання, для визначення пожежної небезпеки технологічних процесів та виробництв. Необхідно вивчити формулу Д.І.Менделєєва для розрахунку питомої теплоти згорання складних, рідких і твердих речовин:
Qв = 339,4С+1257Н – 108,9(О+N-S) кДж /кг
Qн= 339,4С+1257Н-108,9(О+N-S)-25,1(9Н+W) кДж /кг
Теплота згорання може бути визначена і практичним шляхом за допомогою калориметрів КД-І, В-08М, «Юнкерса» і інших типів.
Теплота згорання використовується при визначенні теплового балансу будь-якого технологічного процесу, при експериментальному визначені температури самонагрівання, розрахунку меж поширення полум’я, температури горіння, групи горючості, питомої теплоти пожежі та інших параметрів.
Питання визначення температури пожежі тісно пов’язане з раніше вивченим матеріалом, тому починати його вивчати потрібно з розгляду теплових ефектів хімічних реакцій і теплоти згорання речовин.
Показати вплив температури горіння на вибір засобів гасіння горючих речовин, організацію гасіння пожежі, поведінку будівельних споруд та матеріалів в умовах високих температур. Необхідно звернути увагу на температуру як фактор, який негативно впливає на працездатність людини.
Частина тепла, яка виділилась в зоні горіння витрачається на нагрівання продуктів горіння. Максимальна температура, до якої нагріваються продукти, горіння, називається температурою горіння.
Необхідно пояснити, який вплив на температуру горіння спричиняють такі фактори, як елементарний склад горючого, вологість матеріалу, коефіцієнт повноти горіння, коефіцієнт надлишку повітря.
Температура горіння в практичній роботі пожежно-рятувальних підрозділах використовується при різних теплотехнічних розрахунках, розрахунку тиску під час вибуху, для вибору засобів гасіння і т.д.
Розрахункове визначення температури горіння ґрунтується на рівнянні теплового балансу. При цій температурі сумарний тепловміст (ентальпія) компонентів проектів горіння дорівнює кількості тепла, яке витрачається на їх нагрівання:
Qпг = ∑ Vпгі . Сpt .Тгор
ni = 1
де: Vпг – об’єм продуктів горіння, м3/кг;
Сpt – середній тепловміст продуктів горіння, кДж/м3;
Тгор – температура горіння, К.
Слід показати методику розв’язання даної задачі відносно температури горіння. Під час розв’язування використовуються таблиці тепловмісту продуктів горіння, закон Г.І. Гесса, формули Д.І. Менделєєва, методика визначення об’єму продуктів горіння.
Відповіді на питання № 7, 8, 11, 13 повинні починатися з визначення величини, яка розглядається.
У відповідях на питання № 5, 6, 9, 10, 12, 14 потрібно привести конкретні приклади розрахунку, відмінні від наведених у підручнику.
Поняття:
Згідно ДСТУ речовини й агломерати, які утворюються в результаті горіння називаються продуктами згорання.
Дим – видима аерозольна система летких продуктів згорання.
Кількість тепла,яка виділяється при хімічній реакції, називається тепловим ефектом реакції.
Згідно ДСТУ, теплотою згорання називається кількість теплоти, яка може виділитися при повному згоранні одиниці маси речовини або матеріалу.
Вищою теплотою згорання QВ називають кількість тепла, що виділяється при повному згоранні 1кг або 1 м3 горючої речовини за умови, що весь гідроген який міститься в ній, згоряє з утворенням рідкої води.
Нижчою теплотою згорання QН називають кількість тепла, що виділяється при повному згоранні 1кг або 1 м3 горючої речовини за умови, що весь гідроген який міститься в ній, згоряє до утворення водяної пари і випаровування вологи горючої речовини.
Та максимальна температура, до якої в процесі горіння нагріваються продукти горіння, включаючи азот, називається температурою горіння.
Калометричною є температура, до якої нагріваються продукти повного горіння за таких умов:
1. Усе тепло, що виділяється, витрачається на нагрів продуктів згорання. Втрати тепла дорівнюють нулю.
2. Початкова температура повітря і горючої речовина дорівнює нулю. (за Цельсієм).
3. Кількість повітря дорівнює теоретично необхідній.
4 Відбувається повне згорання.
|
|
|
|
|
Дата добавления: 2014-11-29; Просмотров: 1329; Нарушение авторских прав?; Мы поможем в написании вашей работы!