
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
L-аминокислота D-аминокислота
|
|
|
|
Оптическая изомерия аминокислот
α-Аминокислоты характеризуются наличием оптической активности,
т. е. они могут вращать плоскость поляризованного света вправо или влево. Это свойство природных аминокислот обусловлено наличием ассиметрического атома углерода или иначе: хирального центра (хиральность от греч. Cheir – рука), т. е. атома углерода с четырьмя различными заместителями.
Все α-аминокислоты, имеющие ассиметричесийй атом углерода, образуют оптические (зеркальные, т. е. которые нельзя совместить) изомеры.
Оптические изомеры принято обозначать латинскими буквами. L - (от лат. Louvus – левый) и D - (от лат dexter – правый).
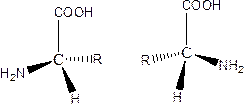
Рис. 1.4. L и D оптические изомеры α-аминокислот
Считают, что кислота относится к L- ряду, если в написании фишеровской проекции аминогруппа расположена слева (рис. 1.4).
Все природные аминокислоты, входящие в состав белков, относятся именно к L- ряду.
Вся белковая жизнь на земле – «левая». Есть и «исключения», но они только подтверждают правило. Оказывается, D-аминокислоты крайне редко, но все же встречаются в природе.
Например, они присутствуют в оболочке бактерии, которая является возбудителем сибирской язвы. Именно поэтому оболочка бактерии не разрушается ферментами, разрывающими белковые цепи L-аминокислот.
Из 20 α - аминокислот, входящих в состав белков:
1) 17 обладают одним ассиметричным атомом углерода;
2) одна не содержит ассиметричного атома углерода: глицин;
3) две имеют два ассиметричных атома углерода: изолейцин и треонин.
1.5.1.3. Классификация α-аминокислот
В настоящее время существуют различные классификации
α-аминокислот.
В зависимости от строения бокового радикала аминокислоты подразделяют на:
1) неполярные (гидрофобные), содержат неполярный гидрофобный радикал (линейную или разветвленную углеводородную цепочку или ароматическое кольцо);
2) полярные (гидрофильные) незаряженные, содержат полярный гидрофильный радикал (полярные группы: -OH; -NH2; -SH);
3) полярные заряженные, содержат заряженный боковой радикал (заряженные группы: -NH3+ и -COO-).
Наиболее распространенные α-аминокислоты приведены на Рис. 1.5:
НЕПОЛЯРНЫЕ АМИНОКИСЛОТЫ 
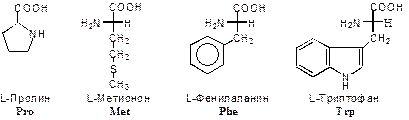
|
|
|
|
|
Дата добавления: 2014-12-07; Просмотров: 9633; Нарушение авторских прав?; Мы поможем в написании вашей работы!