
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Углерод
|
|
|
|
СЕРА
АЗОТ
КИСЛОРОД
Больше половины земной коры как по объему, так и по массе сложено кислородом.
Так как ион кислорода в 3-5 раз больше катионов, то он составляет 93-95 % от объема земной коры. По сути дела, все элементы находятся в атмосфере кислорода.
Сравним:
В 930 г гороха всыпали 70 г пшена, мака и т.д.
Подобным образом устроено и твердое вещество.
Кислород – сильный окислитель. У кислорода на внешней оболочке 6 электронов. Он стремится отобрать 2 электрона, выделив при этом энергию.
Конечно, элементы с 7 электронами на внешней оболочке более мощные окислители (F, Cl, Br, I, At), но их значительно меньше в природе, чем кислорода.
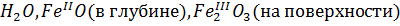
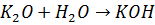
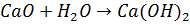
Практически во всех минералах и большинстве органических соединений элементы связаны друг с другом через кислород.
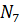
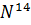
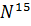
M=14.0067
5 электронов на внешнем уровне.
Кларк 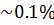
В сухой почве 2-3 %
В живом веществе занимает 4 место (после O, C, H).
Азот образует аминокислоты
Так как азот меняет валентность:
· 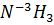
· 
· 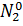
· 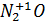
· 
· 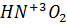
· 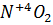
· 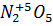
· 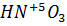
Казалось бы, что азот активен, но это не так. В частности 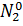 ведет себя как инертный газ.
ведет себя как инертный газ.
Процессы, связанные с азотом:
1) Фиксация атмосферного азота в организмах (немного даже при дыхании)
2) Минерализация (обратный процесс)
N(орг.) àN (неорг.)
3) Нитрификация
Окисление 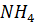 в нитрит
в нитрит 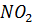 и нитрат
и нитрат 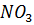
4) Денитрификация
Разложение органического азота до газа 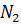
5) Ассимиляция
Превращение: неорганического N в органический N
Энергетический круговорот азота в биосфере подобен биоциклу углерода.
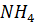 àбелки (N восстановлен, богат энергией) à
àбелки (N восстановлен, богат энергией) à 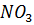 (нуклеиновые кислоты, потеря энергии)
(нуклеиновые кислоты, потеря энергии)
2.5 – 3.5 млрд. лет назад атмосфера была бескислородной и практически целиком состояла из  , как современная атмосфера Венеры (плотная, тяжелая).
, как современная атмосфера Венеры (плотная, тяжелая).
Но азота в объемном отношении было столько же, сколько и сейчас, но не в процентном отношении, т.е.  -тяж.????
-тяж.????
Типы реакций:
1) В бескислородной атмосфере азот образовывал 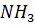 , реагируя с присутствовавшими в атмосфере
, реагируя с присутствовавшими в атмосфере 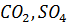 .он мог восстанавливаться до азота атомарного или до
.он мог восстанавливаться до азота атомарного или до 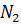 . Возможно, первые органические молекулы начала жизни были цианидами CN
. Возможно, первые органические молекулы начала жизни были цианидами CN
2) Окисление 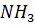 до
до 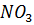 и выделение H
и выделение H
3) Появление N. Азотное дыхание
4) Ассимиляция нитратов – азотное питание (в особенности, бобовыми растениями)
| N | · Азотная панама (прикрытие) |
| · Большая роль в биогенном цикле |
Изотопы:

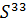
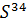
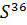
Сера – важнейший биогенный элемент, который передает энергию и способен образовывать вещество.
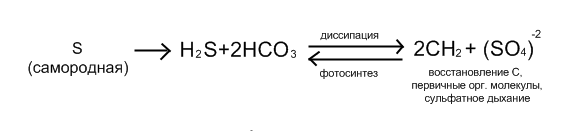
бактерия вдыхает 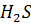 , выдыхает сульфат-ион. Биогенный процесс делит изотопы. В живом веществе концентрируются легкие изотопы. По увеличению количества легких изотопов отбивают первичную серу от вторичной (биогенной).
, выдыхает сульфат-ион. Биогенный процесс делит изотопы. В живом веществе концентрируются легкие изотопы. По увеличению количества легких изотопов отбивают первичную серу от вторичной (биогенной).
Оказалось, биогенная сера появилась в осадках после 2.5 млрд. лет.
Образовавшиеся древнейшие сульфаты(соли 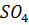 ):
):
Гипс 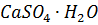
Ангидрид 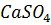
Барит 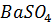
При метаморфизме сульфатов образовался лазурит – продукт синтеза докембрийских сульфатов и силикатов в зоне глубокого метаморфизма:
Лазурит – минерал синего цвета.
2 месторождения:
· На Памире (темно-синий с кристаллами пирита)
· На Байкале
В древности лазурит был ценнейшим камнем.
Природных красок почти нет.
Синий цвет неба и моря получается из «белого» солнечного света, когда пары 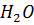 в воздухе поглощают красные лучи.
в воздухе поглощают красные лучи.
Медь à лазурит à малахит
Синий зеленый
Картины богатых художников эпохи Возрождения сохранили свой голубой цвет. Бедные художники применяли в качестве краски лазурит: голубой à зеленый (окисление).
Медь дает голубой цвет. Другие сульфаты имеют биогенное происхождение. Это связано с появлением кислорода в атмосфере.
Ba сроден с Ca и изоморфно с ним сочетается.
Но у Baбольшой радиус катиона. Именно поэтому он выдавливается из кристаллической решетки
Пример: анортит 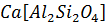
Ba растворим в соединении с Cl (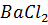 ) и присутствует в растворах вместе с
) и присутствует в растворах вместе с 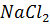 . Но как только Ba встречается с сульфат-ионом, он выпадает в осадок (
. Но как только Ba встречается с сульфат-ионом, он выпадает в осадок (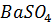 ).
).
Барит может случит указателем на тектонические разломы, т.к. в силу большого размера катиона Ba во время движения он выдавливается в первую очередь.
Ba имеет свойство поглощения 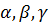 излучения и рентгеновского излучения. Пример: баритовая штукатурка в рентгеновском кабинете, бариевая каша).
излучения и рентгеновского излучения. Пример: баритовая штукатурка в рентгеновском кабинете, бариевая каша).
В последний млрд. лет обогащение серы легкими изотопами достигло равновесия.
Оказалось, в большинстве даже гидротермальных горных пород сера биогенная. Большой процент биогенной серы находится в вулканах, что свидетельствует о том, что и магма нередко оказывается из осадочных горных пород.
Серобактерии едят серу àполучают энергиюàвыделяют 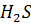 à
à 
 Метеорит «Каньон Дьябло»
Метеорит «Каньон Дьябло»
Существует эталон: метеорит «каньон дьябло» взят за основу по составу свинца и серы.
Изотопный состав первичного свинца был определен по метеоритному веществу, практически свободному от U и Th, исходя из допущения совместного происхождения метеоритов и Солнечной системы. В настоящее время в качестве первичного принят изотопный состав троилита из метеорита Каньон Дьябло.
 В ряде исследований по метеоритам М. Каньон-Дьябло используют в качестве стандартного (напр., при рентгеноспектральном микроанализе никелистого железа М., при масс-спектрометрическом изучении изотопного состава S, не только метеоритной, но и земной и т. п.).
В ряде исследований по метеоритам М. Каньон-Дьябло используют в качестве стандартного (напр., при рентгеноспектральном микроанализе никелистого железа М., при масс-спектрометрическом изучении изотопного состава S, не только метеоритной, но и земной и т. п.).
Для живого вещества важен углерод, который, изменяя свою валентность от +IV до –IV, выделяет большое количество энергии. Углерод является основополагающим элементом, едва ли не самым главным несмотря на то, что он не является самым распространенным элементом в окружающей природной среде.
Валентность IV à громадная энергетика при поглощении и отделении 4 электронов.
Внешняя оболочка достаточно неустойчива.
Эволюция углерода составляет 4.5 млрд. лет. (его геохимическую эволюцию отслеживаем с момента появления живых организмов)
В осадочных породах древнейший возраст углерода составляет 3.8 млрд.лет.
Возраст древнейших бактерий 3.5-3.8 млрд. лет.
Углерода на поверхности всегда было ровно столько же, сколько и в настоящее время.
Общая масса осадочных горных пород 
Органический углерод 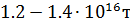
Карбонатный углерод 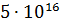
Цикл углерода:
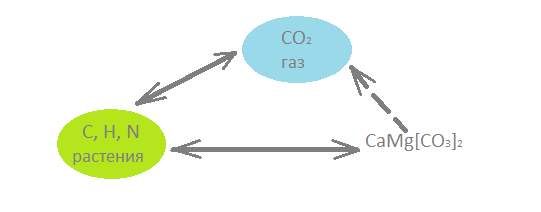
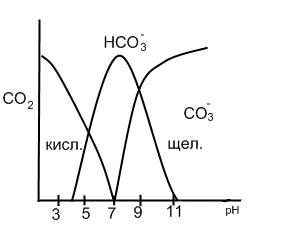
Отношение 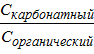 постепенно падает:
постепенно падает:
| Палеозой | |
| Мезозой | 5,2 |
| Кайнозой | 2,9 |
|
|
|
|
|
Дата добавления: 2014-12-07; Просмотров: 508; Нарушение авторских прав?; Мы поможем в написании вашей работы!