
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Общекультурных
|
|
|
|
ЦЕЛЬ ОСВОЕНИЯ ДИСЦИПЛИНЫ
Натрий
Неон
Фтор
Фтор — девятый по счету химический элемент таблицы Менделеева, его атомная масса равна 18,998. Он представляет собой бледно-желтый газ с температурой плавления минус 219,6 и кипения минус 188,1 градусов Цельсия.
Фтор — самый сильный окислитель, он окисляет даже кислород; его химическая активность настолько высока, что он реагирует почти со всеми веществами, за исключением инертных газов: гелия, аргона, неона; при нормальных условиях он не взаимодействует также с азотом и с углеродом в алмазной модификации. При реакциях с его участием выделяется много тепла, иногда это происходит в виде взрыва.
Странное дело, углефторовые соединения — фторопласт и тефлон — отличаются, наоборот, поразительной химической стойкостью: их не берет даже царская водка — концентрированная смесь азотной и соляной кислот. Инертностью отличаются также фреоны (хладоны) — насыщенные углеводороды, в которых водород заменен на фтор и хлор; фреоны являются газами и используются в качестве хладоагентов для холодильников; их температура кипения — около минус 30 градусов Цельсия.
Из других соединений широко известны плавиковая кислота, молекула которой состоит из одного атома углерода и одного атома фтора, и природные минералы: флюорит, плавиковый шпат и другие. Свободный фтор в природе не встречается.
Топология атома фтора завершает треугольную тему. После формирования из исходного тора трехлучевой звезды процесс дальнейшего развития атома выбирает иное, чем у азота и кислорода, направление: два лепестка (луча) успевают сблизиться своими концами, на которых расположены присасывающие петли, раньше, чем, сойтись своими основаниями; сблизившиеся петли разворачиваются и слипаются, нейтрализуя друг друга; слипшиеся петли изгибают дугой свои спаренные шнуры и ловят макушками желоб оставшегося одиночного лепестка. В законченном виде атом фтора напоминает летящего гуся с крыльями из завернувшихся лепестков и с вытянутой шеей последнего третьего из них; петля на конце третьего лепестка ассоциируется с клювом, готовым ущипнуть. Отличие от принятого образа будет состоять, скорее всего, в том, что голова гуся не вытянута в струнку, а мечется из стороны в сторону. Новое, фторовское направление в формировании атома обусловлено удлинением лепестков: у фтора они длиннее приблизительно на 1000 эфирных шариков, чем у кислорода, и на 1500, чем у азота, а вся длина шнура атома фтора составляет 35 000 шариков.
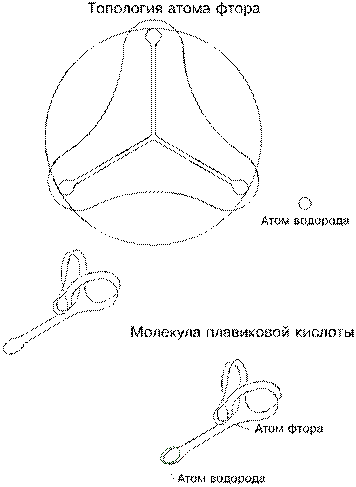
Повышенная активность атома фтора объясняется тем, что он, во-первых, может накапливать на своих присасывающих желобах электронов больше, чем даже атомы кислорода (за счет более длинных желобов, на которых может скопится более 17 000 электронов), а во-вторых, весь этот запас электронов приходится не на два щупальца как у кислорода, а на один клюв. Имея очень длинную шею, атом фтора может дотянуться до самых удаленных слипшихся участков в молекулах других веществ, выбросить на них большую порцию электронов, ослабив тем самым их связи, прилипнуть своей петлей или своим желобом к столкнувшимся атомам или молекулам и образовать новое соединение. Поэтому перед агрессией фтора не может устоять практически ни одно вещество, и поэтому оно называется разрушителем (по гречески “фторос” — разрушение). К слову, разъединительное влияние электронов сказывается и на соединениях самого фтора: если пропустить через плавиковую кислоту электрические разряды, она распадается на водород и фтор.
С другой стороны, удивительную химическую инертность фторопласта и тефлона можно объяснить тем, что в соединениях атомов фтора с атомами углерода нейтрализуются (закрываются) не только присасывающие стороны их петель, но и их присасывающие желоба: и у того и у другого длина каждого из желобов составляет приблизительно 5000 эфирных шариков, поэтому они смыкаются без остатка. Между собой молекулы тетрафторэтилена, образующие фторопласт и тефлон, контактируют отдельными точками, в частности боковушками петель; эти контакты не очень прочны.
С азотом фтор не соединяется по простой причине: молекула азота, как мы знаем, полностью закрыта, и атом фтора бессилен подобрать к ней ключи; к тому же молекула не очень боится его электронных инъекций: у нее у самой имеется большое количество электронов. Также нам должно быть понятно то, что атом фтора не способен разрушить кристаллы алмаза: они так крепко сшиты, что не имеют щелей и прорех, через которые он мог бы проникнуть своим клювом; самое большое, что способен сделать фтор с алмазом, так это прилипнуть к нему, но и это возможно только в том случае, если поверхностные связи кристалла случайно окажутся незавершенными.
В качестве хладоагентов соединения фтора применяют потому, что они имеют очень удобную температуру кипения: давлением компрессора и охлаждением их легко превращать в жидкость, а она, испаряясь, отбирает тепло. К тому же теплоемкость фтора, атом которого имеет консоль, то есть длинную шею, довольно большая. Она — эта теплоемкость — является причиной того, что все реакции с участием фтора идут с выделением тепла: успокаиваясь в соединениях с другими атомами, фтор передает вновь образованным молекулам все свои тепловые движения.
Инертный газ неон занимает в таблице Менделеева десятую позицию: атомная масса неона равна 20,179. Об инертных газах известно только одно: они не способны вступать в химическую реакцию вообще. С одним из таких газов — с гелием — мы уже познакомились: неон — второй из них.
Топология атомов неона открывает новую страницу. Забегая вперед, скажем, что атом неона представляет собой два спаренных атома гелия; и такими же спаренными будут все атомы третьего периода. Отсюда можно сделать вывод о том, что в таблице Менделеева неону больше подходит место в третьем периоде перед натрием. Впрочем, подобную передвижку следовало бы сделать со всеми химическими элементами инертных газов: каждый из них лучше было бы сместить в следующий период и поставить перед первым щелочным металлом.
Исходное кольцо-тор будущего атома неона деформируется уже с четырех сторон; этому способствует длина кольца — она составляет 37 100 эфирных шариков у номинального атома, что на 2 100 шариков больше, чем у фтора. Шнуры выступов сближаются; сами выступы вытягиваются и образуют четырехлучевую звезду; на концах лучей возникают петли. Далее петли попарно сближаются, и фигура приобретает двухчастный вид; полуфигуры разворачиваются на 180 градусов, и в центре между ними возникает перехлест. Столкнувшиеся макушками петли делают полуповорот в разные стороны и взаимно сдвигаются, образуя гелиевые накладки. Завершается топология атома неона тем, что круглые полуфигуры, стягиваемые наружными присасывающими желобами, чуть-чуть поворачиваются вокруг своих осей и успокаиваются, обращенные петлевыми накладками в одну сторону; присасывающие желоба при этом укорачиваются почти до нуля.
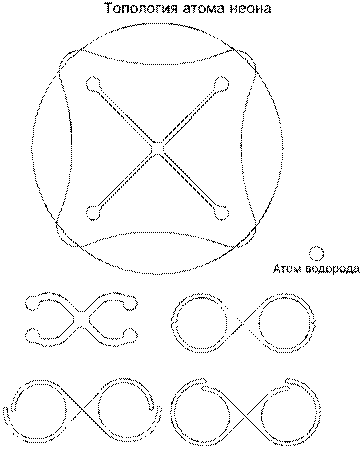
Возникший атом неона пульсирует точно также, как атом гелия; поэтому он такой же пушистый: его температура кипения равна минус 245,9 градуса Цельсия.
Инертность атома неона объясняется тем, что у него практически нет обращенных наружу присасывающих желобов и нет открытых присасывающих сторон петель.
Топология атома первого щелочного металла третьего периода таблицы Менделеева — натрия развивает четырехлучевое направление неона: вместо гелиевых накладок полуфигуры атома натрия образуют литие-бериллиевские сердечки. Они стали возможными потому, что длина шнура атома натрия на 5200 эфирных шариков длиннее, чем у атома неона, и составляет 42 300 шариков.

И так далее.
Целями освоения дисциплины являются обучение студентов пониманию основ правового регулирования отношений в сфере труда в Российской Федерации, умению выявлять тенденции развития законодательства и правоприменительной практики в этой сфере, формирование у обучающихся навыков юридических действий по защите трудовых прав.
Перечисленные результаты образования являются основой для формирования следующих компетенций:
осознает социальную значимость своей будущей профессии, обладает достаточным уровнем профессионального правосознания (ОК-1);
способен добросовестно исполнять профессиональные обязанности, соблюдать принципы этики юриста (ОК-2);
владеет культурой мышления, способен к обобщению, анализу, восприятию информации, постановке цели и выбору путей ее достижения (ОК-3);
способен логически верно, аргументировано и ясно строить устную и письменную речь (ОК-4);
обладает культурой поведения, готов к кооперации с коллегами, работе в коллективе (ОК-5);
имеет нетерпимое отношение к коррупционному поведению, уважительно относится к праву и закону (ОК-6);
стремится к саморазвитию, повышению своей квалификации и мастерства (ОК-7);
способен использовать основные положения и методы социальных, гуманитарных и экономических наук при решении социальных и профессиональных задач (ОК-8);
способен анализировать социально значимые проблемы и процессы (ОК-9);
|
|
|
|
|
Дата добавления: 2014-12-25; Просмотров: 258; Нарушение авторских прав?; Мы поможем в написании вашей работы!