
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Методы контроля качества основных (базисных) гомеопатических препаратов 2 страница
|
|
|
|
б) вещества, пересыщенные растворы которых, соприкасаясь с изоморфным кристаллом, увеличивают его, а сами при этом не кристаллизуются: с помощью пипетки берут несколько миллилитров пересыщенного раствора и осторожно, так, чтобы не смочить край и верхнюю поверхность стенки, помещают в маленькую пробирку, закрываемую резиновой пробкой. С помощью маленького, предварительно прокаленного и полностью охлаждённого платинового шпателя, добавляют к раствору небольшую пробу исследуемого растирания, пробирку закрывают резиновой пробкой, осторожно опрокидывают и оставляют в наклонном положении на несколько часов. Если в пробе были микроскопические изоморфные кристаллы, то через несколько часов на нижней стенке можно заметить некоторое количество выросших кристаллов или друз различной величины. Примером этого класса веществ являются бура и меди сульфат.
Примечание: у растираний веществ, которые в пересыщенных растворах могут вызывать явление перекристаллизации, этот метод можно использовать для проверки приготовления лекарства согласно прописи, т.к. явление перекристаллизации наблюдается и при высоких разбавлениях, например, таких как с 5 до 9 десятичные растирания.
Аналитический контроль* качества основных гомеопатических препаратов по действующим веществам проводят различными методами в зависимости как от природы исходных веществ, так и от того являются ли они фармакопейными или не фармакопейными препаратами.
Фармакопейные аллопатические препараты, которые применяются также в гомеопатии, анализируют на подлинность и количественное содержание по методикам фармакопейных изданий. В качестве примеров можно привести некоторые химические соединения, применяемые для приготовления растворов или порошковых растираний:
|
|
|
меди сульфат (CuSO4 ·5H2O)
подлинность: реакция с железом металлическим (проба на Cu2+);
реакция с аммиаком (проба на Cu2+);
реакция с бария нитратом (проба на SO42–);
количественное определение:
субстанция – йодометрическое определение;
тритурации, дилюции – йодометрическое определение – до Х3;
фотоколориметрически с аммиаком – до Х4;
калия карбонат (K2CO3)
подлинность: реакция с винной кислотой (проба на K+);
реакция с хлороводородной кислотой (проба на CO32-);
количественное определение:
субстанция – кислотно-основное титрование;
тритурации, дилюции до Х3 – кислотно-основное титрование;
потенциометрическое титрование;
прямая потенциометрия;
натрия карбонат (Na2CO3)
подлинность: реакция с цинкуранил ацетатом (проба на Na+);
реакция с хлористоводородной кислотой (проба на CO32-);
количественное определение:
субстанция – кислотно-основное титрование;
тритурации, дилюции до Х3 – кислотно-основное титрование;
потенциометрическое титрование;
прямая потенциометрия;
бура, натрия тетраборат (Na2B4O7 ·10H2O)
подлинность: реакция образования борноэтилового эфира;
количественное определение:
субстанция – кислотно-основное титрование;
тритурации, дилюции до Х3 – кислотно-основное титрование;
потенциометрическое титрование;
прямая потенциометрия;
натрия гидрокарбонат (NaHCO3)
подлинность: реакция с цинкуранил ацетатом (проба на Na+);
реакция с хлористоводородной кислотой (проба на CO32–);
реакция с магния сульфатом (проба на HCO3–);
количественное определение:
субстанция – кислотно-основное титрование;
тритурации, дилюции до Х3 – кислотно-основное титрование;
потенциометрическое титрование;
прямая потенциометрия;
натрия хлорид (NaCl)
подлинность: реакция с цинкуранил ацетатом (проба на Na+);
реакция с серебра нитратом (проба на Cl–);
|
|
|
количественное определение:
субстанция – аргентометрическое определение по Мору;
тритурации, дилюции до Х3 – аргентометрическое титрование;
потенциометрическое титрование;
прямая потенциометрия;
магния сульфат (MgSO4 ·7H2O)
подлинность: реакция с натрия гидрофосфатом в аммиачном буфере (проба на Mg2+);
реакция с бария нитратом (проба на SO42–);
количественное определение:
субстанция – комплексонометрическое титрование;
тритурации, дилюции до Х3 – аналогично;
кислота хлористоводородная (HCl)
подлинность: определение рН (проба на H+)
реакция с серебра нитратом (проба на Cl–);
количественное определение:
субстанция – кислотно-основное титрование;
дилюции до Х3 – кислотно-основное титрование;
потенциометрическое титрование;
кислота уксусная (CH3COOH)
подлинность: определение рН (проба на H+)
реакция со спиртом этиловым (проба на ацетат-ион);
количественное определение:
субстанция – кислотно-основное титрование;
тритурации, дилюции до Х3 – кислотно-основное титрование;
потенциометрическое титрование;
прямая потенциометрия;
железа сульфат (FeSO4 ·H2O)
подлинность: реакция с калия гексацианоферратом (III) K3[Fe(CN)6] (проба на Fe2+);
реакция с бария нитратом (проба на SO42–);
количественное определение:
субстанция – перманганометическое титрование;
тритурации, дилюции до Х3 – аналогично;
серебра нитрат (AgNO3)
подлинность: реакция с хлористоводородной кислотой (проба на Ag+)
количественное определение:
субстанция – прямое тиоцианатометрическое титрование по Фольгарду;
тритурации, дилюции до Х3 – прямое тиоцианатометрическое титрование по Фольгарду;
прямая ионометрия;
железо металлическое (Fe)
получение: восстановление водородом из железа (II) оксида;
подлинность: растворение в серной кислоте и реакция на Fe2+ действием калия гексацианоферрата (III) K3[Fe(CN)6;
количественное определение:
субстанция – растворение в серной кислоте, затем перманганометрическое титрование;
тритурации до Х3 – аналогично.
Если препарат не является фармакопейным, то в качестве субстанций используют химические реактивы квалификации не менее «ч. д. а.». Их качество должно соответствовать ГОСТу на данный химический реактив и подтверждаться стандартными методиками.
Для примера можно привести следующие препараты:
|
|
|
цинк (Zn) марки «ч. д. а.» либо полученный электролизом раствора
цинка сульфата;
подлинность: растворение без остатка в хлористоводородной кислоте;
количественное определение:
субстанция – комплексонометрическое титрование;
тритурации – комплексонометрическое титрование – до Х3;
фотоколориметричеси с дитизоном – до Х5;
серебро (Ag)
подлинность: растворение без остатка в азотной кислоте;
субстанция – растворение в азотной кислоте, затем прямое тиоцианатометрическое титрование по Фольгарду;
тритурации до Х3 – аналогично;
свинец (Pb)
подлинность: растворение без остатка в азотной кислоте;
количественное определение:
субстанция – растворение в азотной кислоте, затем комплексонометрическое титрование;
тритурации до Х3 – аналогично;
кислота азотная (HNO3)
подлинность: определение рН (проба на H+)
реакция с железа сульфатом и серной кислотой (проба на NO3–) или реакция с дифениламином (проба на NO3–);
количественное определение:
субстанция – кислотно-основное титрование;
дилюции до Х3 – кислотно-основное титрование;
потенциометрическое титрование;
кислота серная (H2SO4)
подлинность: определение рН (проба на H+)
реакция с бария нитратом (проба на SO42–);
количественное определение:
субстанция – кислотно-основное титрование;
дилюции до Х3 – кислотно-основное титрование;
потенциометрическое титрование.
В случае отсутствия соответствующих химических реактивов, субстанции получают особыми (специальными) методами. Например:
кальциум карбоникум, кальция карбонат (CaCO3)
получение: белоснежные внутренние чешуйчатые кусочки разбитых раковин превращают в мелкий порошок;
подлинность: растворение в азотной кислоте и реакция с молибденовокислым аммонием (проба на Ca2+);
количественное определение:
субстанция, тритурации – не стандартизуются;
алюмина, обожжённый глинозём (Al2O3)
получение: из криолита или из раствора алюминиево-калиевых квасцов под действием аммиака;
подлинность: щелочное плавление, затем реакция с ализарином (проба на Al3+);
|
|
|
количественное определение:
субстанция, тритурации – не стандартизуются;
калия арсенит (KAsO2·HAsO2·H2O)
получение: реакция мышьяковистого ангидрида с калия карбонатом;
подлинность: реакция с сероводородом, реакция с серебра нитратом (пробы на AsO2–);
количественное определение:
субстанция – иодометрически;
броматометрически;
тритурации до Х3 – иодометрически;
хлористое золото, тетрахлороаурат (III) водорода (H[AuCl4]·H2O)
получение: растворение золота в царской водке (смеси хлороводородной и азотной кислот);
подлинность: реакция с молочным сахаром и раствором формальдегида (проба на Au3+);
количественное определение:
субстанция, дилюции до Х6 – фотоколориметрически с толуидиновым реактивом.
Контроль качества базисных гомеопатических препаратов из растительного сырья (эссенции, настойки) с целью их дальнейшей стандартизации также рекомендуется проводить по содержанию биологически активных веществ. Для этого используют:
Ø качественные реакции на основные группы биологически активных соединений;
Ø хроматографический анализ в различных системах растворителей;
Ø количественное определение инструментальными (газожидкостная хроматография, УФ- и ИК-спектрофотометрия, фотоколориметрия) и другими методами.
Широко распространёнными в растительном сырье классами соединений являются: алкалоиды, кардиотонические (сердечные) гликозиды, флавоноиды, сапонины, дубильные вещества, антраценпроизводные, кумарины, витамины, полисахариды и др. Для обнаружения основных групп биологически активных веществ (БАВ) в растительном сырье и препаратах наиболее часто используют цветные качественные реакции или реакции осаждения.
Алкалоиды обнаруживают следующими общими осадочными реакциями:
þ с реактивом Майера (растворы ртути дихлорида и калия йодида) – бурый осадок;
þ с реактивами Вагнера и Бушарда (растворы йода в растворе калия йодида) – бурый осадок;
þ с реактивом Драгендорфа (раствор висмута нитрата основного, калия йодида и кислоты уксусной) – оранжево-красный или кирпично-красный осадок;
þ с реактивом Марме (раствор кадмия йодида и калия йодида) – белый или желтоватый осадок;
þ с реактивом Зонненшейна (раствор фосфорномолибденовой кислоты) – желтоватый осадок;
þ с раствором кремневольфрамовой кислоты – беловатый осадок;
þ с раствором пикриновой кислоты – жёлтый осадок;
þ с раствором танина –беловатый или желтоватый осадок.
При определении кардиотонических гликозидов проводят цветные реакции на различные фрагменты молекулы:
на стероидную часть молекулы карденолида:
þ реакцию Либермана-Бурхарда (ледяная уксусная кислота, уксусный ангидрид и концентрированная серная кислота) – на границе слоёв окраска от розовой до зелёной и синей;
þ реакция Розенгейма (спиртовый раствор трихлоруксусной кислоты) – окраска от розовой до лиловой и синей;
на бутенолидное (лактонное) кольцо:
þ реакция Раймонда (бензольный раствор м-динитробензола и спиртовый раствор калия гидроксида);
þ реакция Легаля (растворы нитропруссида натрия и натрия гидроксида) – на границе слоёв красное окрашивание в виде кольца;
þ на сахарный компонент:
þ реакция Келлер-Килиани (ледяная уксусная кислота со следами железа сульфата и концентрированная серная кислота) – верхний слой окрашивается в васильково-синий цвет;
þ реакция с реактивом Фелинга – оранжевый осадок после гидролиза.
Последняя из указанных реакций используется также для определения восстанавливающих сахаров.
Наличие флавоноидов устанавливают с помощью таких реакций:
þ цианидиновая проба (порошок металлического магния и концентрированная хлороводородная кислота) – флавоны, флавонолы и флавононы дают красное или оранжевое окрашивание;
þ борно-лимонная реакция – 5-оксифлавоны и 5-оксифлавонолы образуют ярко-жёлтое окрашивание с жёлто-зелёной флуоресценцией;
þ реакция с трёххлористой сурьмой – 5-оксифлавоны и 5-оксифлавонолы дают жёлтое или красное окрашивание;
þ реакции с раствором аммиака или спиртоводным раствором натрия (калия) гидроксида – флавоны, флавонолы, флавононы и флавононолы образуют жёлтое окрашивание, при нагревании переходящее в оранжевое или красное; халконы и ауроны дают сразу красное или пурпурное окрашивание;
þ реакция с хлоридом окисного железа – при наличии полифенолов появляется зеленовато-синее окрашивание;
þ реакция с раствором ванилина в концентрированной хлороводородной кислоте – катехины дают красно-малиновое окрашивание;
þ реакция со средним ацетатом свинца – флавоны, халконы, ауроны, содержащие свободные ортогидроксильные группировки в кольце В, образуют осадки, окрашенные в ярко-жёлтый и красный цвета.
Для обнаружения сапонинов и установления их химической природы используют следующие реакции:
þ проба на пенообразование (в присутствии кислоты и щёлочи) – равная по объёму и стойкости пена образуется в обеих пробирках при наличии тритерпеновых сапонинов; в случае содержания сапонинов стероидной природы в щелочной среде образуется пена в несколько раз больше по объёму и стойкости;
þ реакция со спиртовым раствором холестерина – обе группы сапонинов образуют осадки;
þ реакция с баритовой водой – обе группы сапонинов дают осадки;
þ реакция с растворами ацетата свинца – тритерпеновые сапонины осаждаются средним ацетатом свинца, а стероидные – основным;
þ реакция Либермана-Бурхарда – стероидные сапонины (как и сердечные гликозиды) дают окраску от розовой до зелёной и синей;
þ реакция Лафона (раствор меди сульфата и концентрированная серная кислота) – при нагревании появляется сине-зелёное окрашивание;
þ реакция Сальковского (хлороформ и концентрированная серная кислота) – наблюдается появление окраски от жёлтой до красной;
þ реакция с пятихлористой сурьмой (хлороформный раствор) – появляется красное окрашивание, переходящее в фиолетовое;
þ реакция с раствором натрия нитрата (в присутствии концентрированной серной кислоты) – ярко-красное окрашивание;
þ реакция с ванилином (спиртовый раствор) и концентрированной серной кислотой – появляется красное окрашивание, при разбавлении водой тритерпеноиды образуют синие хлопья.
Наличие кумаринов можно обнаружить с помощью:
þ реакции со щёлочью и диазотированной сульфаниловой кислотой – при нагревании с раствором калия гидроксида раствор желтеет, а после добавления диазотированной сульфаниловой кислоты окраска изменяется от коричнево-красного до вишнёвого цвета;
þ лактонной пробы: после нагревания препарата со спиртовым раствором калия гидроксида, разбавления водой очищенной и добавления хлороводородной кислоты помутнение или выпадение осадка указывает на вероятное наличие кумаринов.
Обнаружение дубильных веществ проводят следующими качественными реакциями:
þ с раствором желатина – образование мути;
þ с раствором хинина гидрохлорида – аморфный осадок;
þ с растворами железо-аммониевых квасцов или хлорида окисного железа появляется окрашивание: чёрно-синее – при наличии гидролизуемых дубильных веществ, и чёрно-зелёное – в присутствии конденсированных;
þ с бромной водой – при наличии конденсированных дубильных веществ сразу образуется осадок;
þ с раствором средней соли свинца ацетата в уксуснокислой среде – осадок выпадает при наличии гидролизуемых дубильных веществ; при добавлении к фильтрату раствора железо-аммониевых квасцов и кристаллического натрия ацетата в присутствии конденсированных дубильных веществ появляется чёрно-зелёное окрашивание;
þ с кристаллическим натрия нитратом в присутствии хлороводородной кислоты – при наличии гидролизуемых дубильных веществ появляется коричневое окрашивание.
Другие классы соединений определяют отдельными специфическими качественными реакциями, описание которых изложено в методических материалах по химическому анализу лекарственных растений (Гринкевич Н. И., Сафронич Л. Н., М, 1983; Ковалёв В. Н., Солодовниченко Н. М., Харьков, 1987).
Для хроматографического анализа алкалоидов используют следующие системы растворителей:
а) для хроматографии на бумаге: н-бутанол – уксусная кислота – вода (5:1:4); этилацетат – уксусная кислота – вода (11:21:85); н-бутанол, насыщенный водой – ледяная уксусная кислота (100:5) и др.;
б) для тонкослойной хроматографии: хлороформ – ацетон – диэтиламин (5:4:1); хлороформ – диэтиламин (9:1); хлороформ – метанол – уксусная кислота (18:1:1); хлороформ – этанол (9:1) или (8:2); ацетон – раствор аммиака (95:5).
Проявителями для хроматограмм служат реактив Драгендорфа, пары йода, хлороформный раствор сурьмы трихлорида.
Обнаружение кардиотонических (сердечных) гликозидов методами ТСХ и хроматографии на бумаге проводят в системах: хлороформ – ацетон – вода (84:15:0,7); хлороформ – бензол – н-бутанол (78:12:5); этилацетат – бензол – вода (84:16:50); бензол – хлороформ (9:1), (7:5) или (3:7).
Для проявления хроматограмм используют реактивы Раймонда (растворы м-динитробензола и калия гидроксида спиртовый) или Йенсена (25%-хлороформный раствор трихлоруксусной кислоты).
Для обнаружения флавоноидов методом хроматографии на бумаге и в тонком слое сорбента рекомендуемые системы растворителей: 15% уксусная кислота; н-бутанол – уксусная кислота – вода (4:1:2); этилацетат – муравьиная кислота – вода (70:15:17) или (10:2:3); метанол – уксусная кислота – вода (18:1:1) и др.
В качестве проявителей используют: 1% спиртовый раствор алюминия хлорида, 10% спиртовый раствор натрия (калия) гидрооксида, пары аммиака в УФ-свете и т. д.
Дубильные вещества методом ТСХ чаще всего анализируют в системе: н-бутанол – уксусная кислота – вода (40:12:28) и обрабатывают 1% раствором ванилина в концентрированной хлороводородной кислоте.
Хроматографирование сапонинов в тонком слое сорбента проводят в системах бензол – метанол (8:2); хлороформ – метанол – вода (61:32:7); изопропанол – вода – хлороформ (30:10:5); хлороформ – метанол (3:1); н-бутанол – этанол – 25% раствор аммиака (7:2:5) и др.
Проявление хроматограмм проводят соответственно парами йода, 20% раствором серной кислоты и 10% спиртовым раствором фосфорновольфрамовой кислоты.
Для анализа кумаринов предлагают такие системы растворителей:
а) для хроматографии на бумаге: петролейный эфир – бензол – метанол (5:4:1);
б) в тонком слое: бензол – этилацетат (2:1); ацетон – гексан (2:8); гексан – бензол – метанол (5:4:1).
Обработку хроматограмм проводят 10% раствором калия гидроксида и диазотированной сульфаниловой кислотой.
Кроме того, методами хроматографии обнаруживают такие классы химических соединений:
каротиноиды – системы: хлороформ – ацетон (9:1); бензол – метанол (1:1) и др.; реактивы для проявления хроматограмм – 10% спиртовый раствор фосфорномолибденовой кислоты, пары йода;
антраценпроизводные –системы: этилацетат – муравьиная кислота – вода (10:2:3), этилацетат – метанол – вода (100:17:13); реактив для проявления хроматограмм – 5% спиртовый раствор гидроксида калия (натрия);
аминокислоты – системы: бутанол – уксусная кислота – вода (4:1:1), этанол – вода (95:5), изопропанол – аммиак – вода (10:1:1), изопропанол – уксусная кислота – вода (7:2:1), н-бутанол – муравьиная кислота – вода (75:15:10); реактив для проявления хроматограмм – 0,2% спиртовый или бутанольный раствор нингидрина.
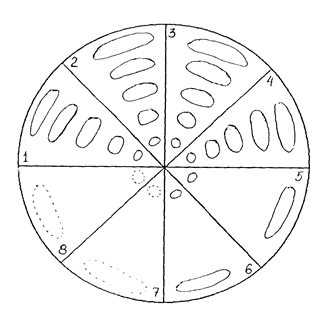
Примеры хроматограмм в тонком слое и на бумаге приведены на рисунке.
| 
| |||
| Примеры схем хроматографии флавоноидов: | ||||
| а) – круговая бумажная хроматография: 1–эссенция туи; 2–тинктура из эссенции; 3–тинктура из свежего сырья; 4–тинктура из сухого сырья; 5–разведение Х2 из тинктуры (из эссенции); 6–разведение Х3 из тинктуры (из свежего сырья); 7–разведение Х3 (тинктура из сухого сырья); 8–гранулы Х3 (тинктура из свежего сырья); | б) – хроматография в тонком слое сорбента: 1–эссенция; 2–тинктура из эссенции; 3–тинктура из свежего сырья; 4–тинктура из сухого сырья; | |||
| Система: 15% уксусная кислота; Проявители: пары аммиака, спирто-водный раствор калия гидроксида, УФ-свет | ||||
Количественное содержание БАВ в матричных настойках и других базисных препаратах в частных статьях фармакопей зарубежных стран указывается лишь в редких случаях, в частности при анализе настоек, содержащих ядовитые и сильнодействующие вещества (аконит, строфант, чилибуха, игнация, белладонна и др.).
В нормативные документы, предназначенные для гомеопатической фармакопеи Российской федерации, включены современные методы анализа, позволяющие осуществлять контроль качества гомеопатических лекарственных средств с учётом содержания БАВ.
Для этой цели можно использовать газожидкостную хроматографию, спектрофотометрию, фотоколориметрию и другие инструментальные методы, в некоторых случаях целесообразно использовать титриметрические методы анализа.
ГЛАВА 8
ЧАСТНАЯ ТЕХНОЛОГИЯ ГОМЕОПАТИЧЕСКИХ
ЛЕКАРСТВЕННЫХ ФОРМ
Все лекарственные средства, используемые в гомеопатической практике для внутреннего и наружного применения, обычно готовят из основных исходных (базисных) препаратов (эссенций, настоек, растворов, тритураций) в точном соответствии с указаниями §§1–9, изложенными в руководстве В. Швабе «Гомеопатические лекарственные средства» (гомеопатическая фармакопея). При описании лекарственных средств, входящих в фармакопею, указывается параграф, согласно которому из этих средств готовятся лекарственные препараты и степень их разведения.
|
|
|
|
|
Дата добавления: 2014-12-25; Просмотров: 862; Нарушение авторских прав?; Мы поможем в написании вашей работы!